In einer Studie, die in Nature Communications veröffentlicht wurde, enthüllen Wissenschaftler im Detail, wie Enzyme, die die DNA kopieren, an der Reparatur dieser Art von Schäden beteiligt sind. Langfristig könnte das tiefgreifende Verständnis der an diesem Mechanismus beteiligten Akteure es ermöglichen, ihn zu manipulieren, um Krebszellen empfindlicher gegenüber Therapien zu machen, deren Wirkmechanismus darin besteht, die DNA zu brechen.
Doppelstrangbrüche der DNA: Eine ständige Bedrohung für unsere Zellen.
Die DNA, die unser genetisches Erbgut ausmacht, wird ständig durch chemische oder physikalische Einflüsse in der Umwelt beschädigt. Eine der schwerwiegendsten Schäden, der Doppelstrangbruch, tritt auf, wenn beide Stränge des DNA-Moleküls gebrochen sind. Diese Schädigung kann für eine Zelle tödlich sein, wenn sie nicht repariert wird.
Doch menschliche Zellen verfügen über einen sehr effizienten Reparaturweg, die nicht-homologe Endverknüpfung (NHEJ). Dieser Mechanismus verbindet die Enden des Bruchs miteinander und kann sogar beschädigte Enden reinigen, um eine perfekte Anpassung vor ihrer Verbindung zu ermöglichen. Es war bereits bekannt, dass bestimmte Enzyme, die die DNA kopieren, die DNA-Polymerasen, an diesem Anpassungsschritt beteiligt sind. Doch ihr genauer Wirkmechanismus blieb unklar.
Eine Schlüsselinteraktion zwischen Ku und den X-Polymerasen enthüllt
In menschlichen Zellen beginnt die NHEJ-Reparatur mit der schnellen Bindung des ringförmigen Ku-Proteinkomplexes an die gebrochenen Enden. Bemerkenswerterweise dient der Ku-Ring als gemeinsamer Ankerpunkt für die verschiedenen Proteinkomplexe, die alle folgenden Schritte der NHEJ sicherstellen.
In einer Studie, die in der Zeitschrift Nature Communications veröffentlicht wurde, haben Wissenschaftler nun aufgeklärt, wie die DNA-Polymerasen der X-Familie an der Reparatur von Doppelstrangbrüchen durch NHEJ beteiligt sind. Diese Studie enthüllt mehrere atomare Strukturen, die durch Kryo-Elektronenmikroskopie gewonnen wurden und die Interaktionen zwischen den X-Polymerasen und Ku an einer DNA-Bruchstelle zeigen. Diese Strukturen zeigen eine spezifische Wechselwirkungsstelle zwischen Ku und der BRCT-Domäne, einem Motiv, das allen X-Polymerasen gemeinsam ist.
Um die Bedeutung dieser Interaktion zu beweisen, führten die Wissenschaftler gezielte Mutationen im Kontaktbereich zwischen Ku und dem BRCT-Motiv ein. Anschließend bewerteten sie die Auswirkungen dieser Veränderungen auf die Fähigkeit der Zellen, DNA-Brüche zu reparieren. Dafür entwickelten sie ein originelles Werkzeug, das die Kopieraktivität an den Enden eines an einer bestimmten Stelle gebrochenen DNA-Moleküls misst, das in die Zellen eingeführt wurde.
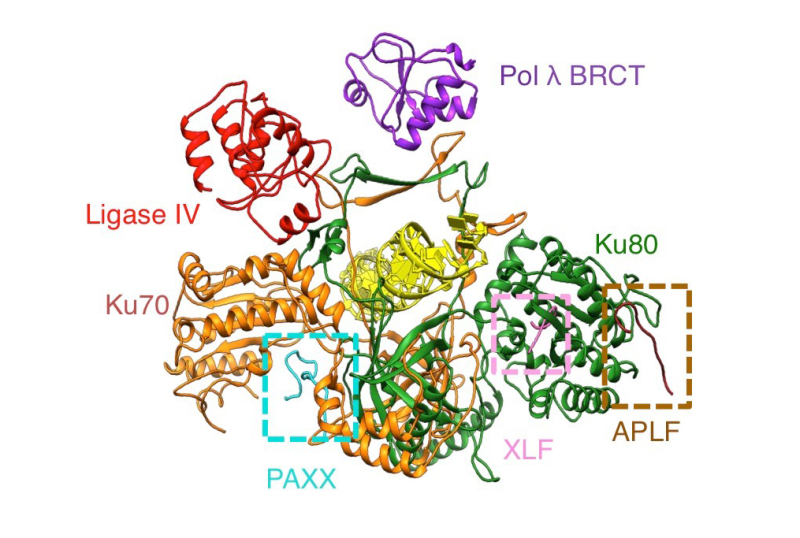
Der Ku70/80-Ring (orange/grün) um die DNA (gelb) dient als Ankerpunkt für die Bindung von Pol λ (BRCT-Domäne, violett), Ligase IV (BRCT1-Domäne, rot), PAXX (P-KBM-Domäne, cyan), XLF (X-KBM-Domäne, rosa) und APLF (A-KBM-Domäne, braun), Proteine, die an der Reparatur von DNA-Doppelstrangbrüchen durch NHEJ beteiligt sind.
© Patrick Calsou
Die Ergebnisse bestätigen, dass die BRCT-Domäne der X-Polymerasen unerlässlich für deren Rekrutierung an den Bruchstellen und ihre Aktivität ist und somit für das Überleben der Zellen bei Doppelstrangbrüchen.
Ein Fortschritt hin zu gezielteren Krebstherapien.
Behandlungen wie Strahlentherapie und andere Krebstherapien zielen darauf ab, in Tumorzellen zahlreiche Doppelstrangbrüche zu induzieren, um einen tödlichen Stress auszulösen. Ein besseres Verständnis des NHEJ-Mechanismus und aller beteiligten Akteure ebnet den Weg für präzisere therapeutische Strategien, die beispielsweise Krebszellen gezielt schwächen können, indem ihre Fähigkeit zur DNA-Reparatur gestört wird.