En un estudio publicado en la revista PNAS, un equipo de investigación del Inserm, de la Universidad de Montpellier y del CHU de Montpellier muestra que los embriones de ratón cultivados en laboratorio solo pueden iniciar la regeneración de los brotes de miembros anteriores, como las patas delanteras, durante un período extremadamente corto: entre 10,5 y 12,5 días después de la fecundación, en el momento en que los brotes de miembros apenas comienzan a formarse. Fuera de esta ventana, esta capacidad desaparece por completo.

Imagen de ilustración Pixabay
Los científicos demuestran que este fenómeno se basa en una población específica de células de la cresta neural, conocidas por desempeñar un papel clave en el desarrollo de muchos tejidos. Sus resultados sugieren que estas células están en el corazón de los mecanismos de regeneración en todos los vertebrados. El equipo también logró inducir la regeneración después de una amputación trasplantando estas células en un embrión que carecía de ellas y había perdido su capacidad de regeneración.
Este estudio realizado en el marco del programa de investigación Bioterapias y bioproducción de terapias innovadoras marca una nueva etapa hacia una medicina regenerativa, capaz de restaurar los tejidos biológicos y sus funciones.
A diferencia de los lagartos y las salamandras, cuya cola puede regenerarse, la regeneración de tejidos es muy limitada en los mamíferos. Sin embargo, existen algunas excepciones bien conocidas: los ciervos renuevan sus cuernos cada año, y los conejos son capaces de reparar tejidos extirpados en sus orejas.
Otra excepción notable concierne a los embriones de ratón. Un estudio anterior [1] mostró que en estos, la regeneración de brotes de miembros anteriores (las patas delanteras) es posible durante el décimo día después de la fecundación. Por otro lado, hasta ahora se ignoraba cuánto tiempo persistía esta facultad y qué mecanismos biológicos y celulares la hacían posible.
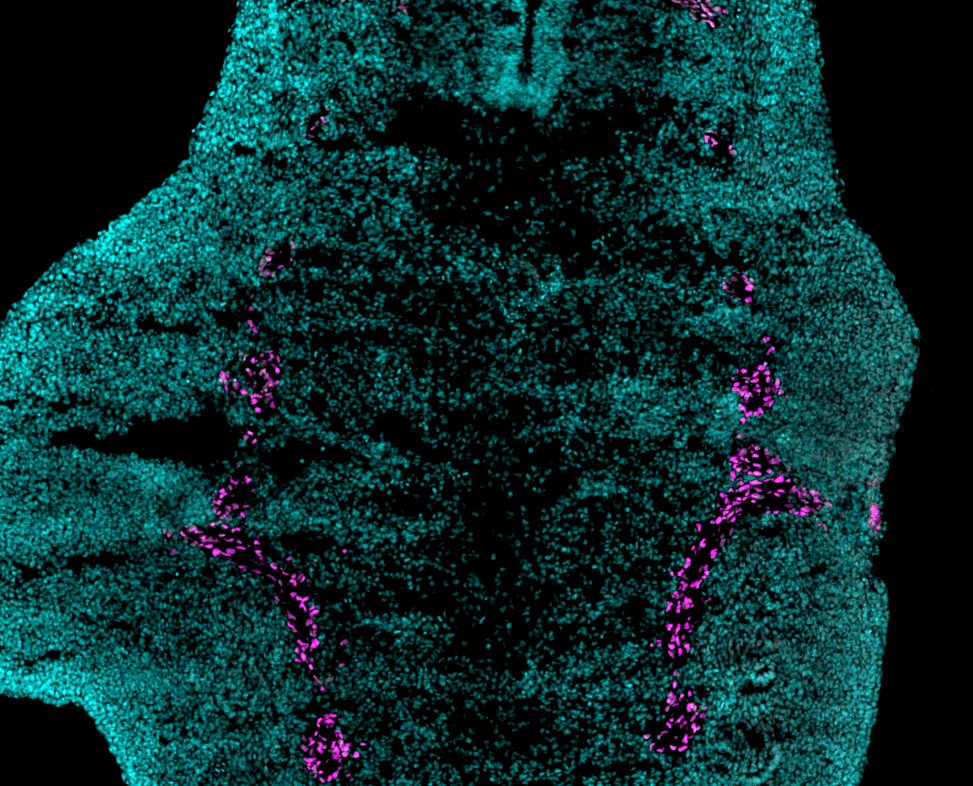
Conocidas por desempeñar un papel clave en el desarrollo de muchos tejidos, las células de la cresta neural (imagen anterior) estarían en el corazón de los mecanismos de regeneración en los mamíferos, según los científicos.
© Jholy De la cruz / Inserm
Un nuevo estudio realizado en el marco del programa de investigación Bioterapias y bioproducción de terapias innovadoras, financiado por el plan de inversión Francia 2030, dirigido por el Inserm y el CEA, aporta hoy respuestas a estas preguntas. Publicados en la revista PNAS, estos trabajos fueron dirigidos por un equipo de investigación del Inserm, de la Universidad de Montpellier y del CHU de Montpellier.
"Nuestro descubrimiento muestra que los embriones de ratón solo pueden iniciar la regeneración de los brotes de miembros anteriores durante un lapso de tiempo extremadamente estrecho del desarrollo: entre 10,5 y 12,5 días después de la fecundación, en el momento en que los brotes apenas comienzan a formarse, explica Farida Djouad, última autora de este estudio. Fuera de este período, esta capacidad desaparece por completo."
Concretamente, los científicos amputaron el brote de miembro anterior de embriones de ratón cultivados en laboratorio 10,5 días después de la fecundación, y observaron que el brote comenzaba a regenerarse durante las 24 horas siguientes. Por otro lado, cuando se realizó el mismo experimento 12,5 días después de la fecundación, no se constató ninguna regeneración.
El estudio revela que esta facultad se basa en una población específica de células llamadas células derivadas de la cresta neural, conocidas por desempeñar un papel clave en el desarrollo del sistema nervioso, del esqueleto facial y de muchos tejidos.
Durante las tres horas siguientes a la amputación, estas células migran hacia la zona lesionada y participan en la formación de un blastema, un cúmulo de células inmaduras en el origen del recrecimiento. "Cuando estas células están ausentes, la regeneración falla. Pero si se trasplantan nuevamente, esta facultad parece poder restaurarse", subraya Farida Djouad.
Gracias a chips de ADN que permiten analizar la actividad de miles de genes simultáneamente, los científicos mostraron que los genes bmp4 y fgf8, marcadores específicos activados durante la formación de los miembros desde la etapa embrionaria, se perdían después de la amputación pero se reactivaban durante la regeneración, subrayando su papel esencial en la restauración de las estructuras amputadas.
Otros genes, WNT1 y FOXD3, característicos de las células de la cresta neural y normalmente activos en una etapa aún más temprana en el embrión (entre el 8º y el 10º día después de la fecundación, en el momento en que los brotes de miembros comienzan a formarse), también se reactivaban. "Esta reactivación temporal parece permitir a las células recuperar un estado más joven y flexible, capaz de movilizarse y participar en la reconstrucción de los tejidos", continúa la última autora.
Estudios anteriores ya habían puesto de relieve el papel de las células derivadas de la cresta neural durante la regeneración de colas o miembros en los tritones [2], así como en la regeneración de la extremidad de los dedos en embriones de ratón [3].
"Nuestros resultados sugieren que las células derivadas de la cresta neural están en el corazón de los mecanismos de regeneración en todos los vertebrados, desde anfibios hasta mamíferos", explica Jholy De La Cruz, co-primer autor del estudio.
Estos resultados ofrecen un comienzo de explicación a la pérdida de la facultad de regeneración en los ratones adultos: las células derivadas de la cresta neural están presentes, pero ya no pueden reactivar los genes necesarios para la regeneración de los tejidos expresados en el estado embrionario.
El equipo de investigación desea ahora saber si estos mecanismos existen también en el humano.
"A largo plazo, esperamos que nuestros trabajos contribuyan a comprender mejor la regeneración de los tejidos, incluso en los humanos, y cómo podría ser posible un día reactivar estos mecanismos con fines terapéuticos", concluye Farida Djouad.
Notas:
[1] Chan WY, Lee KK, Tam PP. Capacidad regenerativa de los brotes de las extremidades anteriores después de la amputación en embriones de ratón en la etapa de organogénesis temprana. J Exp Zool. 1991 Oct;260(1):74-83. doi: 10.1002/jez.1402600110. PMID: 1791423.
[2] Kumar A, Godwin JW, Gates PB, Garza-Garcia AA, Brockes JP. Base molecular de la dependencia nerviosa de la regeneración de extremidades en un vertebrado adulto. Science. 2007 Nov 2;318(5851):772-7. doi: 10.1126/science.1147710. PMID: 17975060; PMCID: PMC2696928.
[3] Johnston AP, Yuzwa SA, Carr MJ, Mahmud N, Storer MA, Krause MP, Jones K, Paul S, Kaplan DR, Miller FD. Se requieren precursores de células de Schwann desdiferenciados que secretan factores paracrinos para la regeneración de la punta del dígito en mamíferos. Cell Stem Cell. 2016 Oct 6;19(4):433-448. doi: 10.1016/j.stem.2016.06.002. Epub 2016 Jul 1. PMID: 27376984.