Estas pequeñas estructuras actúan como tapas protectoras: evitan que nuestro ADN se dañe cuando las células se dividen. Pero con cada división, los telómeros se acortan un poco. Cuando se vuelven demasiado cortos, la célula pierde su capacidad para funcionar correctamente, lo cual está relacionado con el envejecimiento y varias enfermedades, incluidos algunos cánceres.
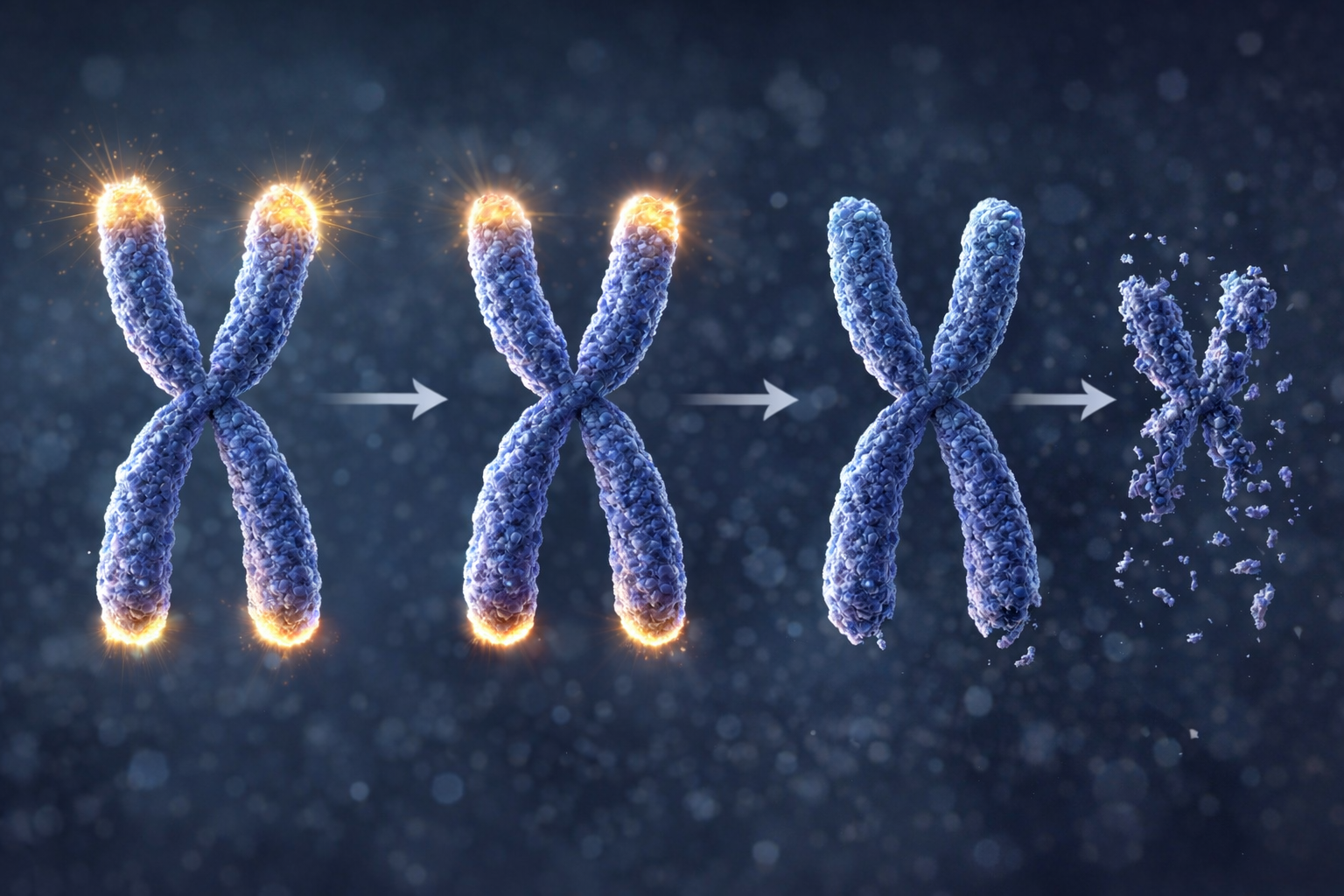
Para ralentizar este proceso, las células disponen de una herramienta crucial: la telomerasa. Esta enzima tiene la función de reparar y alargar los telómeros, contribuyendo así a mantener la salud celular. Comprender mejor su funcionamiento es, por lo tanto, un desafío mayor para la investigación sobre el envejecimiento.
En un estudio publicado en la revista Science, Cryo-electron microscopy structure of the budding yeast telomerase holoenzyme, un equipo internacional de investigadores compuesto por Raymund Wellinger, profesor investigador de la FMSS de la Universidad de Sherbrooke, Pascal Chartrand, profesor de la Universidad de Montreal y Thi Hoang Duong Nguyen, del Laboratory of Molecular Biology, logró una hazaña: identificar por primera vez la estructura atómica de la telomerasa de la levadura. Aunque este organismo pueda parecer lejano al ser humano, es sin embargo un modelo de elección en biología, ya que muchos mecanismos fundamentales son similares a los nuestros.
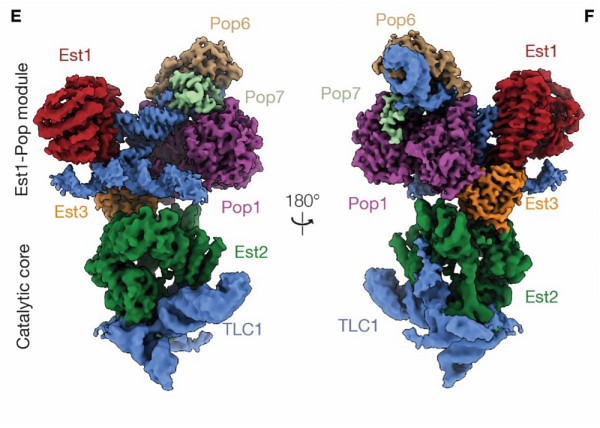
Gracias a una tecnología de imagen de vanguardia, el equipo de investigadores descubrió que la telomerasa de la levadura tiene una estructura arquitectónica muy compleja. En su centro se encuentra un largo fragmento de ARN que actúa como un andamio, manteniendo unidas numerosas proteínas. Algunas forman parte del núcleo central muy estable, esencial para la actividad de la enzima, mientras que otras están unidas de manera más flexible, lo que le da al conjunto una gran flexibilidad.
Más allá de los descubrimientos en torno al papel del ARN, los resultados del estudio destacan que la proteína Est3, un pequeño factor específico de la telomerasa y poco conocido hasta ahora, juega un papel central como plataforma de interacciones proteína-proteína, estabilizando toda la telomerasa. La perturbación de las interacciones de Est3 con otros factores como Est2 y Pop1 provoca un acortamiento de los telómeros y un envejecimiento acelerado de las células, demostrando la importancia funcional de estos contactos. La estructura también confirma que Est3 es un homólogo estructural de una proteína telomérica humana que forma parte de los telómeros.
EST3
Finalmente, un subcomplejo de tres proteínas llamadas Pop1/6/7, que se comparte con enzimas de maduración del ARN, facilita la asociación de tres proteínas esenciales para las funciones de la telomerasa a través de interacciones combinadas ARN-proteína. De manera notable, el equipo de investigadores identificó un bucle específico de Pop1 necesario para el mantenimiento de los telómeros, pero prescindible para la maduración del ARN, demostrando que Pop1 es una verdadera subunidad de la telomerasa dotada de una función específica para los telómeros.
Más allá de la levadura, estos resultados permiten comprender mejor cómo se ensambla y funciona la telomerasa, incluso cuando se basa en un ARN largo, flexible y complejo. Estos principios descubiertos podrían aplicarse a la telomerasa de otras especies, pero también a otras estructuras celulares que contienen largas moléculas de ARN. El estudio muestra finalmente cómo, a lo largo de la evolución, han surgido diferentes formas de organización según las especies, manteniendo al mismo tiempo una función esencial: proteger el ADN y asegurar el buen funcionamiento de las células, un desafío central del envejecimiento y las enfermedades asociadas.