Phosphine - Définition
Source: Wikipédia sous licence CC-BY-SA 3.0.
La liste des auteurs de cet article est disponible ici.
La liste des auteurs de cet article est disponible ici.
Introduction
| Phosphine | ||||
|---|---|---|---|---|
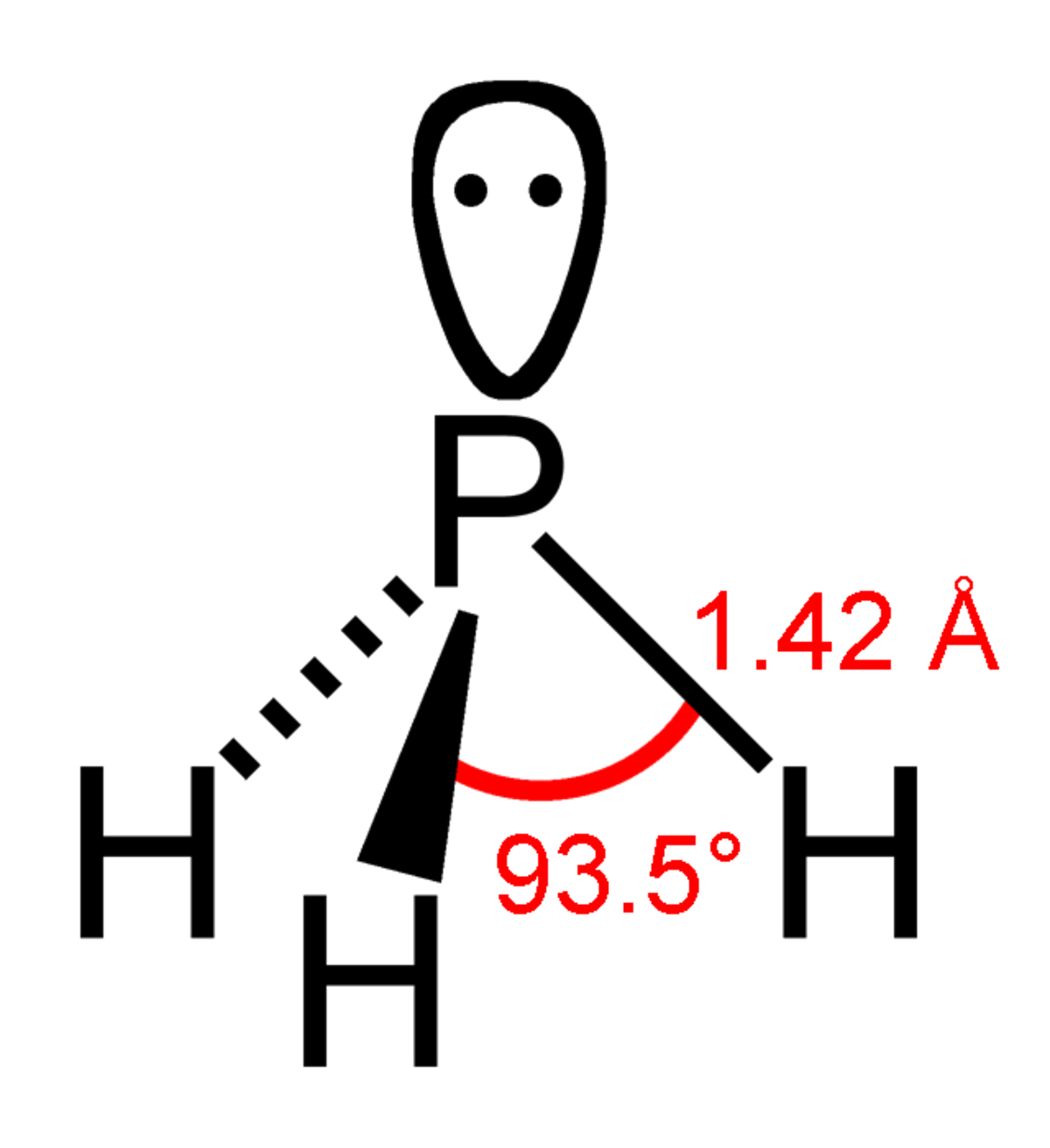 | ||||
| Général | ||||
| Nom IUPAC | ||||
| No CAS | ||||
| No EINECS | ||||
| Apparence | gaz comprimé liquéfié incolore. | |||
| Propriétés chimiques | ||||
| Formule brute | PH3 | |||
| Masse molaire | 33,99758 ± 0,00021 g·mol-1 | |||
| Moment dipolaire | 0,5740 ± 0,0003 D | |||
| Propriétés physiques | ||||
| T° fusion | -133 °C | |||
| T° ébullition | -87,7 °C | |||
| Solubilité | dans l'eau à 17 °C : 26 ml/100 ml | |||
| Masse volumique | 0,8 g·cm-3 | |||
| T° d’auto-inflammation | 38 °C | |||
| Point d’éclair | Gaz Inflammable | |||
| Limites d’explosivité dans l’air | en volume % dans l'air : 1.8-? | |||
| Pression de vapeur saturante | à 20 °C : 4 186 kPa | |||
| Point critique | 65,4 bar, 51,35 °C | |||
| Thermochimie | ||||
| ΔH° | 14,6 kJ·mol-1 (1 atm, -87,75 °C) | |||
| Propriétés électroniques | ||||
| 1re énergie d'ionisation | 9,869 ± 0,002 eV (gaz) | |||
| Cristallographie | ||||
| symbole de Pearson | cP16 | |||
| Classe cristalline ou groupe d’espace | P213 (n°198) | |||
| Strukturbericht | D1 | |||
| Structure type | NH3 | |||
| Précautions | ||||
| | ||||
| ||||
| Phrases R : 12, 17, 26, 34, 50, | ||||
| Phrases S : 1/2, 28, 36/37, 45, 61, | ||||
| | ||||
| ||||
| | ||||
|
4 4 2 | ||||
| | ||||
   | ||||
| | ||||
     Danger | ||||
| Écotoxicologie | ||||
| Seuil de l’odorat | bas : 0,01 ppm haut : 5 ppm | |||
| | ||||
La phosphine est le nom commun de l'hydrure de phosphore (nom IUPAC : phosphane).
Il s'agit d'un gaz incolore et inflammable. Son point d'ébullition est de -88 °C à 1 atm. La phosphine pure est inodore, mais la « phosphine technique » a une odeur extrêmement déplaisante évoquant l'ail ou le poisson pourri, à cause de la présence de phosphine substituée et de diphosphine (P2H4).
Sa formule est PH3. Elle peut être le résultat d'un sel de phosphure d'aluminium ou de magnésium, par exemple, qui aurait réagi avec un acide ou tout simplement avec l'eau où il est hydrolysé.
Exemple : AlP+ 3H2O --> PH3 + Al(OH)3
phosphure d'aluminium + eau --> phosphine (gaz) + hydroxyde d'aluminium.
Utilisation
- Rodenticide utilisé pour tuer des taupes ou autres vermines.
- Dopant dans l'industrie des semi-conducteurs.
- Destruction des insectes et des acariens dans les denrées et semences stockées (fûts, silos, bateaux etc)
Populaires