Duas equipes do Inserm, do CNRS e da Universidade Paris Cité acabam de descobrir o maestro desse mecanismo de progressão inexorável: a proteína HNF1B. Além de um avanço importante no conhecimento dessas doenças, as equipes identificaram um novo alvo terapêutico de grande interesse. Este trabalho será publicado na revista Science.
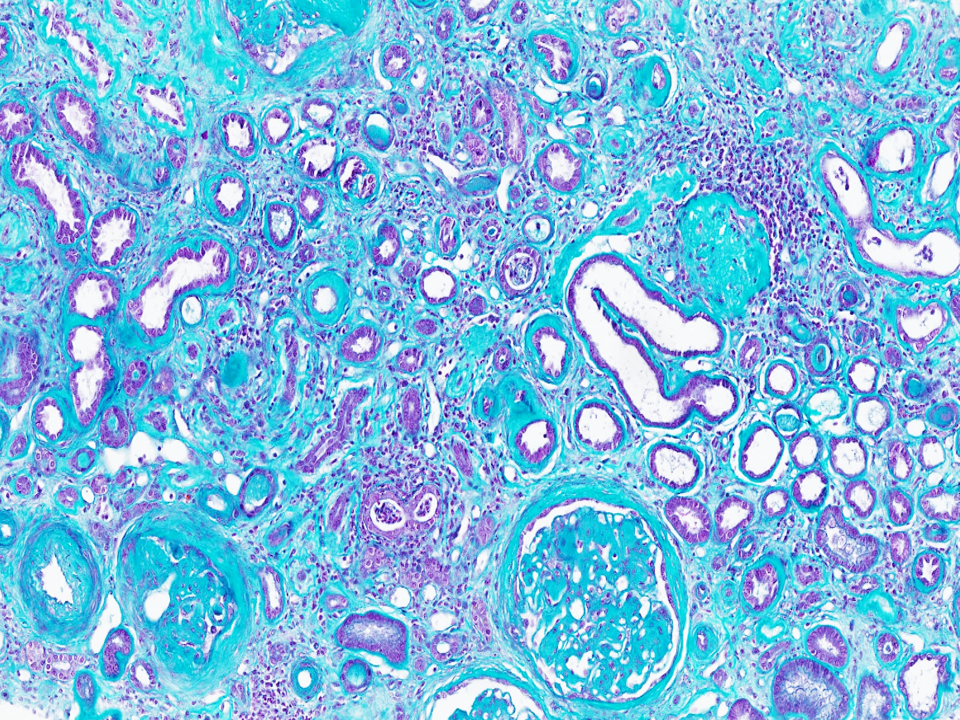
Imagem de microscopia óptica de um rim de paciente com insuficiência renal terminal. A fibrose intersticial importante (colágeno e tecido conjuntivo fibrosado em ciano) e a atrofia dos túbulos renais (pequenos canais rodeados por uma parede espessada em violeta) evidenciam uma substituição progressiva e irreversível do tecido renal funcional por tecido cicatricial.
Coloração: tricrômico de Masson.
© Fabiola Terzi, Marco Pontoglio/Inserm
A doença renal crônica afeta mais de 10% da população mundial, cerca de 850 milhões de pessoas. Caracteriza-se por uma perda progressiva e irreversível da função renal, podendo necessitar de diálise ou até mesmo transplante.
Vários fatores de risco são bem identificados: diabetes, hipertensão, obesidade ou inflamação. No entanto, mesmo que a causa inicial seja tratada, o declínio da função renal é, na grande maioria dos casos, inevitável. Esse caráter autossustentável representa um aspecto particularmente preocupante da doença renal; ao adquirir sua própria dinâmica, torna-se difícil de interromper. Até agora, os mecanismos biológicos responsáveis por essa progressão continuavam amplamente desconhecidos.
Duas equipes do Instituto Necker-Enfants malades (Inserm/CNRS/Universidade Paris Cité) dirigidas por Marco Pontoglio, diretor de pesquisa do CNRS, e Fabiola Terzi, diretora de pesquisa do Inserm e diretora do Instituto Necker-Enfants malades, se interessaram por esses mecanismos biológicos, e mais particularmente pelo papel no rim adulto da proteína HNF1B (Hepatocyte Nuclear Factor 1 beta). Ela controla a expressão de muitos genes e desempenha um papel indispensável na formação do rim durante o desenvolvimento embrionário.
De fato, em humanos, mutações no gene HNF1B causam uma diminuição da atividade dessa proteína, o que leva a uma doença genética rara do rim. E fato marcante: as lesões observadas em pacientes podem se assemelhar às encontradas nas formas mais comuns da doença renal crônica, ou seja, fibrose ou atrofia do tecido renal.
Essa similaridade levou os pesquisadores a formularem uma hipótese: a disfunção do HNF1B poderia representar um mecanismo comum conectando as doenças renais raras e as formas muito mais frequentes, como a doença renal crônica.
As equipes de pesquisa observaram que a perda da atividade do HNF1B no rim adulto humano e de camundongos provocava uma insuficiência renal crônica rápida e severa, acompanhada de fibrose e atrofia do tecido renal. Privadas da atividade do HNF1B, as células tubulares renais - que revestem os túbulos renais e desempenham um papel importante na função do rim -, normalmente altamente diferenciadas e estáveis, perdiam sua identidade e especialização e começavam a proliferar de forma inadequada.
Essa proliferação era acompanhada de morte celular ou envelhecimento prematuro das células, contribuindo para a fibrose progressiva do rim e a degradação de sua função.
Os pesquisadores também identificaram um conjunto de genes cuja expressão é regulada pelo HNF1B. Esse conjunto aparecia alterado muito precocemente em vários modelos de doença renal crônica em camundongos, às vezes antes mesmo do aparecimento de lesões visíveis, e estava associado a um defeito na reparação do tecido renal.
Os cientistas também mostraram que fatores associados à doença renal, como inflamação ou presença de albumina na urina, reduziam a atividade do HNF1B. Graças a técnicas avançadas de análise da atividade dos genes, eles evidenciaram um fenômeno chave: o estresse sofrido pelas células do rim durante uma doença renal crônica leva a uma repressão dos genes regulados pelo HNF1B.
"Nossos resultados revelam a existência de um verdadeiro círculo vicioso que explica o caráter autossustentável das doenças renais: a diminuição da atividade do HNF1B favoreceria a doença renal, e em contrapartida, a doença renal suprimiria progressivamente a atividade do HNF1B, agravando ainda mais as lesões renais. Esse mecanismo poderia explicar por que a doença renal crônica tende a piorar de forma contínua, mesmo na ausência de uma nova agressão", resume Marco Pontoglio.
Esse mecanismo seria comum a muitas doenças renais. De fato, a análise de mais de 900 biópsias renais de pacientes com doença renal crônica de diferentes origens e abrangendo todos os estágios de gravidade, evidenciou sistematicamente a assinatura molecular característica da perda de função do HNF1B.
As anomalias eram tanto mais marcadas quanto a doença estava avançada, confirmando o papel importante dessa proteína na gravidade da lesão renal. "Este estudo estabelece o HNF1B como um verdadeiro guardião da função renal. Sua perda de atividade conecta pela primeira vez as doenças genéticas renais raras e as formas comuns de doença renal crônica por um mecanismo único", esclarece Fabiola Terzi.
Esses resultados abrem uma nova perspectiva terapêutica importante: "encontrar uma maneira de restaurar a atividade do HNF1B poderia permitir retardar, ou até mesmo modificar a evolução da doença renal crônica" conclui Fabiola Terzi.
Este trabalho é objeto de uma patente depositada junto à Inserm Transfert em 2025.