Restez toujours informé: suivez-nous sur Google Actualités (icone ☆)
Les simulations effectuées apportent des informations sur les propriétés physiques du carbone dans des conditions extrêmes, essentielles dans la conception de modèles de planètes comme Neptune ou Uranus, d'étoiles naines blanches, voire de planètes extrasolaires riches en carbone.
Simulation graphique de la fonction d'onde électronique dans le
carbone liquide à 9.000 K et sous cinq millions d'atmosphères.
A cette pression le diamant fond à environ 8.000 K.
Sous sa forme élémentaire, le carbone se trouve dans le charbon, le graphite, le diamant, ou encore les nanotubes. Ce sont des matériaux dont les propriétés sont très différentes, bien qu'au niveau microscopique ils ne diffèrent que par l'agencement géométrique de leurs atomes.
Le carbone élémentaire est connu depuis la préhistoire, et une de ses formes les plus connues, le diamant, est supposé avoir été extrait pour la première fois en Inde il y a plus de 2.000 ans. Les propriétés du diamant et ses applications pratiques et technologiques sont considérables et se sont vérifiées au cours du temps. Mais en dépit de tous ces siècles d'investigations et de l'important travail expérimental des dernières décennies sur le diamant fortement compressé, les limites entre phases et les propriétés de fusion du carbone restent mal connues. Ses propriétés électroniques ne sont non plus pas bien comprises dans ces conditions extrêmes. Les données expérimentales sont rares en raison des difficultés d'atteindre le mégabar (un million d'atmosphères) et les milliers de kelvins nécessaires en laboratoire.
Les travaux des chercheurs montrent une description cohérente du carbone élémentaire pour un large intervalle de températures et de pressions et une description de ses propriétés électroniques dans ces conditions. Les scientifiques ont également découvert que le point triple diamant/BC8/liquide (défini par la température et la pression pour lesquelles ces trois phases coexistent en équilibre thermodynamique) est à une plus basse pression que ce que l'on pensait auparavant (Le "BC8" est une phase solide du carbone dans laquelle le diamant se transforme au-dessus de 12 Mbar, pour une température nulle). Les conditions pour lesquelles le point triple est atteint sont proches des évaluations récentes des conditions (de température et de pression) qui doivent exister dans le noyau de Neptune et de Uranus.
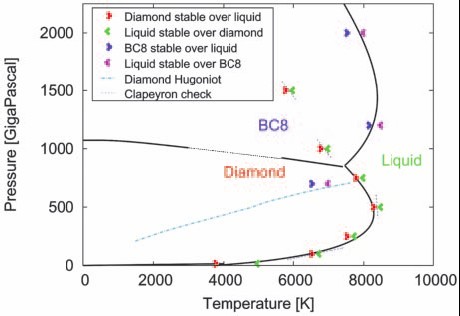
Point triple du carbone à haute pression:
T= 7445 K, Pression = 8,5 Mbar (850 Gpa)
Selon les chercheurs, les modèles planétaires actuels devront être partiellement révisés, en particulier pour ce qui concerne le noyau des planètes. Leurs travaux pourront également servir à interpréter de futurs résultats expérimentaux.