Restez toujours informé: suivez-nous sur Google Actualités (icone ☆)
La maladie d'Alzheimer entraîne une perte progressive de la mémoire. Elle résulte d'une lente dégénérescence des cellules du cerveau. Ces altérations sont associées à l'accumulation de dépôts constitués d'une substance appelée amyloïde-β dans le cerveau.
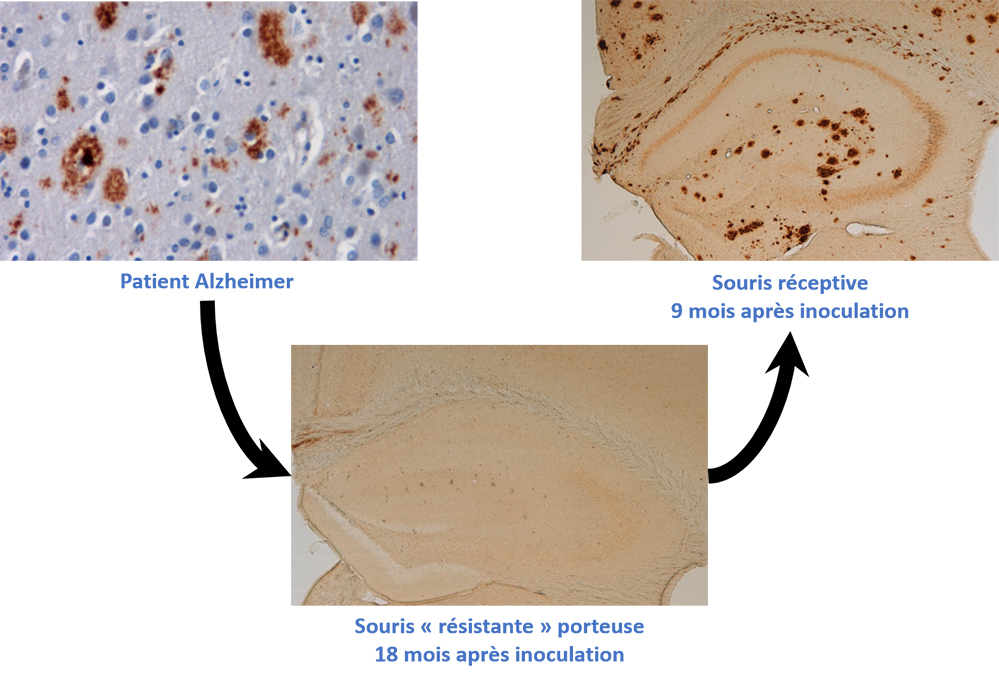
Figure: Inoculation séquentielle d'extraits de cerveau humain Alzheimer démontrant qu'une transmission des lésions de cette maladie est possible à partir de cerveaux apparemment sains.
En haut à gauche: Cerveau humain présentant des lésions amyloïdes-β caractéristiques de la maladie d'Alzheimer.
En bas: Cerveau d'une souris, "résistante à la pathologie", ne montrant pas de traces visibles de lésions amyloïdes-β suite à l'inoculation du cerveau humain Alzheimer. En haut à droite: Induction de lésions amyloïdes-β, semblables à celles observées chez l'Homme, chez une souris suite à l'inoculation du cerveau "résistant" apparemment sain.
© A.S. Herard & M. Dhenain
Chez l'homme, des travaux épidémiologiques suggèrent que des dépôts d'amyloïde-β peuvent être transmis d'un patient à l'autre dans des circonstances exceptionnelles suite à un acte médical (injections d'hormone de croissances issues de cerveaux, procédures neurochirurgicales avec greffes de tissus d'origine cérébrale). Jusqu'à maintenant, l'hypothèse avancée était que ce sont les cerveaux de patients présentant les lésions de la maladie d'Alzheimer qui sont responsables de l'induction de la pathologie.
Dans ce travail, les chercheurs observent que l'inoculation d'échantillons de cerveaux en apparence sains peuvent induire la pathologie amyloïde-β et démontrent ainsi que l'élément transmissible est invisible avec des techniques d'analyses classiques. Pour arriver à cette conclusion, ils ont créé des échantillons de cerveaux qui ne présentent pas de lésions amyloïde-β visibles, mais qui ont cependant déjà été en contact avec l'amyloïde-β. Pour réaliser ces expériences, ils ont inoculé des broyats de cerveaux humains Alzheimer à une lignée de souris résistante aux dépôts de lésions amyloïde-β. Plus de 1,5 ans après cette inoculation, les animaux ne développaient pas de lésions dans une région du cerveau (appelée hippocampe). Un broyat issu de ces hippocampes apparemment sains a ensuite été injecté à une autre souche murine plus apte à développer des lésions amyloïde-β. Or ces souris ont développé des lésions de la maladie. Cela suggère que des "graines" de substance amyloïde-β issues d'échantillons de cerveau humain peuvent persister sous des formes furtives dans les tissus cérébraux tout en conservant leur capacité à favoriser le dépôt de ce peptide chez des hôtes réceptifs.
Ces résultats appellent à la plus grande vigilance et soulignent la nécessité de mesures préventives de haut niveau, notamment en neurochirurgie, pour prévenir le risque de transmission suite à un acte médical impliquant du tissu cérébral potentiellement contaminé bien qu'apparemment sain.
Pour en savoir plus:
Induction of amyloid-β deposits from serially transmitted, histologically silent, Aβ seeds issued from human brains.
Hérard AS, Petit F, Gary C, Guillermier M, Boluda S, Garin CM; Brainbank Neuro-CEB Neuropathology Network, Lam S, Dhenain M.
Acta Neuropathol Commun. 2020 Nov 30;8(1):205. doi: 10.1186/s40478-020-01081-7
Laboratoire:
Laboratoire des Maladies Neurodégénératives - (Université Paris Saclay/CEA/CNRS)
18 route du Panorama, 92265 Fontenay aux Roses.
Contact:
Marc Dhenain - Chercheur au CNRS au laboratoire des Maladies Neurodégénératives - marc.dhenain at cea.fr