En un estudio publicado en Nature, químicos franceses e ingleses demuestran cómo motores moleculares artificiales muy simples son capaces de producir tal trabajo catalizando la conversión de un combustible químico quiral. Esto podría impulsar la robótica blanda y la materia activa.

Imagen de ilustración Pixabay
¿Cómo pueden algunas moléculas realizar un trabajo organizado y ordenado en un entorno caótico? El mundo de las moléculas sumergidas en un líquido está gobernado por un proceso estocástico, llamado movimiento browniano, que describe las trayectorias aleatorias de las partículas.
Forzar una trayectoria en lugar de otra no es más fácil que moverse en un ciclón. Sin embargo, es en este entorno desordenado donde los motores biológicos, proteínas con estructuras complejas, producen un trabajo mecánico perfectamente definido.
Por ejemplo, la miosina-II es responsable de la contracción muscular en la mayoría de los animales. Para ello, esta proteína con actividad enzimática convierte una fuente de energía química (el adenosín trifosfato (ATP)) en un producto de reacción (el adenosín difosfato (ADP)).
Esta transformación va acompañada de una cascada de movimientos perfectamente ordenados que se traducen en la contracción macroscópica del tejido muscular. Sin embargo, el mecanismo detrás de esta conversión de energía química en trabajo aún no ha sido resuelto por la comunidad científica.
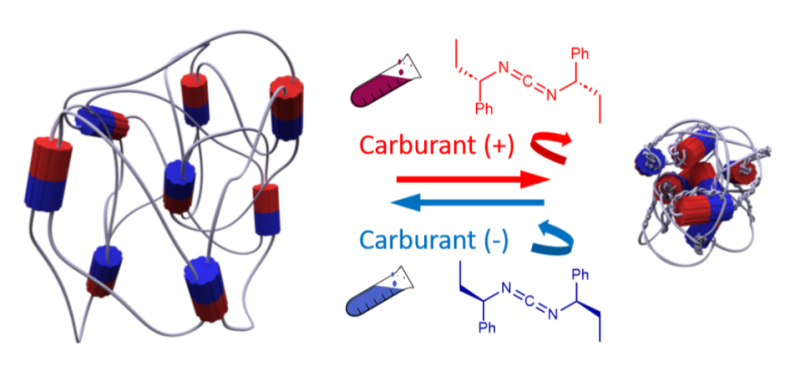
Músculo artificial que utiliza motores moleculares rotativos y se activa mediante un combustible químico quiral. El sentido de rotación de los motores está determinado por el exceso enantiomérico del combustible, lo que permite controlar la contracción o extensión del músculo artificial.
© Nicolas Giuseppone
En el marco del proyecto colaborativo europeo ITN-ArtMoMa, químicos del Instituto Charles Sadron (CNRS/Universidad de Estrasburgo/Instituto Universitario de Francia) y de la Universidad de Manchester han logrado responder a esta pregunta utilizando un sistema químico mínimo. Para ello, combinaron pequeños motores rotativos (1000 veces más pequeños que la miosina-II) con una red polimérica para formar un hidrogel activo.
Los motores moleculares utilizados están compuestos por una parte estática (estator) y una parte móvil (rotor). Al añadir un combustible químico, el motor cataliza la transformación del combustible en un producto de reacción, lo que provoca la rotación del rotor a través de una secuencia ordenada de cambios conformacionales.
El rotor, químicamente unido a las cadenas de polímero, a su vez provoca la contracción o expansión del material, dependiendo de si gira en un sentido o en el otro. Este sentido preferencial de rotación transferido a la red polimérica está determinado por la quiralidad del combustible. Según el exceso enantiomérico de este último, se observa una contracción o extensión macroscópica del hidrogel.
Al medir los cambios en las propiedades del material hidrogel, los investigadores también pudieron determinar la fuerza generada por el motor y su eficiencia energética.
Este sistema tan simple demuestra cómo un catalizador es capaz de convertir una fuente de energía química en movimientos controlados hasta la escala macroscópica, jugando con la asimetría de las constantes de velocidad de las reacciones involucradas en el ciclo catalítico.
Este estudio, publicado en la revista Nature, destaca el potencial de los motores moleculares artificiales para explicar uno de los grandes principios del funcionamiento de los seres vivos. También podría inspirar el diseño de nuevos elementos activos en el campo de la ciencia de materiales y las nanotecnologías.
Referencia:
Transducing chemical energy through catalysis by an artificial molecular motor
Peng-Lai Wang, Stefan Borsley, Martin J. Power, Alessandro Cavasso, Nicolas Giuseppone & David Leigh.
Nature 2024
https://doi.org/10.1038/s41586-024-08288-x