Dos equipos del Inserm, del CNRS y de la Universidad París Citè acaban de descubrir el director de orquesta de este mecanismo de progresión inexorable: la proteína HNF1B. Más allá de un avance importante en el conocimiento de estas enfermedades, los equipos han identificado un nuevo objetivo terapéutico de gran interés. Estos trabajos se publicarán en la revista Science.
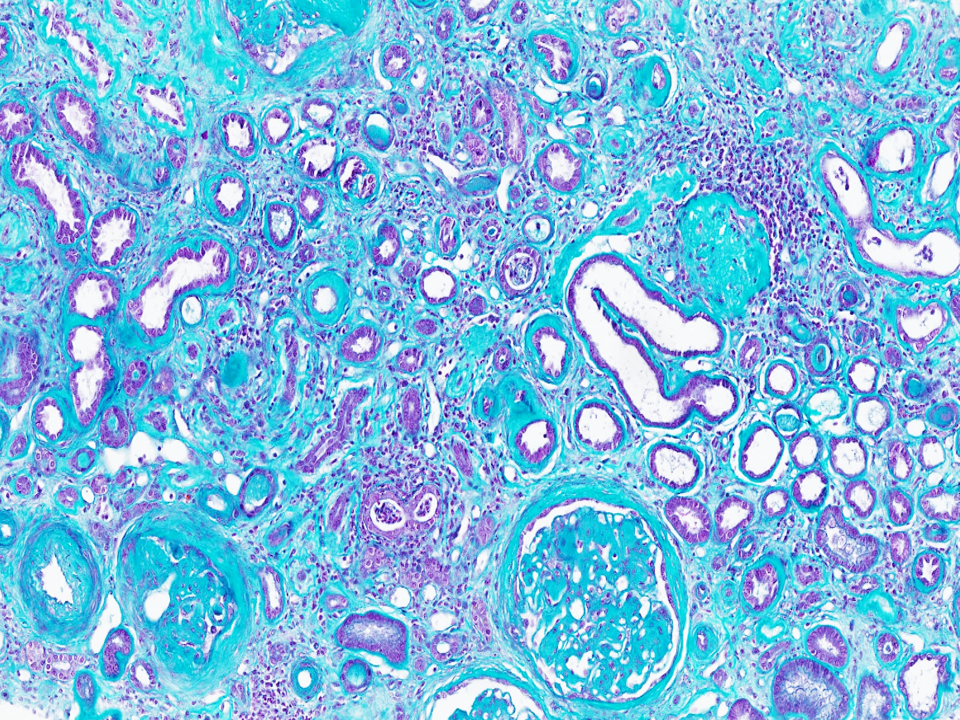
Imagen de microscopía óptica de un riñón de un paciente con insuficiencia renal terminal. La fibrosis intersticial importante (colágeno y tejido conjuntivo fibrosado en cian) y la atrofia de los túbulos renales (pequeños conductos rodeados de una pared engrosada en violeta) evidencian un reemplazo progresivo e irreversible del tejido renal funcional por tejido cicatricial.
Tinción: tricrómico de Masson.
© Fabiola Terzi, Marco Pontoglio/Inserm
La enfermedad renal crónica afecta a más del 10 % de la población mundial, es decir, aproximadamente 850 millones de personas. Se caracteriza por una pérdida progresiva e irreversible de la función renal, que puede requerir diálisis o incluso un trasplante.
Varios factores de riesgo están bien identificados: diabetes, hipertensión, obesidad o inflamación. Sin embargo, incluso si la causa inicial es tratada, el deterioro de la función renal es, en la gran mayoría de los casos, inevitable. Este carácter auto-mantenido representa un aspecto particularmente preocupante de la enfermedad renal; al adquirir su propia dinámica, se vuelve difícil de detener. Hasta ahora, los mecanismos biológicos responsables de esta progresión seguían siendo en gran medida desconocidos.
Dos equipos del Instituto Necker-Enfermedades de los Niños (Inserm/CNRS/Universidad París Citè) dirigidos por Marco Pontoglio, director de investigación del CNRS, y Fabiola Terzi, directora de investigación del Inserm y directora del Instituto Necker-Enfermedades de los Niños, se interesaron en estos mecanismos biológicos, y más particularmente en el papel en el riñón adulto de la proteína HNF1B (Hepatocyte Nuclear Factor 1 beta). Esta controla la expresión de numerosos genes y juega un papel indispensable en la formación del riñón durante el desarrollo embrionario.
De hecho, en humanos, las mutaciones del gen HNF1B provocan una disminución de la actividad de esta proteína, lo que conduce a una enfermedad genética renal rara. Y hecho llamativo: las lesiones observadas en los pacientes pueden parecerse a las encontradas en las formas más comunes de la enfermedad renal crónica, es decir, fibrosis o atrofia del tejido renal.
Esta similitud llevó a los investigadores a formular una hipótesis: el disfuncionamiento de HNF1B podría representar un mecanismo común que vincula las enfermedades renales raras con las formas mucho más frecuentes, como la enfermedad renal crónica.
Los equipos de investigación observaron así que la pérdida de la actividad de HNF1B en el riñón adulto humano y de ratón provocaba una insuficiencia renal crónica rápida y severa, acompañada de fibrosis y atrofia del tejido renal. Privadas de la actividad de HNF1B, las células tubulares renales —que recubren los túbulos renales y juegan un papel importante en la función del riñón—, normalmente altamente diferenciadas y estables, perdían su identidad y especialización y comenzaban a proliferar de manera inapropiada.
Esta proliferación se acompañaba entonces de muerte celular o de envejecimiento prematuro de las células, contribuyendo a la fibrosis progresiva del riñón y al deterioro de su función.
Los investigadores también identificaron un conjunto de genes cuya expresión regula HNF1B. Este conjunto aparecía alterado muy tempranamente en varios modelos de enfermedad renal crónica en ratón, a veces incluso antes de la aparición de lesiones visibles, y estaba asociado a un defecto de reparación del tejido renal.
Los científicos también demostraron que los factores asociados a la enfermedad renal, como la inflamación o la presencia de albúmina en la orina, reducían la actividad de HNF1B. Gracias a técnicas avanzadas de análisis de la actividad de los genes, pusieron en evidencia un fenómeno clave: el estrés sufrido por las células del riñón durante una enfermedad renal crónica provoca una represión de los genes regulados por HNF1B.
"Nuestros resultados revelan la existencia de un verdadero círculo vicioso que explica el carácter auto-mantenido de las enfermedades renales: la disminución de la actividad de HNF1B favorecería la enfermedad renal, y a su vez, la enfermedad renal suprimiría progresivamente la actividad de HNF1B, agravando aún más las lesiones renales. Este mecanismo podría explicar por qué la enfermedad renal crónica tiende a agravarse de forma continua, incluso en ausencia de una nueva agresión", resume Marco Pontoglio.
Este mecanismo sería común a muchas enfermedades renales. De hecho, el análisis de más de 900 biopsias renales de pacientes con enfermedad renal crónica de diferentes orígenes y que cubren todos los estadios de gravedad, puso sistemáticamente en evidencia la firma molecular característica de la pérdida de función de HNF1B.
Las anomalías eran tanto más marcadas cuanto más avanzada estaba la enfermedad, confirmando el papel importante de esta proteína en la severidad de la afectación renal. "Este estudio establece a HNF1B como un verdadero guardián de la función del riñón. Su pérdida de actividad conecta por primera vez las enfermedades genéticas renales raras y las formas comunes de la enfermedad renal crónica mediante un mecanismo único", aclara Fabiola Terzi.
Estos resultados abren una nueva perspectiva terapéutica importante: "encontrar una manera de restaurar la actividad de HNF1B podría permitir ralentizar, o incluso modificar la evolución de la enfermedad renal crónica" concluye Fabiola Terzi.
Estos trabajos son objeto de una patente depositada en Inserm Transfert en 2025.