O conceito científico subjacente, denominado ventilação entérica, poderia constituir uma alternativa às técnicas convencionais de suporte respiratório. Seu princípio ativo utiliza um líquido com propriedades físico-químicas particulares, capaz de fixar quantidades significativas de oxigênio. O objetivo terapêutico é permitir que este gás vital atravesse a mucosa retal para alcançar a circulação sanguínea, contornando assim as vias aéreas superiores quando estas se tornam deficientes.

Uma inspiração vinda do mundo animal
Várias espécies aquáticas desenvolveram capacidades respiratórias intestinais para sobreviver em ambientes pobres em oxigênio. As cobitídeos, peixes de água doce, podem assim engolir ar na superfície e extrair oxigênio através do seu tubo digestivo. Algumas tartarugas de água doce também utilizam sua cloaca para realizar trocas gasosas debaixo d'água. Estas observações forneceram aos pesquisadores pistas sérias para explorar vias respiratórias alternativas em mamíferos.
A mucosa intestinal humana apresenta características anatômicas favoráveis a este tipo de troca. Fina e ricamente vascularizada, ela permite normalmente a absorção de nutrientes e de certos medicamentos. Os cientistas levantaram a hipótese de que esta membrana poderia também permitir a difusão de moléculas de oxigênio para os capilares sanguíneos. Trabalhos anteriores em modelos suínos haviam validado este princípio, demonstrando a possibilidade de oxigenar o sangue por esta via não convencional.
O líquido utilizado nestas pesquisas, a perfluorodecalina, possui uma afinidade excepcional pelos gases respiratórios. Este composto pode dissolver até cinquenta vezes mais oxigênio que a água, criando assim um gradiente de concentração favorável à sua difusão passiva através dos tecidos. Já aprovado para certos usos médicos, este produto oferece a vantagem de ser biologicamente inerte e não absorvido pelo organismo.
Primeiros resultados em humanos
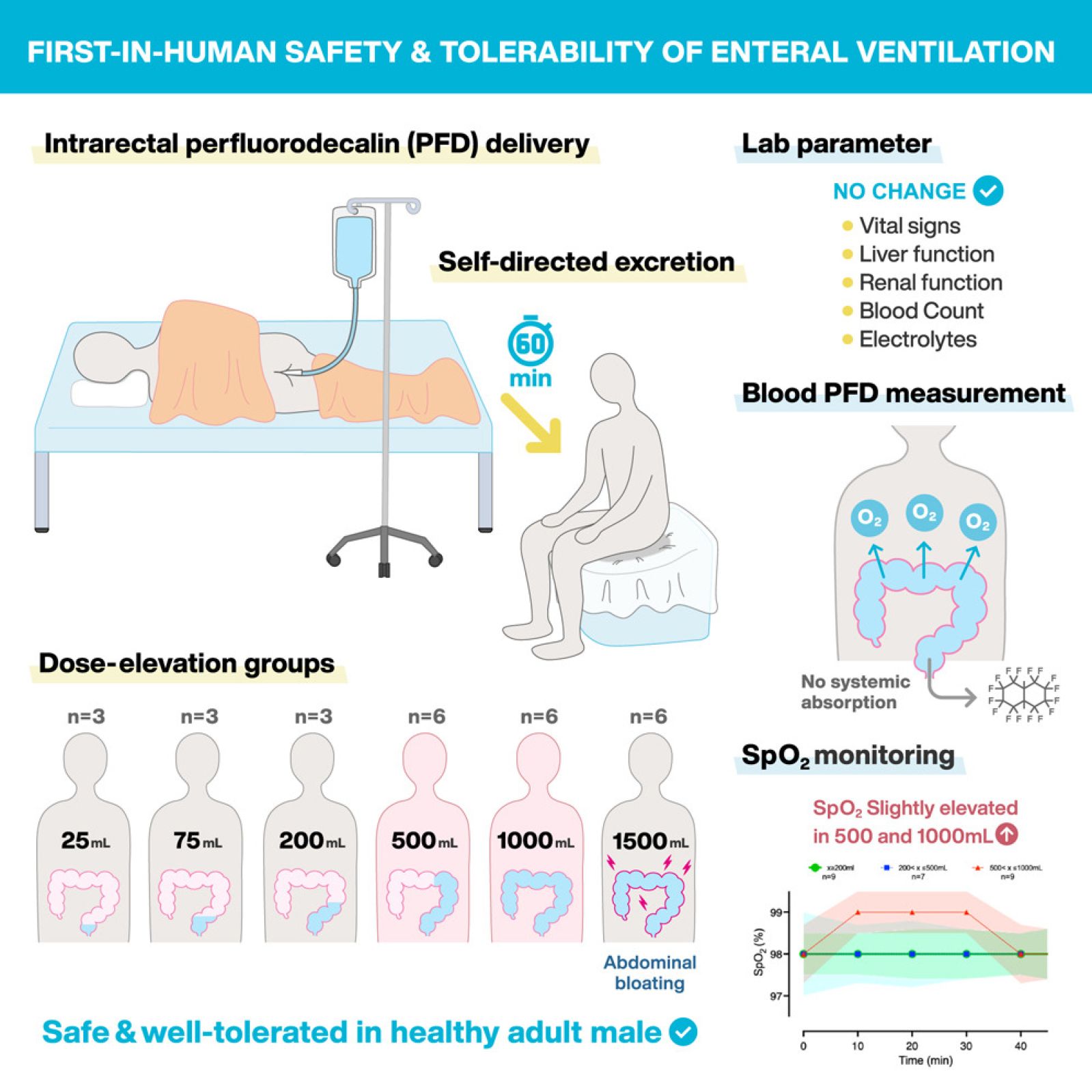
O ensaio clínico preliminar incluiu 27 voluntários masculinos saudáveis. Os participantes receberam diferentes quantidades de perfluorodecalina não oxigenada (entre 0,25 e 1,5 litros), que deveria ser conservada durante 60 minutos no seu reto. Esta fase inicial visava exclusivamente avaliar a tolerância local e sistêmica do procedimento, sem medir a eficácia das trocas gasosas. O protocolo experimental aumentou cuidadosamente os volumes administrados para identificar possíveis efeitos adversos.
Entre os participantes, 20 suportaram a totalidade do tempo previsto, incluindo aqueles que receberam os volumes mais importantes. As observações clínicas não revelaram nenhuma modificação dos parâmetros vitais durante a experimentação. Os pesquisadores notaram, no entanto, o aparecimento de sensações de inchaço abdominal e desconforto nos sujeitos que receberam os maiores volumes, sem contudo constatar reações adversas severas.
Os investigadores destacam o caráter preliminar destes dados nas colunas da revista Med. Eles indicam que esta primeira etapa valida apenas o aspecto de segurança do método em sujeitos saudáveis. A demonstração da sua eficácia para melhorar a oxigenação sanguínea necessitará de investigações complementares utilizando a versão oxigenada do líquido. Estes resultados abrem, no entanto, um caminho promissor para o desenvolvimento desta abordagem terapêutica.