Restez toujours informé: suivez-nous sur Google Actualités (icone ☆)
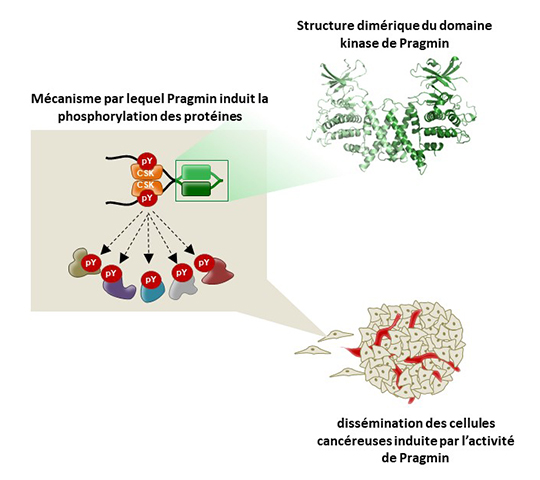
Figure: La Pragmin est impliqué dans la dissémination des cellules tumorales de certains cancers d'origine digestives. Son activité est reliée à sa capacité à phosphoryler les protéines sur tyrosine. La cartographie établie à partir de l'analyse structurale révèle qu'elle est inactive mais qu'elle utilise un mécanisme de dimérisation pour activer la kinase cible CSK.
© Gilles Labesse, Céline Lecointre et Serge Roche
La phosphorylation des protéines joue un rôle central dans les mécanismes moléculaires qui contrôlent la croissance et l'adhésion des cellules. La dérégulation des protéines kinases, les enzymes responsables de cette phosphorylation, conduit souvent à des états pathologiques tels que le cancer. Ces enzymes sont donc des cibles privilégiées en oncologie médicale comme en témoigne l'approbation de près de 30 inhibiteurs de kinases en clinique.
De manière surprenante, parmi les 530 "kinases" que code le génome humain, il en existe environ 50 qui sont prédites non catalytiques, en raison de l'absence des acides aminés essentiels pour assurer la phosphorylation. Ces protéines sont appelées pseudo-kinases. Malgré cette absence avérée d'activité enzymatique, elles présentent pourtant des rôles aussi importants que les kinases actives dans la physiopathologie humaine, mais les mécanismes en jeu n'étant que très peu connus, elles n'étaient pas considérées comme des cibles thérapeutiques intéressantes.
Ce travail met en lumière un mécanisme original qui explique l'activité biologique de l'une de ces pseudo-kinases, la Pragmin, encore appelé SGK223, à cause de son rôle central dans l'agressivité de cancers digestifs. Les chercheurs ont d'abord analysé la structure de cette pseudo-kinase et vérifié que, malgré une conformation globale semblable aux protéines kinases actives, elle ne peut lier l'ATP ni catalyser le transfert du phosphate vers la protéine substrat en raison de la présence d'acides aminés qui rendent le site catalytique inactif.
Ils démontrent que c'est par une association avec la protéine kinase active CSK que la Pragmin induit la phosphorylation des protéines sur résidus tyrosine pour induire son activité biologique. De manière importante, l'analyse structurale révèle également des séquences responsables de la dimérisation de la protéine qui conduit à l'activation efficace de CSK.
Ces résultats permettent de comprendre comment une pseudo-kinase, a priori inactive, peut cependant induire la phosphorylation des protéines. Ainsi, la cartographie de sa structure pourrait ouvrir de nouvelles pistes pour bloquer son activité oncogénique dans certains cancers agressifs.