Restez toujours informé: suivez-nous sur Google Actualités (icone ☆)
Des réactions qui semblent défier les lois de la thermodynamique
La vie possède une propriété remarquable: elle parvient à maintenir et exploiter des états chimiques loin de l'équilibre. Dès 1945, le physicien Erwin Schrödinger s'interrogeait sur cette particularité dans son ouvrage What is Life?, soulignant que les organismes vivants tirent parti de gradients d'énergie pour organiser la matière.

Ces photos illustrent des cheminées hydrothermales, également appelées "Fumeurs noirs".
Image Wikimedia
Un exemple central est la chimiosmose, un mécanisme utilisé par les cellules pour produire de l'énergie. Dans les mitochondries ou les bactéries, un gradient de protons à travers une membrane permet de générer des réactions chimiques essentielles au métabolisme.
Mais une question demeure: des processus similaires pourraient-ils exister dans des environnements purement minéraux, avant même l'apparition des premières cellules ?
Des "membranes" minérales capables de produire du fer métallique
Pour explorer cette hypothèse, des scientifiques ont reproduit en laboratoire des analogues de cheminées hydrothermales alcalines riches en fer, semblables à celles qui existaient sur la Terre primitive.
Les résultats, publiés dans la revue Nature Communications, révèlent un phénomène inattendu: l'énergie d'un gradient de pH peut être convertie en production de fer métallique, une réaction qui, en principe, ne devrait pas se produire sans la présence d'un agent réducteur chimique.
Ce processus repose sur des transferts couplés d'ions et d'électrons au sein de "membranes" minérales. Ces structures agissent alors comme de véritables interfaces énergétiques, comparables par certains aspects aux membranes biologiques.
Localement, ces transferts permettent de maintenir des états redox hors équilibre, associés à une diminution locale de l'entropie, une condition considérée comme essentielle à l'émergence de réactions métaboliques primitives.
Un mécanisme inattendu
Les résultats remettent en question certaines hypothèses précédentes. Jusqu'ici, on pensait que ce type de réaction dépendait surtout de composés chimiques réactifs générés par des différences de pH.
Or l'étude montre que les propriétés intrinsèques des minéraux suffisent: la structure même de la membrane minérale permet la conversion directe de l'énergie du gradient de pH en gradient redox, essentiel aux réactions chimiques retrouvées dans le vivant.
Cette découverte suggère que des systèmes purement géologiques pourraient avoir joué un rôle actif dans les premières conversions d'énergie prébiotiques.
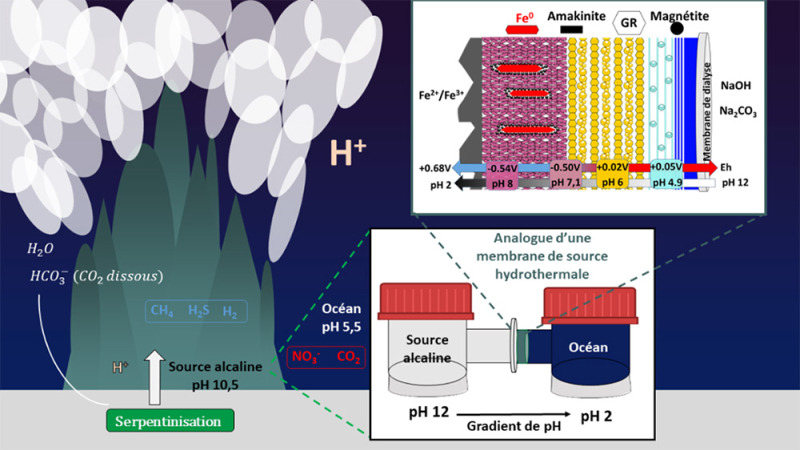
Reconstitution expérimentale d'un analogue de membrane minérale des sources hydrothermales alcalines (AHV).
La précipitation d'oxyhydroxydes de fer à l'interface entre une solution alcaline et une solution acide conduit à la formation d'une barrière minérale structurée.
Cette membrane génère des gradients de pH et de potentiel redox, associés à la dismutation du Fe²⁺ en Fe³⁺ (magnétite) et Fe⁰ qui évoque un mécanisme analogue aux mécanismes vivants, produisant localement des états redox hors équilibre thermodynamique.
© Simon Duval
Vers une reconstitution des premières étapes du métabolisme
Cette étude suggère que des environnements géologiques, comme les cheminées hydrothermales, pourraient avoir joué un rôle clé dans la catalyse de réactions prébiotiques. Elle offre aussi un modèle expérimental pour étudier les processus bioénergétiques qui fonctionnent encre dans les cellules actuelles. Il pourrait également expliquer des transformations géochimiques encore inexpliquées dans des milieux naturels.
À l'avenir, les scientifiques envisagent d'explorer des réactions plus complexes dans ce type de dispositif, notamment la condensation d'unités phosphates, pour se rapprocher des processus cellulaires.
Il s'agit d'une étape de plus vers la reconstitution des conditions ayant permis l'émergence de l'ancêtre commun à toutes les formes de vie sur Terre.