Restez toujours informé: suivez-nous sur Google Actualités (icone ☆)
Afin de subvenir aux besoins de la planète et de réduire la dépendance aux énergies fossiles, l'hydrogène est aujourd'hui envisagé comme une source d'énergie alternative de premier choix. Il peut être produit par électrolyse de l'eau, procédé qui consiste à décomposer la molécule d'eau (H2O) en oxygène (O2) et en hydrogène (H2) à l'aide d'un courant électrique. Or le catalyseur – élément clé de cette réaction chimique –, à ce jour le plus performant, se compose de platine, métal noble, rare et cher, qui rend le procédé trop couteux pour une utilisation industrielle. Le défi actuel est donc d'élaborer des catalyseurs alternatifs, formés de métaux non nobles, qui soient aussi efficaces pour synthétiser l'hydrogène.
C'est là le résultat que des chercheurs de l'Institut des sciences moléculaires de Marseille (CNRS/AMU) et du Laboratoire de chimie et bologie des métaux de Grenoble (CNRS/CEA/UGA) ont obtenu en concevant un complexe catalytique formé d'un métal abondant, le cobalt, et d'un ligand(1) particulier, le thiosemicarbazone. Ce ligand est rédox-actif, autrement dit il peut emmagasiner des électrons et donc servir de médiateur dans la catalyse. Un tel système catalytique doté de deux sites de stockage des électrons et des protons (l'un au niveau du métal, l'autre au niveau du ligand) optimise la réduction des protons en hydrogène.
Les chercheurs ont ensuite étudié le comportement et les performances de ce nouveau catalyseur en combinant des données expérimentales (rendement de la production d'hydrogène) et de modélisation (décomposition des étapes de la réaction de catalyse et identification des composés formés à chaque étape).
Résultat: avec une vitesse de réaction et un rendement équivalents aux catalyseurs disponibles, et un coût énergétique moins élevé, le nouveau complexe catalytique se place parmi les meilleurs existants. Si d'autres travaux doivent être réalisés avant d'envisager une utilisation à large échelle, ces résultats témoignent de la pertinence d'utiliser des ligands rédox-actifs pour améliorer les procédés de synthèse catalytique de l'hydrogène.
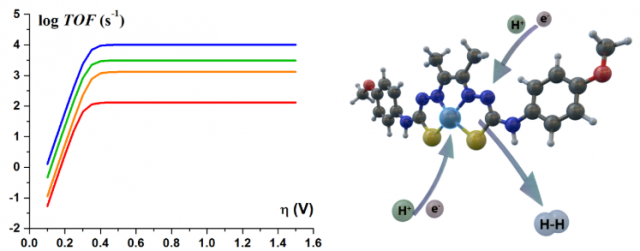
À gauche: graphe comparatif des performances des catalyseurs (vitesse de catalyse, énergie requise). Les courbes en orange et bleu désignent respectivement les complexes de nickel et de cobalt les plus performants de la littérature. Les courbes verte et rouge désignent respectivement les complexes de nickel et de cobalt conçus par l'iSm2 et le LCBM ; le complexe de cobalt et de thiosemicarbazone se distingue par une dépense énergétique moins élevée que les autres, ce qui en fait un catalyseur particulièrement compétitif.
À droite : représentation du catalyseur à base de cobalt et du ligand thiosemicarbazone (les flèches indiquent les sites de rencontres entre électrons et protons).
© M. Orio
Note:
(1) Molécule capable de se lier spécifiquement à une autre molécule ou atome, ici au cobalt.
Référence publication:
T. Straistari, R. Hardré, J. Fize, S. Shova, M. Réglier, V. Artero, M. Orio
Experimental and theoretical studies of a thiosemicarbazone cobalt electrocatalyst for proton reduction.
Chem. Eur. J. – Avril 2018
DOI:10.1002/chem.201801155
Contact chercheur:
Maylis Orio, Institut des Sciences Moléculaires de Marseille (iSm2), Université Aix-Marseille