Réaction chimique - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
Une réaction chimique est une transformation de la matière au cours de laquelle les espèces chimiques (atomiques, ioniques ou moléculaires) qui constituent la matière sont modifiées : les espèces qui sont consommées sont appelées réactifs. Les espèces formées au cours de la réaction sont appelées produits (de réaction). Depuis les travaux de Lavoisier (1777), les scientifiques savent que la réaction chimique se fait sans variation mesurable de la masse : « Rien ne se perd, rien ne se crée, tout se transforme » qui traduit la conservation de la masse.
Les réactions chimiques provoquent un changement de la nature chimique de la matière, sont donc exclues les transformations purement physiques, comme les changements d'état (fusion, solidification, évaporation, ébullition...), l'usure et l'érosion, la rupture... Une réaction peut dégager de l'énergie (en général sous forme de chaleur, mais aussi de la lumière), elle est alors dite « exothermique ». Elle peut nécessiter un apport d'énergie, sous forme de chaleur (donc « produire du froid ») ou de lumière, elle est alors dite « endothermique ». D'une manière générale, une réaction ne peut avoir lieu que si certaines conditions sont réunies (présence de tous les réactifs, conditions de température, de pression, de lumière). Certaines réactions nécessitent ou sont facilitées par la présence d'une substance chimique appelée catalyseur. Classiquement, les réactions chimiques impliquent des changements qui concernent le mouvement des électrons, la formation et la rupture des liaisons chimiques. Cependant, le concept général d'une réaction chimique, en particulier la notion d'équation chimique, est aussi applicable aux transformations élémentaires des particules et des réactions nucléaires. En chimie organique, diverses réactions chimiques sont combinées dans la synthèse chimique afin d'obtenir le produit désiré. En biochimie, des séries de réactions chimiques catalysées par des enzymes forment les voies métaboliques, par lesquelles des synthèses et les décompositions d'habitude impossibles sont exécutées dans une cellule.
Vision microscopique (au niveau atomique)
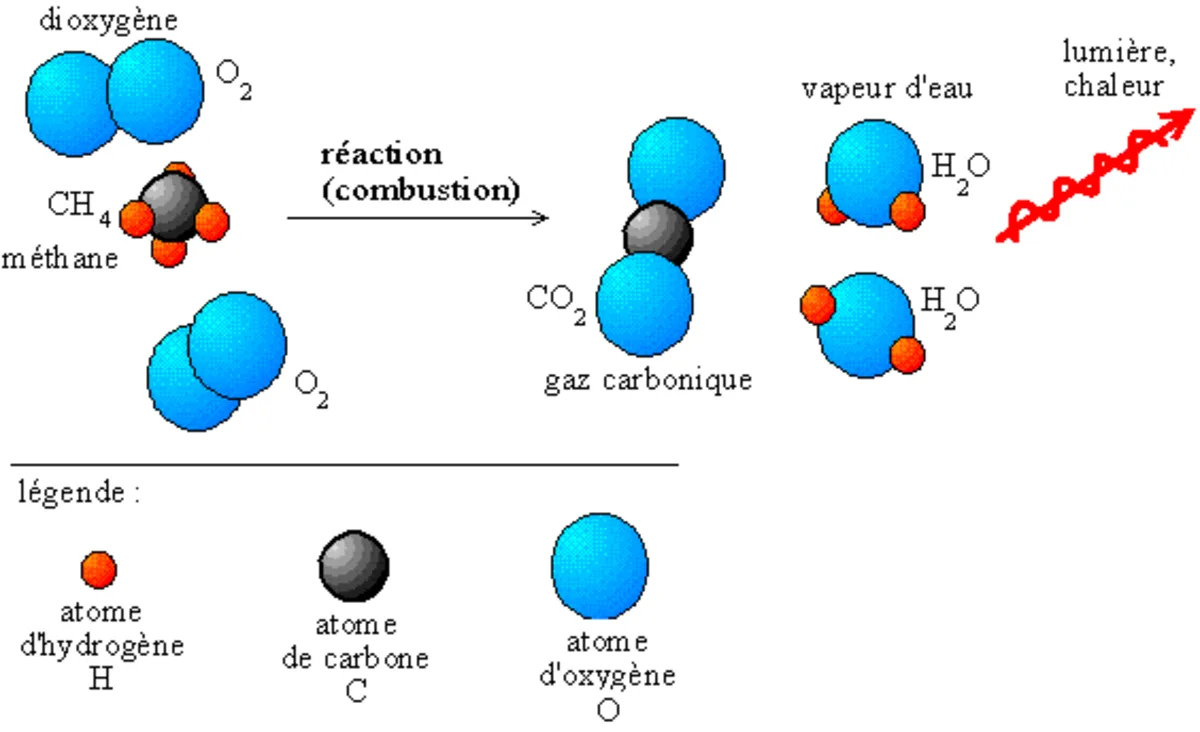
La matière est composée d'atomes regroupés dans des composés chimiques, au cours d'une réaction chimique, les composés s'échangent leurs atomes ; ce faisant, la nature des composés change. Les réactions chimiques ne concernent que les changements de liaisons entre les atomes (liaisons covalentes, liaisons ioniques, liaisons métalliques).
Pour représenter les phénomènes qui ont lieu au cours d'une réaction chimique, on écrit une équation chimique.
Vitesse de réaction
L'étude de l'énergie du système (thermochimie) permet de savoir si une réaction peut se produire ou non, quelle énergie initiale il faut fournir pour franchir la barrière. Mais il y a un autre paramètre important : la vitesse de réaction.
La vitesse de réaction est la mesure de la modification avec le temps des concentrations ou/et pressions des substances engagées dans cette réaction. L'analyse des vitesses de réaction est importante pour beaucoup d'applications comme l'ingénierie chimique ou l'étude des équilibres chimiques.
La vitesse de réaction dépend de :
- La concentration des réactifs: une plus grande concentration augmente la possibilité de collision entre les molécules et ainsi augmente la vitesse de réaction.
- La surface disponible pour le contact entre les molécules spécialement du solide dans les systèmes hétérogènes. Une plus grande surface produit une plus grande vitesse de réaction.
- La pression, qui en augmentant, diminue le volume et donc la distance entre les molécules. Cela augmente la fréquence des collisions des molécules.
- L'énergie d'activation qui est définie comme la quantité d'énergie nécessaire pour que la réaction débute et s'entretienne spontanément.
- La température qui en s'élevant active la réaction augmentant l'énergie des molécules et créant plus de collisions par unité de temps
- L'absence ou la présence d'un catalyseur qui modifie le mécanisme de la réaction qui, à son tour, augmente la vitesse de la réaction abaissant l'énergie d'activation nécessaire. Un catalyseur n'est pas détruit durant la réaction.
- Pour certaines réactions, la présence de radiations électromagnétiques, spécialement les radiations ultraviolettes, sont nécessaires pour briser des liaisons pour commencer la réaction.
Notons que certaines réactions ne dépendent pas de la concentration des réactifs.