Restez toujours informé: suivez-nous sur Google Actualités (icone ☆)
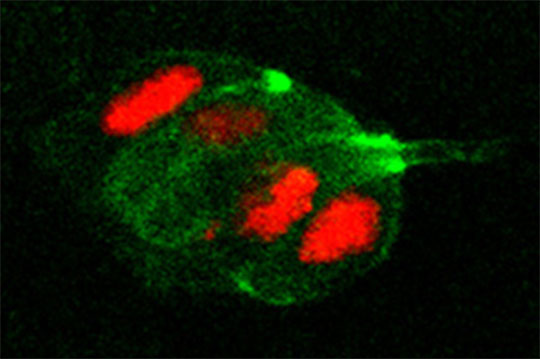
Figure 1: Image confocale d'un groupe de cellules de bordure migrant au sein d'un follicule ovarien en direction de l'ovocyte (vers la droite). La cellule à l'avant du groupe étend une protrusion (structure enrichie en actine) permettant la migration de la cohorte de cellules. Les cellules expriment un marqueur membranaire coloré en vert (mCD8 GFP) et un marqueur nucléaire en rouge (NLS-dsRed).
La migration cellulaire concerne des cellules individuelles ou bien des groupes de cellules migrant de manière collective et coordonnée. La migration collective a été peu étudiée bien qu'elle soit très largement impliquée dans des processus physiologiques, comme le développement embryonnaire, ou pathologiques, notamment lors de maladies inflammatoires ou de la formation de métastases.
Les chercheurs de l'équipe "Migration cellulaire et cancer" au Laboratoire de Biologie Cellulaire et Moléculaire du Contrôle de la Prolifération, utilisent la migration des cellules de bordure dans le follicule ovarien durant l'ovogénèse chez la drosophile comme un modèle de choix pour étudier la migration collective in vivo. Les cellules de bordure forment un groupe d'environ six cellules, qui migrent au milieu d'autres cellules appelées cellules nourricières pour atteindre l'ovocyte (Figure 1). La migration de ce groupe de cellules est divisée en deux phases. Lors de la première qui s'étend du début de la migration jusqu'à la moitié du parcours, les cellules de bordure adoptent un mouvement linéaire, au cours duquel chaque cellule maintient sa position au sein de l'entité, et une seule et même cellule conduit le groupe vers l'avant. Ensuite, à partir de la moitié du parcours, le groupe commence à effectuer des mouvements de rotation sur lui-même ce qui permet à n'importe quelle cellule du groupe de mener la migration jusqu'à l'ovocyte.
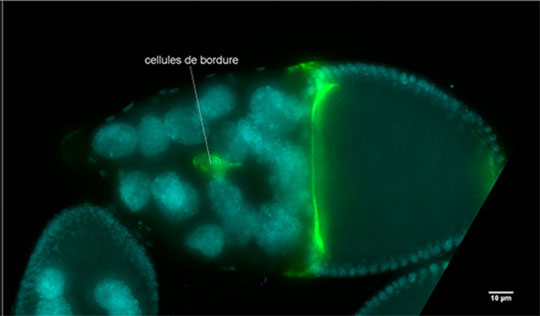
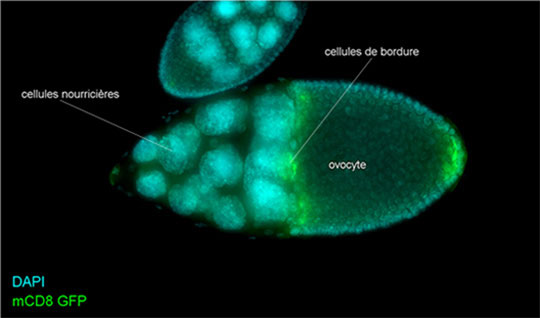
Figure 2: Images de follicules ovariens de drosophile au stade 10 de l'ovogenèse prises avec un microscope à fluorescence. En haut: les cellules de bordure ont atteint l'ovocyte. En bas, les cellules de bordure dans lesquelles l'activité de la Myosine II a été diminuée par RNAi, ne sont pas capables d'arriver à leur destination au stade 10.
© Xiaobo Wang
Les chercheurs ont mis en évidence le rôle de la myosine II dans le contrôle du passage d'un mouvement linéaire à un mouvement rotationnel. La myosine II est une protéine motrice qui joue un rôle majeur lors des processus de migration cellulaire par l'intermédiaire de la régulation de l'actine. Ces travaux mettent en évidence que l'apparition des mouvements de rotation effectués par les cohortes de cellules de bordure est corrélée à une augmentation de l'activité de la myosine II. Il est possible de moduler l'activité de cette protéine dans les cellules de bordure. Tout d'abord, l'activation ou l'inhibition de la myosine II conduit à une migration des cellules ralentie et donc moins efficace au sein du follicule. Cela se traduit par une incapacité des cellules de bordure à atteindre l'ovocyte (Figure 2). De plus, l'inhibition de l'activité de la myosine II entraîne une migration uniquement linéaire, bloquant ainsi le passage d'un mouvement linéaire à rotationnel. En contrepartie, lorsque l'activité de la myosine II est augmentée dans les cellules de bordure, le mouvement majoritairement utilisé est rotationnel.
Ces résultats ont conduit les chercheurs à élucider les mécanismes régulant la myosine II au cours de cette migration collective. La directionnalité du mouvement des cellules de bordure est déterminée par deux voies de signalisation impliquant les récepteurs PVR (Platelet-derived growth factor/Vascular endothelial growth factor receptor) et EGFR (Epidermal Growth Factor Receptor). La migration des cellules de bordure est guidée par un gradient de ligands de PVR et EGFR sécrétés par l'ovocyte. Des études précédentes ont montré que PVR a un rôle crucial dans la première phase alors que l'activité d'EGFR prédomine durant la deuxième phase. Dans cette étude, les chercheurs montrent que les cellules de bordure sur-exprimant PVR ont un phénotype de migration similaire à celui induit par l'inhibition de la myosine II. Ces groupes de cellules migrent moins efficacement en n'utilisant qu'un mouvement linéaire. Au contraire, la surexpression d'EGFR dans les cellules de bordure entraine majoritairement une utilisation du mouvement rotationnel comme mode de migration. Le phénotype obtenu est similaire à celui observé après l'activation de la myosine II. A partir de ces résultats, les chercheurs ont finalement testé si l'activité de la myosine II pouvait être régulée de manière antagoniste par ces deux récepteurs. En effet, l'inhibition de la myosine II dans des cellules de bordure sur-exprimant EGFR induit un blocage du mouvement rotationnel.
En conclusion, cette étude démontre que la myosine II, régulée positivement par EGFR, est le chef d'orchestre du contrôle du mode de migration des cellules de bordure.