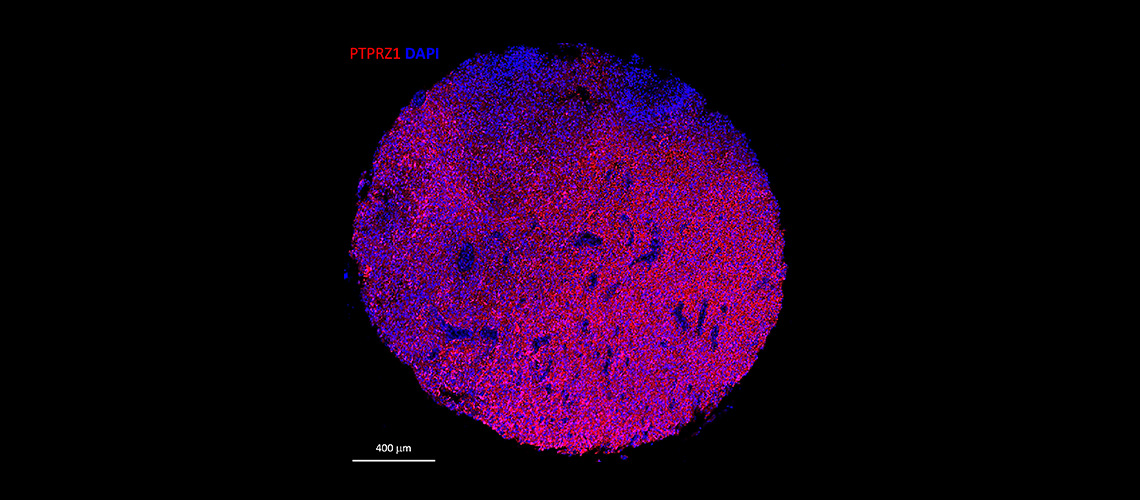
Coloração por imunofluorescência de uma secção de tecido de glioblastoma humano. Em vermelho, os marcadores PTPRZ1, e em azul, os núcleos celulares (escala: 400 μm).
© Denis Migliorini - UNIGE/HUG
Uma equipa da Universidade de Genebra (UNIGE) e dos Hospitais Universitários de Genebra (HUG) conseguiu identificar um marcador específico na superfície das células tumorais e gerar células imunitárias portadoras de um anticorpo para as destruir. Além disso, essas células, chamadas "CAR-T", parecem capazes de alvejar, no tumor, as células doentes que não possuem este antigénio enquanto poupam as células saudáveis.
Estes resultados, publicados na revista Cancer Immunology Research, representam um primeiro passo para o desenvolvimento de ensaios clínicos em humanos.
Os glioblastomas possuem características biológicas que os tornam particularmente difíceis de tratar. Capazes de induzir um microambiente que limita o ataque do sistema imunitário, escapam aos tratamentos padrão e recidivam rapidamente.
Denis Migliorini, professor assistente do Departamento de Medicina da Faculdade de Medicina da UNIGE, titular da Cátedra Fundação ISREC em Imunologia de Tumores Cerebrais, membro do Centro de Pesquisa Translacional em Onco-Hematologia (CRTOH) e médico adjunto agregado, responsável pela Unidade de Neuro-oncologia dos HUG, é especialista em "células CAR-T", ou linfócitos T com recetor antigénico quimérico.
Esta imunoterapia consiste em recolher linfócitos T — células imunitárias — da pessoa doente e modificá-los geneticamente em laboratório para dotá-los de anticorpos capazes de detetar componentes específicos das células tumorais antes de os reintroduzir para que possam atacar o tumor de forma direcionada.
"Há já vários anos que procuramos identificar os marcadores proteicos expressos pelas células que compõem estes gliomas malignos", explica Denis Migliorini. "Um desses marcadores, o PTPRZ1, revelou-se particularmente importante: conseguimos gerar células CAR-T portadoras de anticorpos que visam o PTPRZ1. Esta foi a primeira etapa para criar CAR-T eficazes contra esses tumores."
O ARNm para criar uma célula personalizada
A maioria das células CAR-T é gerada usando vetores virais, uma técnica que provou ser eficaz em algumas doenças, mas é pouco adequada para o cérebro. "De fato, elas persistem por muito tempo em cancros de células sanguíneas. Contudo, o cérebro é um órgão frágil, e essa persistência pode gerar um risco de toxicidade", explica Darel Martinez Bedoya, pós-doutorando no laboratório de Denis Migliorini e principal autor deste estudo.
Os cientistas então introduziram, nos linfócitos T, o RNA mensageiro específico do anticorpo desejado. A maquinaria celular encarrega-se de produzir a proteína certa para formar o recetor que se posicionará na superfície do linfócito e reconhecerá o alvo tumoral.
"Esta técnica tem inúmeras vantagens. As células CAR-T oferecem uma plataforma flexível: permitem diversas adaptações de acordo com as especificidades e evolução do tumor", detalha Darel Martinez Bedoya.
Eficácia e segurança
Para verificar que as CAR-T atacam apenas as células tumorais, a equipa de Genebra testou-as primeiro in vitro, em células saudáveis e doentes.
"Tivemos a agradável surpresa de constatar que, além de as CAR-T não atacarem as células saudáveis, elas também eram capazes, por efeito de proximidade, de identificar e combater células doentes que não possuíam o marcador PTPRZ1", comemora Denis Migliorini. "Neste contexto, as CAR-T são provavelmente capazes de secretar moléculas pró-inflamatórias que estão na origem da eliminação das células tumorais, mesmo na ausência do marcador original."
A segunda etapa consistiu em testar o tratamento in vivo em modelos murinos de glioblastoma. O crescimento do tumor foi controlado, prolongando notavelmente a vida dos ratos sem sinais de toxicidade. "Administrámos as CAR-T diretamente no tumor, o que permite utilizar menos células e reduzir significativamente o risco de toxicidade periférica."
"Todos os sinais são favoráveis para agora considerarmos um primeiro ensaio clínico em humanos", concluem os cientistas.