
Em um artigo publicado na revista Nature Communications, os cientistas revelam informações cruciais sobre o modo de ação do Mavacamten, uma molécula de interesse terapêutico recentemente aprovada pela FDA. Esta pesquisa de ponta abre caminho para o desenvolvimento de uma medicina de precisão contra as doenças cardíacas.
As CHF são um problema de saúde pública que afeta cerca de uma pessoa em 500. De um ponto de vista clínico, essas doenças se manifestam por contrações anormais do coração que, ao longo do tempo, levam a insuficiências cardíacas.
"Essas contrações anormais são devidas à presença de mutações que se expressam nas fibras musculares contráteis chamadas miosinas, que atuam como motores da bomba. Sabemos que existem hoje várias centenas dessas mutações, com efeitos moleculares diferentes, mas sintomas semelhantes." explica o Dr. Julien Robert-Paganin.
Os tratamentos propostos atualmente baseiam-se em cirurgias invasivas, chegando até ao transplante cardíaco nas fases avançadas da doença, com consequências severas na qualidade de vida dos pacientes.
"Surge uma questão diante desses dados: é possível desenvolver medicamentos capazes de corrigir a força de contração do coração modulando diretamente a atividade da miosina?" continua Anne Houdusse.
Duas moléculas têm esses efeitos: o Omecamtiv mecarbil, que ativa a contração das miosinas, e o Mavacamten, que a inibe. Para compreender como essas moléculas mediam seus efeitos opostos, os cientistas utilizaram a cristalografia de raios-X para identificar o sítio de ligação na miosina.
O estudo revela que essas duas moléculas, apesar de terem efeitos inversos na contração da miosina, ligam-se exatamente ao mesmo ponto na fibra muscular. Estudos aprofundados de dinâmica molecular mostram como esses dois medicamentos mediam seus efeitos opostos. De fato, embora a sua o alvo seja o mesmo, as moléculas não têm a mesma mobilidade e estabilidade na cavidade, interagindo de formas diferentes com o domínio motor da miosina, explicando suas ações inversas.
Além de tratar os sintomas, essas moléculas também são capazes de retardar a progressão da doença. O espessamento da parede do coração, que causa complicações a longo prazo, deve-se à força anormal de contração dos músculos cardíacos. Estudos mostraram que, ao corrigir essa força, as paredes são menos danificadas, sugerindo que tomar este tipo de medicamento nas fases iniciais da doença pode diminuir o risco de desenvolver insuficiências cardíacas.
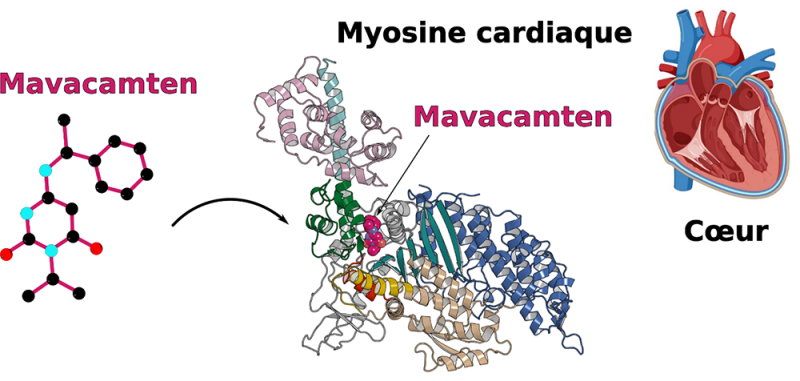
© Julien Robert-Paganin, Daniel Auguin e Anne Houdusse
Para a continuidade deste projeto, os cientistas continuam a combinar o estudo estrutural com a análise das dinâmicas moleculares para caracterizar outras moléculas terapêuticas.
"Nossa equipe também compara o modo de ação de outras moléculas de interesse terapêutico. Com o objetivo de desenvolver uma medicina de precisão, agora é necessário testar a eficácia desses medicamentos para várias doenças cardíacas" indica Julien Robert-Paganin.
Eles têm como objetivo compreender melhor como a contração muscular é controlada para diversificar as moléculas de interesse que podem modular a força produzida.
"Este estudo é um marco fundamental na nossa compreensão dos moduladores de função dos motores moleculares. Enquanto o Mavacamten acaba de ser disponibilizado aos pacientes, nossa pesquisa fornece um conhecimento fundamental para informar os médicos sobre seu modo de ação e aconselhar melhor sobre os futuros tratamentos revolucionários que estão hoje na fase clínica 3 para as doenças cardíacas." conclui Anne Houdusse.
Referência:
Omecamtiv mecarbil and Mavacamten target the same myosin pocket despite antagonistic effects in heart contraction
D. Auguin, J. Robert-Paganin, S. Réty, C. Kikuti, A. David, G. Theumer, A. W. Schmidt, H.-J. Knölker, A. Houdusse.
Nature Communications, 7 de junho de 2024, https://doi.org/10.1038/s41467-024-47587-9