Restez toujours informé: suivez-nous sur Google Actualités (icone ☆)
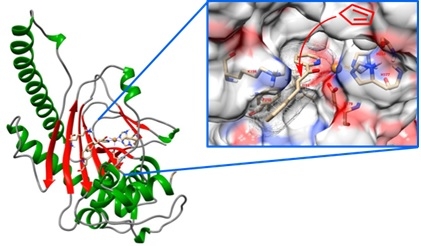
À gauche, la structure cristalline de l'ACCO.
À droite, un agrandissement au niveau de son site actif.
© Wadih Ghattas
Produits ménagers, médicaments, arômes, parfums... Les réactions de Diels-Alder participent à de nombreuses synthèses de produits à haute valeur ajoutée, mais demandent généralement l'emploi de solvants organiques et de catalyseurs comportant des métaux lourds. Des scientifiques de l'Institut de chimie moléculaire et des matériaux d'Orsay (ICMMO, CNRS/Université Paris-Sud) et de l'institut de sciences moléculaires de Marseille (ISM2, CNRS/Université Aix-Marseille/École Centrale Marseille) s'intéressent aux métalloenzymes artificielles, connues pour catalyser ces réactions. Le remplacement des centres métalliques de certaines metalloenzymes naturelles par d'autres métaux peut leur conférer de nouvelles propriétés catalytiques. Les chercheurs ont ainsi pris l'oxydase de l'acide 1-AminoCyclopropane carboxylique (ACCO), une enzyme issue de plantes, et ont échangé l'ion ferreux Fe2+ de son site actif par un ion cuivrique Cu2+.
L'ACCO modifiée montre une grande activité catalytique pour les réactions de Diels-Alder, qui peuvent alors se dérouler dans des conditions douces et sans autre solvant que de l'eau. Si ces réactions peuvent donner quatre isomères différents, soit des molécules de même composition chimique mais d'agencements distincts, un seul est obtenu ici. Les chercheurs envisagent par la suite de moduler l'isomère obtenu grâce à des techniques d'évolution dirigée, qui imitent la sélection naturelle pour modifier protéines et enzymes. Un axe de recherche qui a le vent en poupe, puisque le prix Nobel de chimie 2018 a été décerné à des travaux sur l'évolution dirigée des enzymes.
Références
Wadih Ghattas, Virginie Dubosclard, Sybille Tachon, Morane Beaumet, Régis Guillot, Marius Réglier, A. Jalila Simaan, et Jean-Pierre Mahy.
Cu(II)-containing 1-aminocyclopropane carboxylic acid oxidase is an efficient stereospecific Diels-Alderase
Angewandte Chemie - 5 septembre 2019.
https://doi.org/10.1002/anie.201909407