Restez toujours informé: suivez-nous sur Google Actualités (icone ☆)
Des scientifiques de l'ISCR (CNRS/ENSC Rennes/Université de Rennes 1/INSA Rennes), de l'IRL à UCSD, de l'ISM2 (CNRS/Université d'Aix-Marseille/Ecole Centrale Marseille) et du KAUST en Arabie Saoudite ont récemment démontré la possibilité de préparer de manière éco-efficiente des oléfines chirales par métathèse asymétrique grâce à un catalyseur inédit à base de ruthénium, lui-même chiral. Ces résultats, parus dans la revue JACS, ont également fait l'objet d'un brevet pour les nombreuses possibilités qu'ils offrent en synthèse organique.
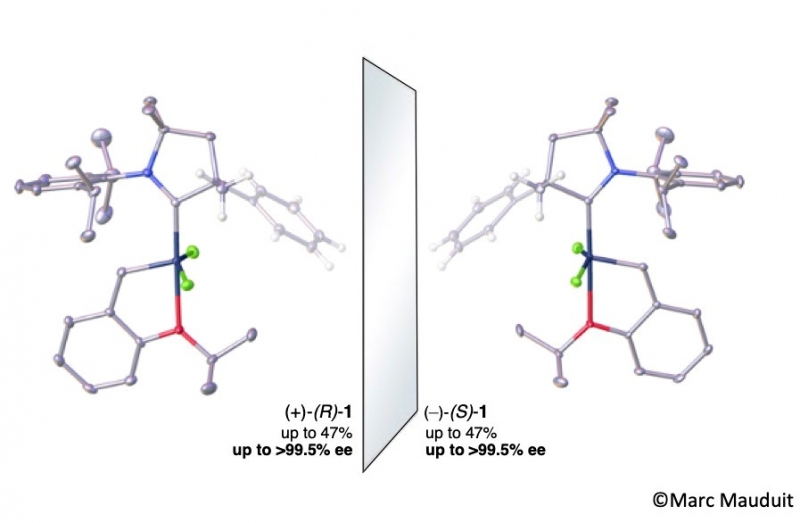
Accessibles en 3 étapes à partir d'aldéhydes bon marchés, les carbènes aminoalkyles cycliques (CAAC) chiraux forment des complexes très stables avec le Ru, ce qui permet d'isoler par HPLC les deux énantiomères (+)-(R)-1 et (-)-(S)-1 avec d'excellents rendements et des puretés optiques optimales (>99.5% ee). © Marc Mauduit
La préparation de composés chiraux, de même formule chimique, mais dont les structures moléculaires sont l'image l'une de l'autre dans un miroir, est un domaine de recherche très actif pour l'industrie cosmétique et pharmacologique. Et pour cause: une différence de structure apparemment négligeable peut avoir un impact considérable sur l'activité biochimique et les propriétés physico-chimiques des deux formes chirales ou "énantiomères". Ainsi, un énantiomère peut soigner tandis que l'autre empoisonne, avoir des odeurs différentes ou être porteur d'une activité biologique tandis que l'autre l'inhibe.
Un mélange racémique, qui contient une quantité équivalente des deux énantiomères, peut donc s'avérer inactif ou même dangereux. La catalyse asymétrique (Prix Nobel de Chimie 2001, Knowles/Noyori/Sharpless), qui permet de préparer de façon sélective un des deux énantiomères d'une molécule chirale, est donc en plein essor. Appliquée en métathèse des oléfines* (Prix Nobel de Chimie 2005, Grubbs/Schrock/Chauvin), elle permet d'accéder à de nombreuses briques moléculaires très recherchées pour la préparation de molécules chirales plus complexes à visée pharmaceutique ou cosmétique.
C'est dans ce contexte que des chercheurs de l'Institut des sciences chimiques de Rennes (CNRS/ENSC Rennes/Université de Rennes 1/INSA Rennes), de l'Unité mixte internationale basée à l'Université de Californie à San Diego (CNRS/UCSD), de l'Institut des sciences moléculaires de Marseille (CNRS/Université d'Aix-Marseille/Ecole Centrale Marseille) et de la King Abdullah University of Science and Technology (KAUST) en Arabie Saoudite ont développé une technologie innovante permettant d'accéder rapidement aux premiers catalyseurs à base de ruthénium optiquement purs contenant des ligands carbèniques chiraux inédits. Ces carbènes aminoalkyles cycliques (CAAC) forment avec le ruthénium des complexes suffisamment stables pour permettre la séparation de leur forme énantiomère par chromatographie en phase liquide à haute performance (HPLC), ce qui permet d'isoler chaque énantiomère.
Le catalyseur chiral ainsi obtenu est optiquement pur à plus de 99% ee et son action catalytique a été testée pour deux types de métathèses asymétrique: l'ouverture de cycles suivi d'une métathèse croisée (ou ROCM) et la métathèse croisée (ou CM). Dans le premier cas, une excellente énantiosélectivité de plus de 90% ee a été observée. En métathèse croisée asymétrique, une sélectivité de 50% ee a pu être démontrée, un résultat très prometteur si l'on considère qu'il surpasse déjà les meilleurs catalyseurs décrits à ce jour dans la littérature. Des calculs théoriques ont permis d'élucider l'origine de cette sélectivité et permettront encore d'optimiser le design architectural des ligands carbènes utilisés. Ces travaux, en rupture avec l'existant, ont fait l'objet d'un dépôt de brevet et ont récemment été publiés dans la revue Journal of the American Chemical Society.
Référence:
Optically Pure C1‑Symmetric Cyclic(alkyl)(amino)carbene Ruthenium Complexes for Asymmetric Olefin Metathesis
Jennifer Morvan, Francois Vermersch, Ziyun Zhang, Laura Falivene, Thomas Vives, Vincent Dorcet, Thierry Roisnel, Christophe Crevisy, Luigi Cavallo, Nicolas Vanthuyne, Guy Bertrand, Rodolphe Jazzar et Marc Mauduit
J. Am. Chem. Soc. 2020, 142, 19895−19901.
https://doi.org/10.1021/jacs.0c10705