Restez toujours informé: suivez-nous sur Google Actualités (icone ☆)
Les fractals, des structures où chaque sous-partie reproduit la forme globale, sont présents dans la nature, comme dans les flocons de neige ou les feuilles de fougère. Cependant, les fractals moléculaires réguliers, où cette autosimilarité se maintient à toutes les échelles, n'avaient jamais été observés jusqu'à présent.

Crédit: MPI f. Terrestrial Microbiology/ Hochberg
Les chercheurs des instituts Max Planck et de l'Université Philipps à Marbourg ont découvert une enzyme microbienne, la citrate synthase d'une cyanobactérie, qui s'assemble spontanément en un fractal régulier appelé triangle de Sierpiński. Ce modèle est une série de triangles qui se répètent à l'infini, avec des triangles de plus en plus petits.
L'enzyme forme des triangles géométriques uniques lors de son assemblage, un phénomène observé accidentellement grâce à la microscopie électronique. Cette découverte a étonné les chercheurs par sa rareté et sa complexité inattendue.
Pour comprendre comment cette structure exceptionnelle s'est formée, l'équipe a collaboré avec un biologiste de l'université de Marbourg pour déterminer la structure moléculaire de l'assemblage. Leur étude a révélé que cette formation fractale résulte d'une violation de la symétrie habituelle des assemblages protéiques. Habituellement, les interactions entre les protéines sont symétriques, conduisant à des structures qui deviennent uniformes à grande échelle.
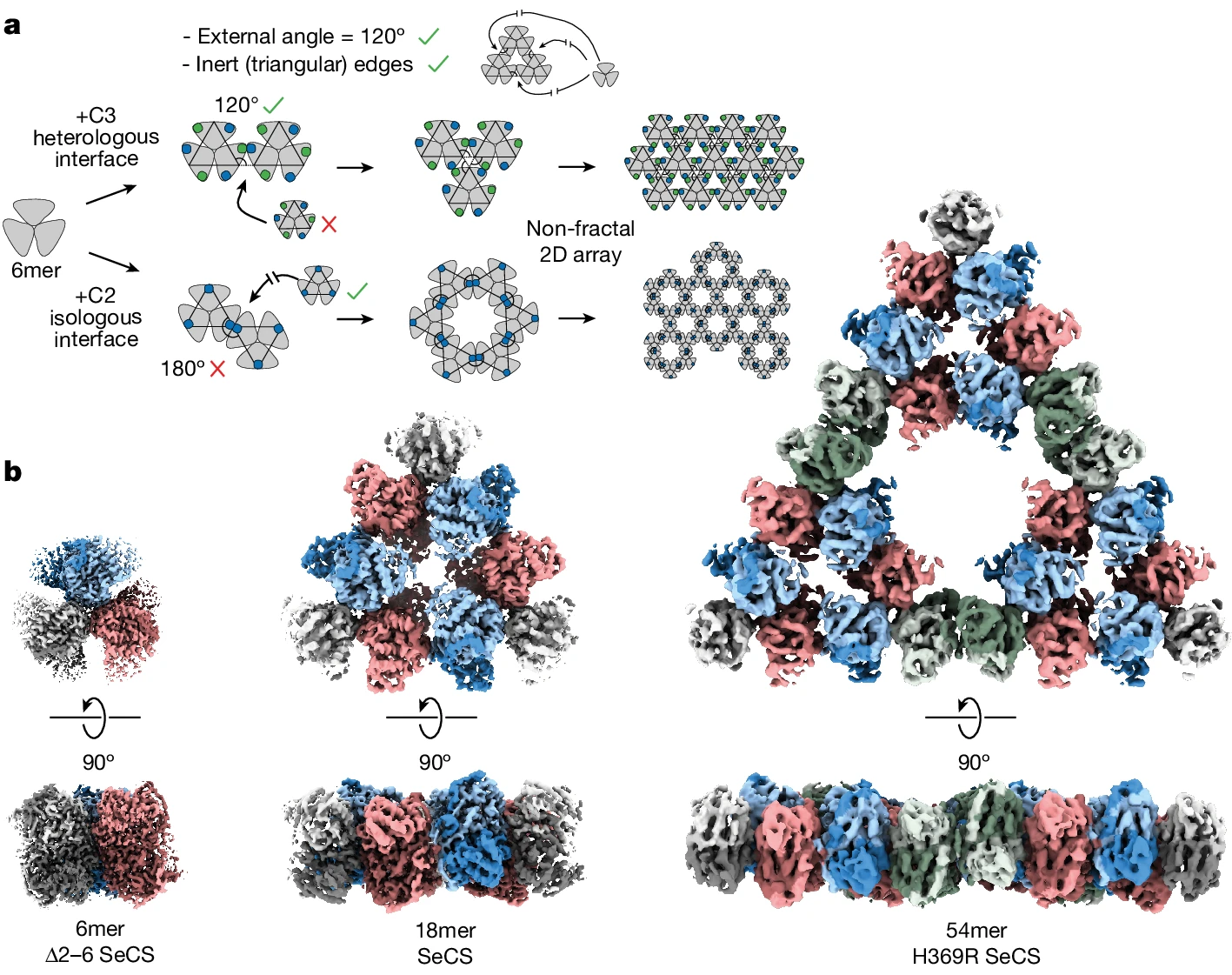
a - Représentation schématique des conditions nécessaires pour produire une fractale de Sierpiński à partir de blocs hexamères et des contraintes basées sur la symétrie sur l'assemblage oligomère. Les points verts et bleus représentent respectivement les interfaces actives ou ouvertes.
b - Cartes de densité Cryo-EM des triangles de Sierpiński des niveaux zéro, un et deux.
Le rôle de cette structure fractale reste incertain. Lorsque l'équipe a modifié génétiquement la bactérie pour empêcher l'assemblage fractal de la citrate synthase, les cellules ont continué à se développer normalement. Cela suggère que l'existence de cette structure pourrait être un accident évolutif sans conséquence notable pour la bactérie.
Pour explorer cette hypothèse, les chercheurs ont recréé en laboratoire le développement évolutif de cette structure protéique. Ils ont utilisé des méthodes statistiques pour retracer la séquence protéique de l'enzyme telle qu'elle était il y a des millions d'années. Les résultats montrent que cette disposition fractale est apparue soudainement suite à un petit nombre de mutations et a disparu rapidement dans plusieurs lignées de cyanobactéries, persistant uniquement dans cette espèce spécifique.
Cette découverte souligne que des structures biologiques complexes et apparemment sans fonction peuvent émerger et persister dans la nature.