Restez toujours informé: suivez-nous sur Google Actualités (icone ☆)
La transformation biologique du CO2 atmosphérique en glucose se produit dans les plantes grâce à la photosynthèse qui est catalysée par l'enzyme Rubisco. D'autres processus bactériens non photosynthétiques savent aussi valoriser le CO2 et réduire cette molécule en source de carbone directement utilisable par la cellule, comme le pyruvate, le monoxyde de carbone ou encore le formiate. Cette dernière réaction est catalysée par l'enzyme formiate déshydrogénase, et en particulier par son site actif à base de Molybdène/Tungstène. Mais les mécanismes de cette réduction restent encore peu compris.
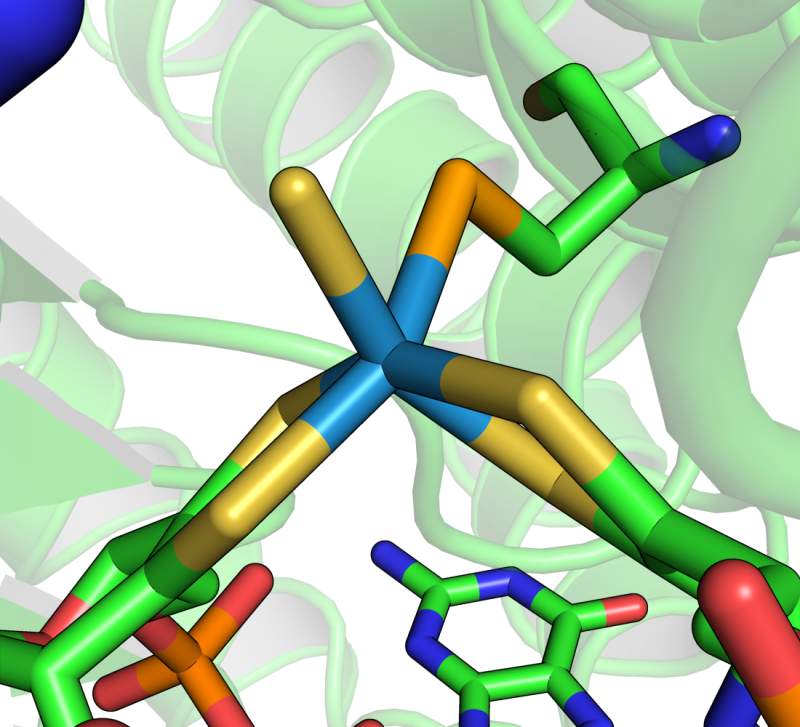
Structure du site actif de la formiate déshydrogénase de D. vulgaris montrant une sphère de coordination du tungstène (bleu) complètement saturée, ce qui empêche la coordination directe du formiate.
© Vincent Fourmond
Des équipes du laboratoire Bioénergétique et ingénierie des protéines (BIP), du laboratoire de chimie bactérienne (LCB, CNRS/Aix-Marseille Université) et de l'ITQB à Lisbonne ont utilisé une méthode cinétique basée sur des mesures d'électrochimie et développée au BIP pour mesurer l'activité de l'enzyme formiate déshydrogénase et clarifier plusieurs questions liées à son mécanisme catalytique. La première concerne la molécule sur laquelle l'enzyme agit, et qu'on appelle substrat: s'agit-il du CO2 ou du bicarbonate, la forme la plus abondante du CO2 dans des conditions physiologiques ? La preuve que le substrat est bien le CO2 a été apportée par des expériences de mesures d'activité électrochimique résolues en temps réel en suivant l'équilibration lente du rapport CO2/bicarbonate.
La seconde question concerne le cycle catalytique. L'analyse de la façon dont l'activité enzymatique dépend des différents paramètres expérimentaux (concentration en CO2, acidité et potentiel d'électrode) a permis de déterminer l'enchaînement des étapes du cycle catalytique et trancher parmi les hypothèses rencontrées dans la littérature. L'excellente résolution temporelle et le contrôle sur l'état de l'enzyme sont les principaux avantages de la mesure d'activité enzymatique par électrochimie utilisée ici. Ces résultats, à retrouver dans la revue Angewandte Chemie Int. Ed., apportent des éléments clefs dont la chimie pourrait s'inspirer pour valoriser le CO2 atmosphérique.
Références:
Formate dehydrogenases reduce CO2 rather than HCO3-: an electrochemical demonstration
Marta Meneghello, Ana Rita Oliveira, Aurore Jacq-Bailly, Inês A. C. Pereira, Christophe Léger & Vincent Fourmond, Angewandte Chemie Int. Ed. 2021
doi: 10.1002/anie.202101167 [Author version on HAL]
Electrochemical Kinetics Support a Second Coordination Sphere Mechanism in Metal-Based Formate Dehydrogenase
Marta Meneghello, Alexandre Uzel, Marianne Broc, Rita R. Manuel, Axel Magalon, Christophe Léger, Inês A. C.Pereira, Anne Walburger & Vincent Fourmond, Angewandte Chemie Int. Ed. 2022
10.1002/anie.202212224