Acide hydroxamique - Définition
La liste des auteurs de cet article est disponible ici.
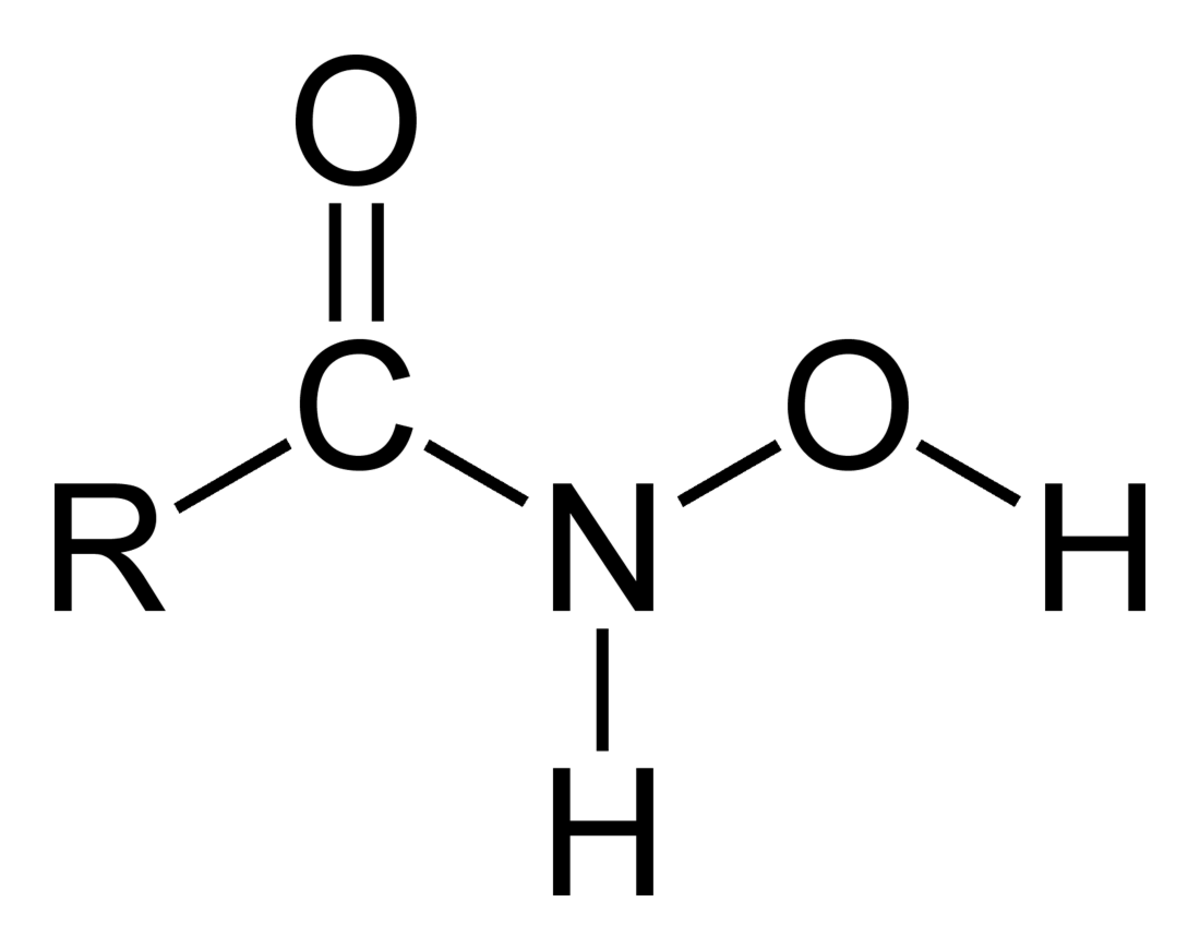
On appelle acide hydroxamique une famille de composés chimiques partageant un même groupe fonctionnel constitué par une hydroxylamine sur un carbonyle : la forme générale de ces acides est donc R–CO–NH–OH.
Les acides hydroxamiques sont utilisés comme chélateurs d'ions métalliques. Ils peuvent être préparés à partir d'aldéhydes via la réaction d'Angeli-Rimini. Une réaction bien connue de ces acides est le réarrangement de Lossen conduisant à des isocyanates.
Les hydroxamates sont des facteurs de croissance essentiels de certains micro-organismes, qui les utilisent comme sidérophores (littéralement : « transporteurs de fer ») pour absorber les ions ferriques Fe3+, qui ne sont pas solubles (contrairement aux ions ferreux Fe2+). Le fer est un composant clef des cytochromes et des protéines fer-soufre telles que les ferrédoxines, qui interviennent notamment dans la photosynthèse et la phosphorylation oxydative.