Isomérie - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
En chimie organique, on parle d'isomérie lorsque deux molécules possèdent la même formule brute mais ont des formules semi-développées ou des formules développées différentes. Ces molécules, appelées isomères, ont des propriétés physiques, chimiques et biologiques différentes.
Le terme isomérie vient du grec ίσος (isos = identique) et μερος (meros = partie).
L'isomérie a été remarquée la première fois en 1827, quand Friedrich Woehler a préparé l'acide isocyanique (H-C=N=O) et a noté que, bien que sa composition élémentaire soit la même que celle de l'acide fulminique (H-N=C=O, préparé par Justus von Liebig l'année précédente), les propriétés chimiques de ces substances sont radicalement différentes. Cette découverte était en contraste avec les théories de l'époque dans le cadre desquelles l'on pensait que les propriétés d'une substance étaient entièrement déterminées par sa formule brute.
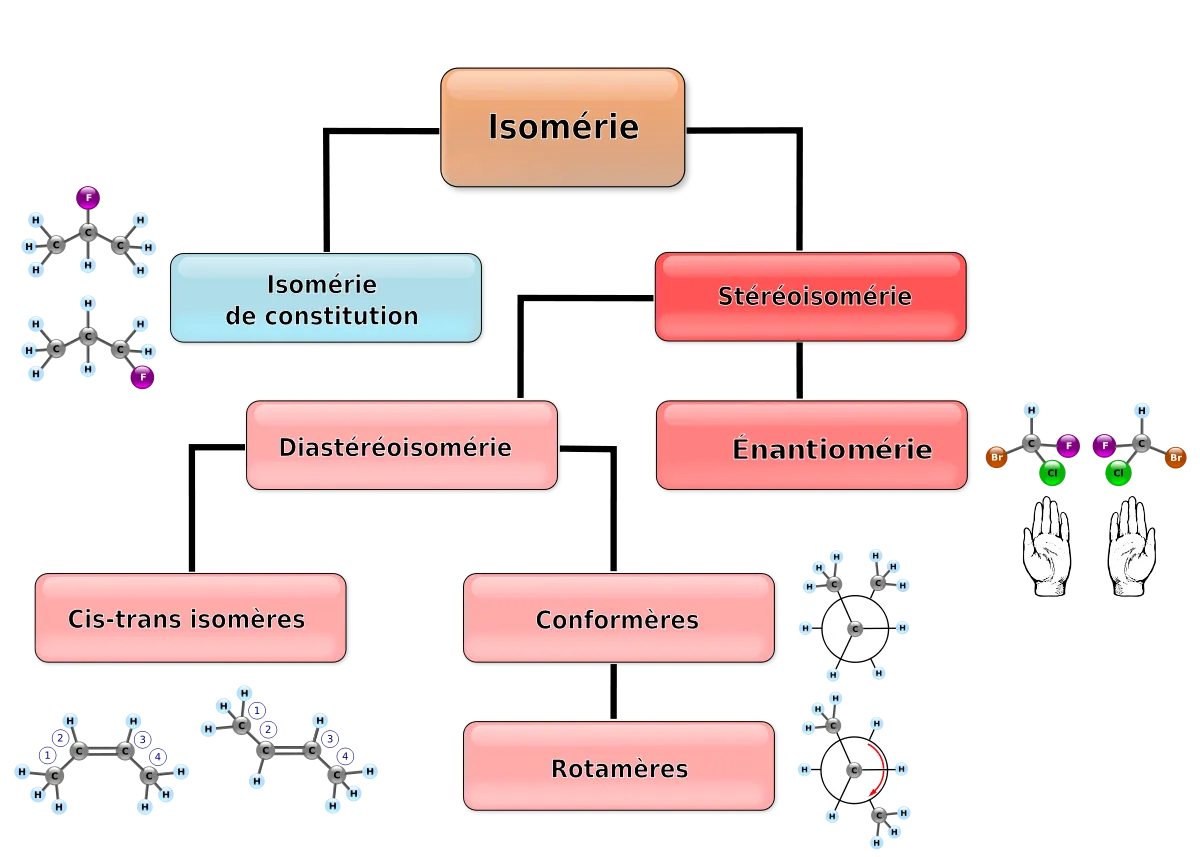
On distingue différentes isoméries, principalement les isoméries de constitution et de configuration (stéréoisomérie). Il y a aussi des isoméries de conformation.
Isomérie de constitution (ou de structure)
L'isomérie de constitution correspond aux isoméries désignant des enchaînements d'atomes différents. Des isomères de constitution ont pour seul point commun leur formule brute; ils ne sont pas constitués des mêmes fonctions chimiques.
Isomérie de chaîne
L'isomérie de chaîne désigne les isomères qui diffèrent par leur chaîne carbonée (squelette). Ces isomères sont caractérisées par leurs propriétés chimiques identiques et propriétés physiques différentes.
Exemple : C4H10
butane méthylpropane CH3-CH2-CH2-CH3 CH3-CH-CH3 | CH3 Isomérie de position de fonction
L'isomérie de position de fonction qualifie les isomères dont un groupement fonctionnel est placé sur des carbones différents de la chaîne carbonée, qui veut dire que c'est la fonction qui se déplace à l'intérieur du squelette. Ces isomères sont caractérisés par leurs propriétés physiques différentes et chimiques légèrement différentes. On appelle ces isomères, des isomères de "position".
Exemple : C3H8O
propan-1-ol propan-2-ol CH2-CH2-CH3 CH3-CH-CH3 | | OH OH Isomérie de nature de fonction
L'isomérie de nature de fonction caractérise les isomères dont les groupes fonctionnels sont différents, donc de propriétés physiques et chimiques différentes. On appelle ces isomères, des isomères de "fonction".
Exemple : C2H6O
éthanol méthoxyméthane CH3-CH2-OH CH3-O-CH3 Isomérie d'insaturation
L'isomérie d'insaturation caractérise les isomères dont les insaturations sont différentes.
Exemple : C3H6
propène cyclopropane CH2=CH-CH3 H2C——CH2 \ / CH2