Polymérisation - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
La polymérisation désigne la réaction chimique, ou le procédé, permettant la synthèse de polymères à partir de molécules réactives qui peuvent être des monomères ou des prépolymères linéaires.
En général, en présence de réactifs (catalyseurs...) et sous l'action de la chaleur et de la pression, il se forme des chaînes macromoléculaires constituées de motifs de répétition identiques ou différents, liés de façon covalente. On obtient des polymères de masses molaires éventuellement élevées, linéaires (ramifiés ou non, en étoile...) car issus de monomères bivalents, ou tridimensionnels.
La plupart des polymères sont thermoplastiques (structure linéaire).
Les macromolécules sont le plus souvent organiques.
On distingue les polymères « synthétiques », comme le polyéthylène (par opposition aux polymères d'origine naturelle, tels la cellulose), et les « artificiels » (cas de l'acétate de cellulose).
En industrie textile, la polymérisation est le processus chimique par lequel des résines ou des plastiques sont fixés à des matières textiles au moyen de la chaleur.
Les différentes réactions chimiques utilisables pour synthétiser des polymères se regroupent en deux familles, comme indiqué ci-dessous.
Polymérisations en chaîne
Le cas le plus important concerne la polymérisation des monomères vinyliques (CH2=CHR) ou de formule CH2=CR1R2. Voir aussi : polyoléfine.
La réaction de polymérisation en chaîne comporte trois étapes successives :
- une étape d'amorçage permet de créer un centre actif (amorceur), de nature radicalaire (résultant par exemple de la décomposition thermique d'un peroxyde ou de l'AIBN), ionique (anionique ou cationique) ou organométallique (cas de la polymérisation coordinative) ;
- l'espèce active permet la création d'une chaîne qui croît par propagation (fixation de monomère sur le centre actif). Dans ce cas, la croissance d'une chaîne polymère résulte exclusivement de réaction(s) entre monomère(s) et site(s) réactif(s) de la chaîne. L'étape de propagation est environ cent mille fois plus rapide que la précédente ;
- étape de terminaison : le centre actif finit à un moment par être détruit.
Elles conduisent à des polymères constitués d'enchaînements -C-C-.
Exemples :
-
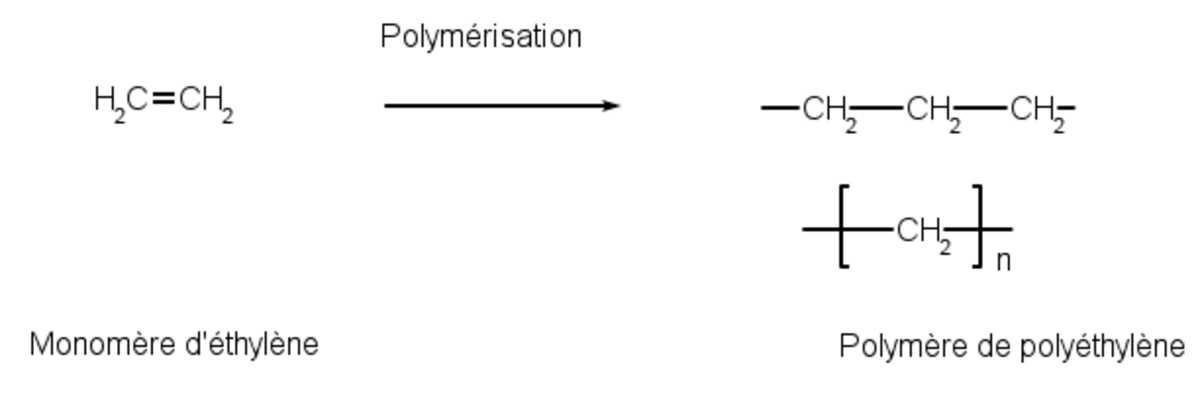
- * polymérisation de l'éthylène, pour former du polyéthylène :
-
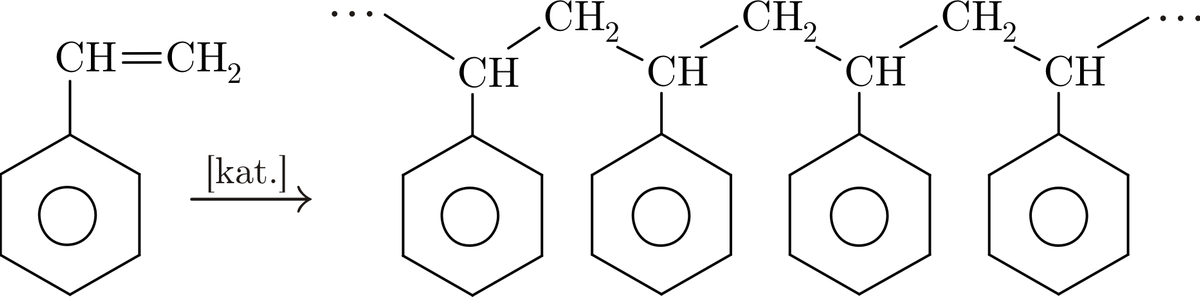
- * polymérisation du styrène, pour synthétiser du polystyrène :
Conditions expérimentales
Il existe quatre techniques de préparation : la polymérisation peut se faire en masse, en émulsion, en suspension ou en solution. Ces techniques présentent chacune des intérêts et inconvénients propres.
Polymérisations par étape
Dans ce cas, on forme des dimères, des trimères... qui peuvent réagir entre eux, et les masses molaires croissent progressivement. Deux types de polymérisations par étapes est à distinguer :
- la polyaddition : cette réaction se fait sans élimination de petites molécules. Exemple : la polyaddition des diols sur les diisocyanates qui conduit aux polyuréthanes.
- la polycondensation : cette réaction se fait avec élimination de petites molécules (H2O, HCl, NH3, etc.). Exemple : la polycondensation des diamines et des diacide carboxyliques qui conduit à des polyamides et à de l’eau :
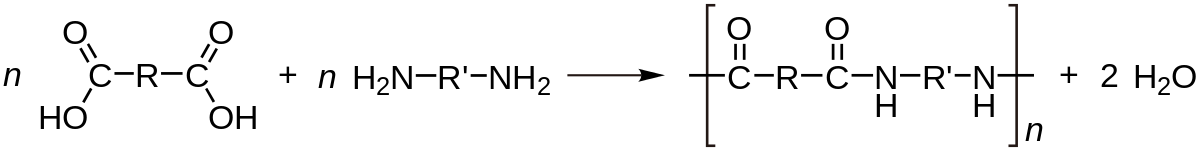
Le choix des matières premières est très vaste et permet une large variété de combinaisons conduisant à des propriétés et des applications différentes. Exemples parmi les polyamides : PA 6, PA 6-6, PA 11, PA 12, PA 4-6.
Les polymères obtenus contiennent souvent des hétéroatomes sur la chaîne principale.