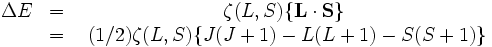Règle de Hund - Définition
La liste des auteurs de cet article est disponible ici.
Règle 3
Cette règle prend en compte les différences d'énergie liées au couplage spin-orbite. Dans le cas où le couplage est faible devant les répulsions électrostatiques des électrons,
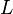
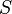
La valeur de
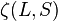
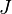
Exemples
Le terme de plus faible énergie du silicium,
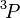
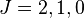
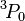
Pour le soufre (S), le terme de plus faible énergie est à nouveau
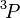
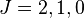
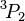
Règle 2
Cette règle vise aussi à minimiser l'énergie de répulsion entre électrons. Elle peut être comprise en utilisant l'analogie classique suivante : si tous les électrons orbitent dans une même direction (celle de moment cinétique orbitalaire le plus élevé), ils se rencontrent moins souvent que si certains d'entre eux orbitent dans des directions opposées. Dans ce cas la force de répulsion électrostatique augmente, ce qui sépare les électrons, ajoutant une énergie potentielle répulsive, et donc augmentant l'énergie.
Exemple
Pour le silicium, il n'y a pas de choix de l'état triplet de spin
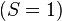
États excités
Les règles de Hund marchent mieux pour la détermination de l'état fondamental d'un atome ou molécule.
Elles sont aussi assez fiables (avec échecs occasionnels) pour déterminer l'état le plus bas en énergie d'une configuration électronique excitée donnée. Alors dans l'atome d'hélium, la première règle prédit bien que l'état triplet 1s2s (3S) est plus bas que le singulet 1s2s (3S). De même pour les molécules organiques, cette règle prédit que le premier état triplet (écrit T1 dans la photochimie) est plus bas que le premier état excité singulet (S1), ce qui est généralement vrai.
Cependant les règles de Hund ne doivent pas être employées pour prévoir l'ordre des états autre que le plus bas état de chaque configuration. (Levine p.303) Par exemple, l'état fondamental de l'atome de titane possède une configuration 3d2, et l'application naïve des règles de Hund suggérerait l'ordre 3F < 3P < 1G < 1D < 1S. Mais en réalité l'état 1D est inférieure en énergie à 1G.