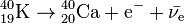Calcium 40 - Définition
La liste des auteurs de cet article est disponible ici.
Le calcium 40, noté 40Ca, est l'isotope du calcium dont le nombre de masse est égal à 40 : son noyau atomique compte 20 protons et 20 neutrons avec un spin 0+ pour une masse atomique de 39,96259098 g/mol. Il est caractérisé par un défaut de masse de 34 846 110 ± 293 eV/c2 et une énergie de liaison nucléaire de 342 051 954 ± 297 eV. Le calcium naturel en contient 96,941 %.
Le noyau de 40Ca est remarquable dans la mesure où il est constitué d'un « nombre magique » à la fois de protons et de neurons ; il est donc « doublement magique ». C'est un noyau stable, bien qu'en relatif déficit de neutrons.
C'est un produit de désintégration du potassium 40 :
Cette réaction illustre bien l'importance de la parité des nombres de protons et de neutrons dans la stabilité d'un noyau : avec 20 protons et 20 neutrons et malgré son déficit de neutrons, le 40Ca est plus stable que le 40K, qui compte 19 protons et 21 neutrons et n'a donc aucun déficit de neutrons ; l'argon 40, avec 18 protons et 22 neutrons est également plus stable que le potassium 40.
Le calcium 48 est l'autre isotope « doublement magique » du calcium (20 protons et 28 neutrons), avec une abondance naturelle de seulement 0,187 % bien qu'il soit quasi-stable.