Insertion cotraductionnelle des protéines membranaires - Définition
La liste des auteurs de cet article est disponible ici.
Insertion cotraductionnelle des protéines membranaires de type II et III
Peptide signal de type II et III
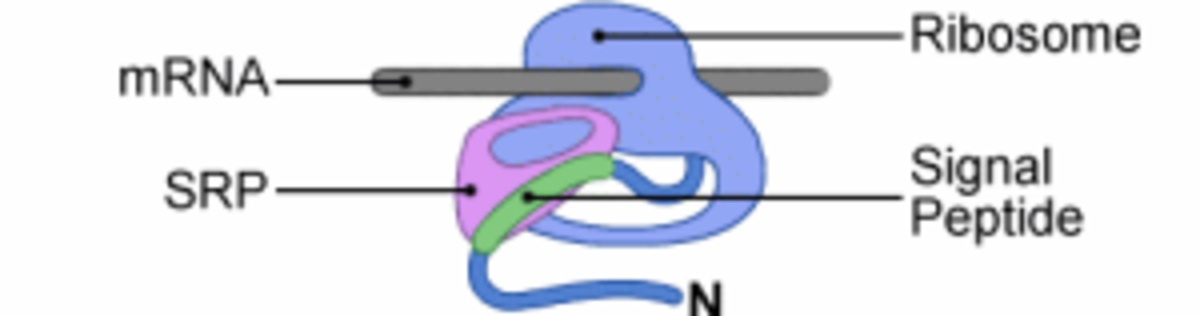
L'insertion cotraductionelle des protéines membranaires de type II et III utilise également le complexe de translocation. C'est le peptide signal qui est différent car il est responsable à la fois de l'adressage au translocon et de l'ancrage membranaire. Ce Peptide Signal ne possède pas de site de clivage comme dans les cas des protéines de type I. Il est généralement plus long (de 18 à 25 résidus essentiellement apolaires) puisqu'il doit être suffisamment long pour former une hélice transmembranaire. De plus, le peptide signal des protéines membranaires de type II et III est positionné à l'intérieur de la séquence plutôt qu'à l'extrémité N-terminale. On parle également de Signal d'Ancrage pour désigner le Peptide Signal des protéines de type II et III.
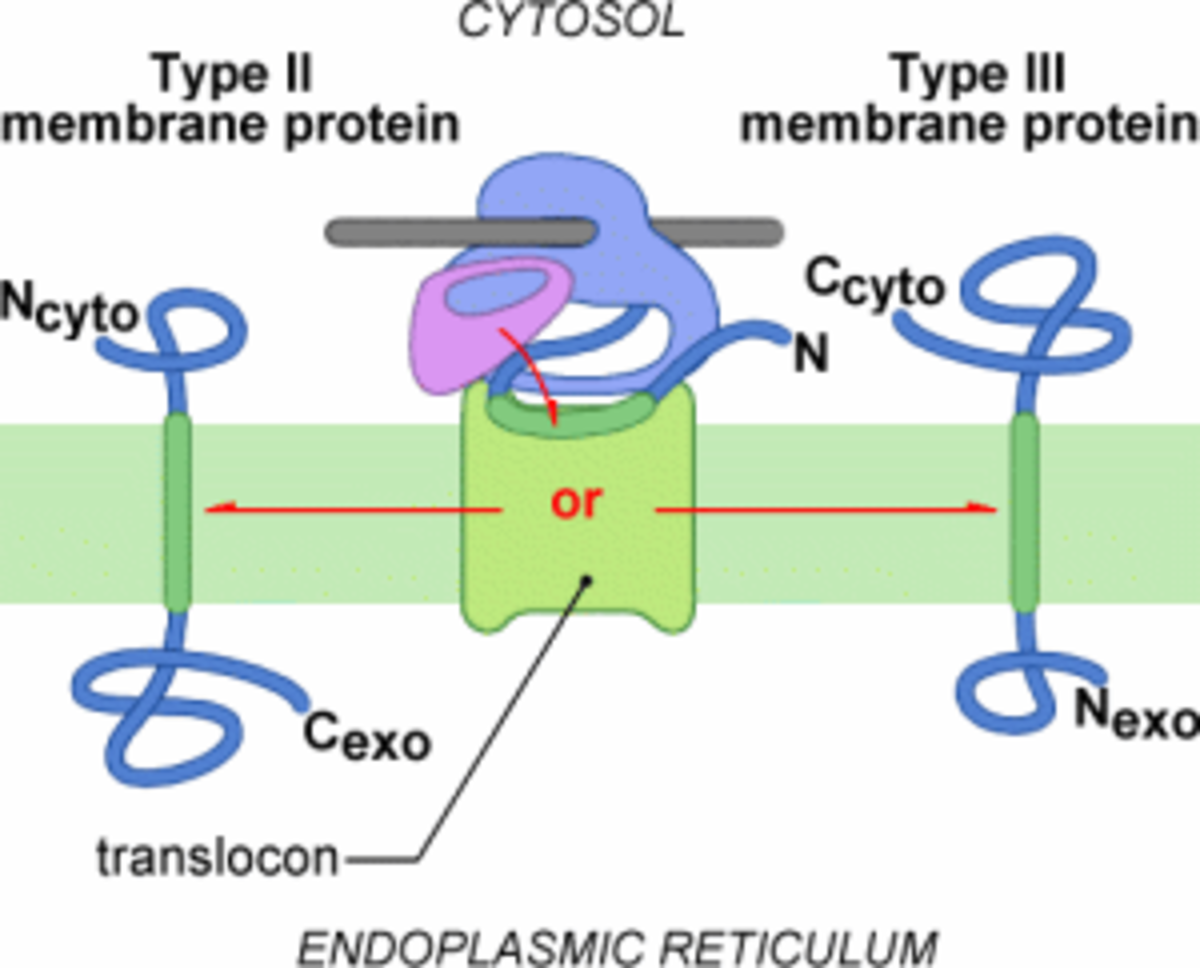
Mais quelle est la différence entre les protéines membranaires de type II et de type III ? En fait, le signal d'ancrage de type II induit une translocation C-terminale, comme dans le cas du peptide signal de type I. En revanche, le signal d'ancrage de type III induit une translocation N-terminale. On parle alors de signal d'ancrage reverse.
Déterminants de l'orientation du signal d'ancrage
Règle du positif à l'intérieur
Le déterminant le mieux connu de l'orientation du Signal d'Ancrage est la distribution des charges à proximité immédiate du cœur hydrophobe du signal. C'est la règle du positive inside (positif à l'intérieur). Autrement dit, les résidus basiques sont statistiquement quatre fois plus abondants du côté cytoplasmique que du côté périplasmique chez les bactéries. La corrélation inverse existe aussi pour les résidus acides (plus de résidus acides dans les segments périsplasmiques), bien que moins marquée. La règle du « positive-inside » se vérifie aussi avec les protéines membranaire du Réticulum Endoplasmique, du chloroplaste et de la mitochondrie.
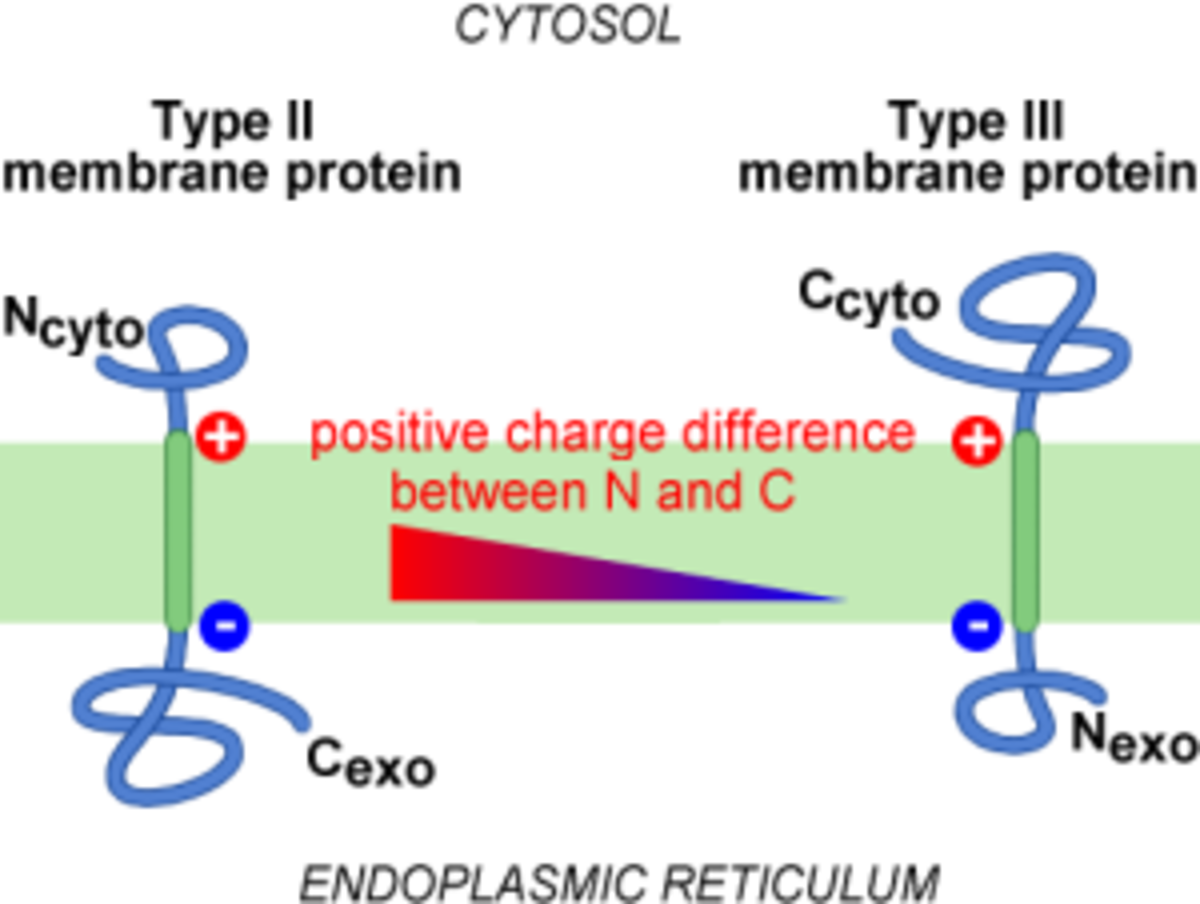
Dans le cas de l'insertion cotraductionnelle, c'est plutôt la différence de charge de part et d'autre du cœur hydrophobe qui guide l'orientation de l'insertion. C'est le côté le plus positif qui est généralement cytoplasmique. Il est donc possible l'orientation du signal en modifiant Ses charges flanquantes. Le changement d'orientation ne touche le plus souvent qu'une partie des protéines produites. Cela signifie tout simplement que la distribution des charges n'est pas le seul déterminant de la topologie membranaire. positive inside rule
Quels sont les facteurs responsables de la règle du « positive inside » ? La réponse n'est pas encore clairement établie à l'heure actuelle. Il est certain que les phospholipides ont une influence importante sur la translocation mais il est difficile de connaître sont rôle exact dans l'orientation des peptides lors de la translocation. Il a été démontré que les phospholipides anioniques pouvaient retenir les charges positives des peptides signaux procaryotes et empêcher leur translocation, suggérant une interaction peptide-lipide directe. Des facteurs protéines interviennent probablement aussi. Récemment, il a été démontré que Sec61p (chez Saccharomyces cerevisiae) contribuait à l'orientation du peptide signal probablement par des interactions de type électrostatique. Il semble que les charges positives puissent directement avec les phospholipides chargés négativement dans le cas des procaryotes.
Hydrophobie du signal
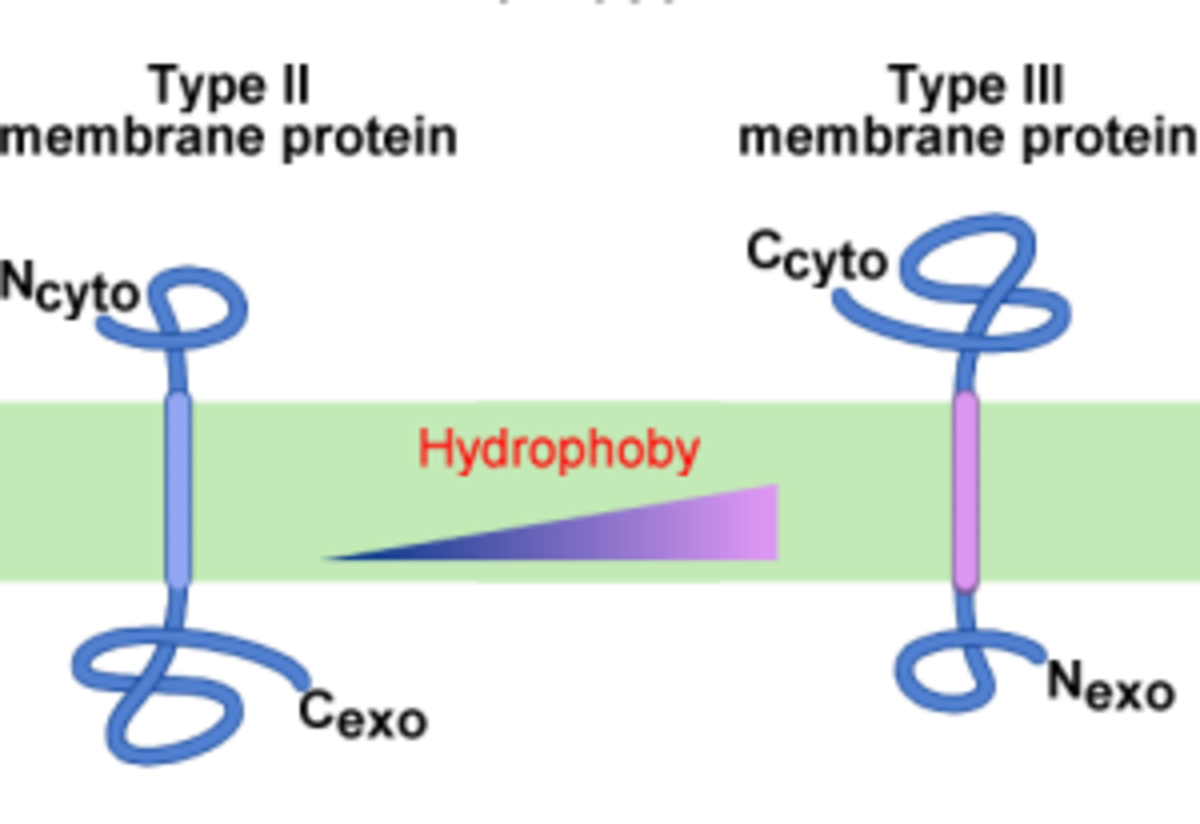
De manière générale, plus le signal d'ancrage est hydrophobe, plus la translocation est N-terminale, i.e. l'insertion est de type III. Un signal d'ancrage suffisamment hydrophobe peut même outrepasser la règle du « positive inside ».
Comment l'hydrophobie du signal intervient dans la topologie membranaire ? Il a été proposé que ce soit un gradient apolaire, plutôt qu'une hydrophobie globale, qui intervienne dans l'orientation du signal. Apparemment, un signal plus hydrophobe sur la fin est plus efficacement transloqué. Cela peut suggérer l'existence d'un site d'ancrage du signal dans le translocon plus hydrophobe du côté extracytoplasmique.
Repliement du domaine N-terminal
Dans le cas des protéines de type II et III, un segment N-terminal est généralement synthétisé avant le peptide signal. Le repliement d'un domaine N-terminal peut donc interférer avec la translocation à travers le translocon et favoriser la rétention de la partie N-terminale dans le cytosol. Ainsi, beaucoup de protéines de type III n'ont pas réellement de domaine structural en N-terminal afin de faciliter la translocation. Dans les autres cas, il est possible que des chaperons interviennent pour empêcher un repliement stable.