1,1,2,2-tétrachloroéthane - Définition
Source: Wikipédia sous licence CC-BY-SA 3.0.
La liste des auteurs de cet article est disponible ici.
La liste des auteurs de cet article est disponible ici.
Introduction
| Tétrachloroéthane | |||
|---|---|---|---|
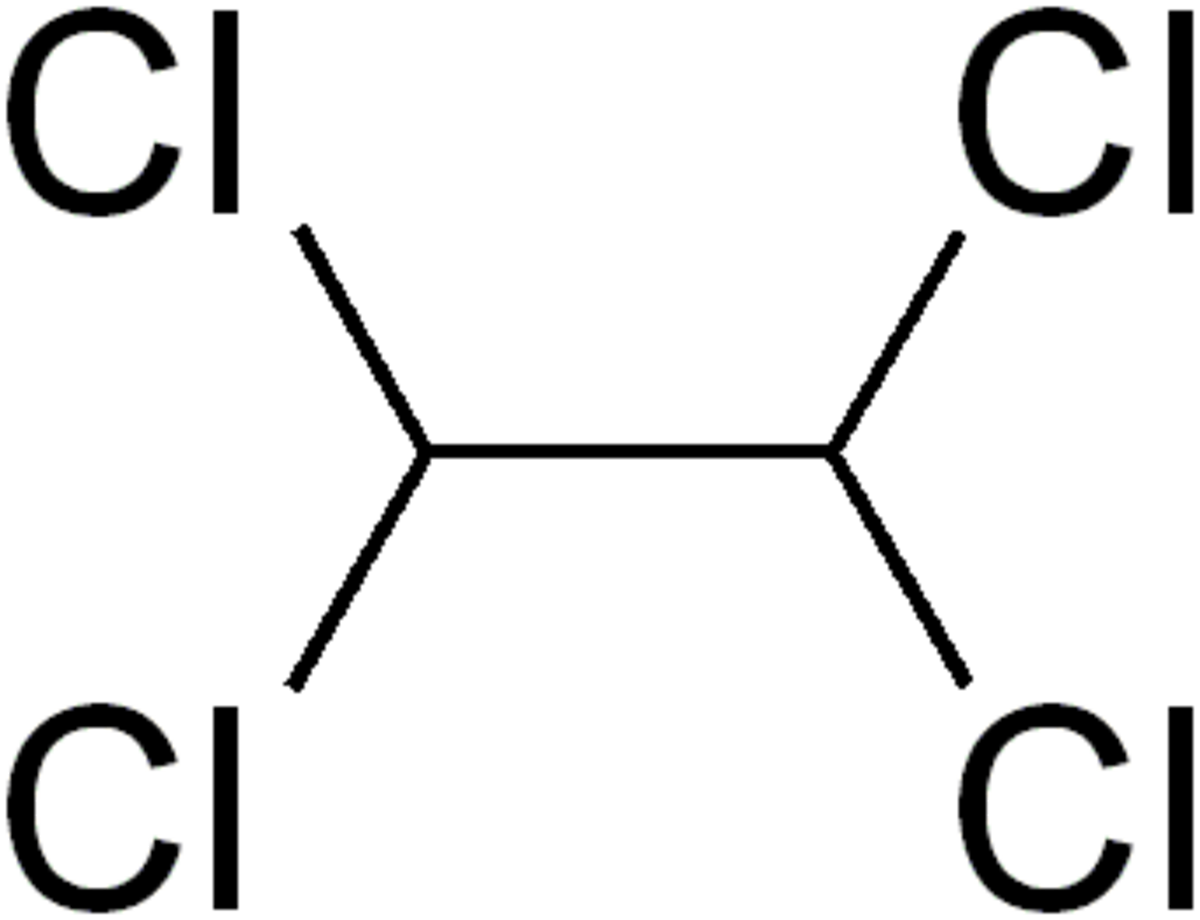
| |||
| Général | |||
| Nom IUPAC | |||
| Synonymes | tétrachloroéthane Tétrachlorure d'acétylène | ||
| No CAS | |||
| No EINECS | |||
| PubChem | |||
| SMILES | |||
| InChI | |||
| Apparence | liquide incolore, d'odeur caractéristique. | ||
| Propriétés chimiques | |||
| Formule brute | C2H2Cl4 | ||
| Masse molaire | 167,849 ± 0,01 g·mol-1 | ||
| Moment dipolaire | 1,32 ± 0,07 D | ||
| Diamètre moléculaire | 0,578 nm | ||
| Propriétés physiques | |||
| T° fusion | -42,5 °C | ||
| T° ébullition | 146 °C | ||
| Solubilité | 2,9 g·l-1 (eau, 20 °C) | ||
| Masse volumique | 1,597 g·cm-3 à 20 °C | ||
| Pression de vapeur saturante | à 25 °C : 780 Pa | ||
| Point critique | 58,4 bar, 388,05 °C | ||
| Thermochimie | |||
| S0 | 244,3 J·K-1·mol-1 | ||
| ΔH0 | -155,6 kJ·mol-1 | ||
| ΔH0 | -195,4 kJ·mol-1 | ||
| ΔH° | 37,64 kJ·mol-1 à 146 °C | ||
| Cp | 168 J·K-1·mol-1 à 25 °C | ||
| Propriétés optiques | |||
| Indice de réfraction |
| ||
| Précautions | |||
| | |||
| |||
| Phrases R : 26/27, 51/53, | |||
| Phrases S : 1/2, 38, 45, 61, | |||
| | |||
| |||
| | |||

| |||
| | |||


Danger | |||
| | |||
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme | |||
| Écotoxicologie | |||
| DL | 200 mg·kg-1 (rat, oral) | ||
| LogP | 2,39 | ||
| Seuil de l’odorat | bas : 0,23 ppm haut : 7,9 ppm | ||
| | |||
Le 1,1,2,2-tétrachloroéthane est un hydrocarbure chloré de formule brute C2H2Cl4. Il est utilisé comme réfrigérant sous le nom de R-130 et comme solvant.
Utilisation
Il était autrefois largement utilisé comme solvant et comme intermédiaire de synthèse dans la production industrielle du trichloréthylène, du tétrachloroéthylène et du 1,2-dichloroéthylène. Toutefois, le 1,1,2,2-tétrachloroéthane n'est plus beaucoup utilisé aux États-Unis en raison d'inquiétudes au sujet de sa toxicité.
Production et synthèse
Il est produit soit :
- C2H2 + 2 Cl2 → C2H2Cl4
- Par chloration de l’éthylène :
- C2H4 + 3 Cl2 → C2H2Cl4 + 2 HCl
- Par chloration du 1,2-dichloroéthane :
- C2H 4Cl2+ 2 Cl2 → C2H2Cl4 + 2 HCl