Acide acrylique - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Acide acrylique | |||
|---|---|---|---|

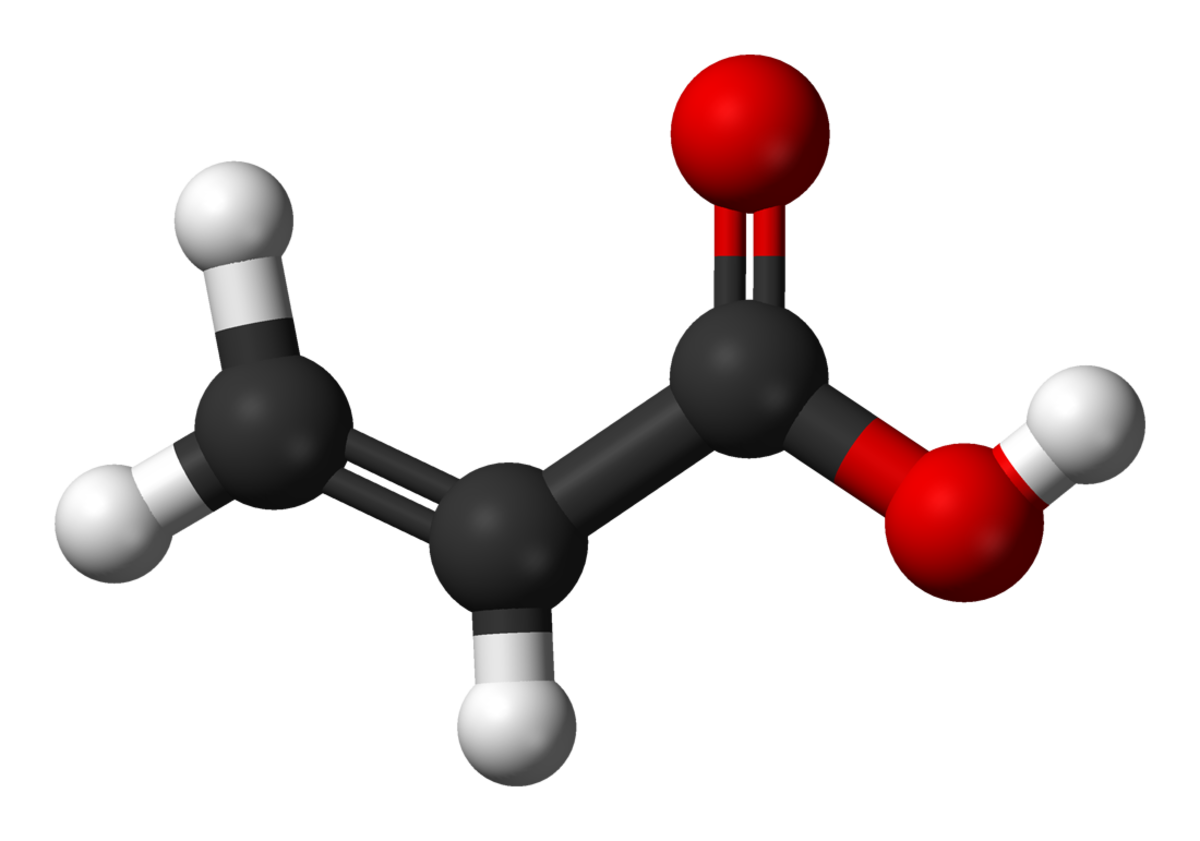
| |||
| Général | |||
| Nom IUPAC | |||
| Synonymes | Acide propénique | ||
| No CAS | |||
| No EINECS | |||
| Apparence | liquide incolore, d'odeur caractéristique. | ||
| Propriétés chimiques | |||
| Formule brute | C3H4O2 | ||
| Masse molaire | 72,0627 ± 0,0033 g·mol-1 | ||
| pKa | 4,25 | ||
| Propriétés physiques | |||
| T° fusion | 14 °C | ||
| T° ébullition | 141 °C | ||
| Solubilité | dans l'eau : miscible | ||
| Masse volumique | (eau = 1) : 1.05 | ||
| T° d’auto-inflammation | 360 °C | ||
| Point d’éclair | 54 °C (coupelle fermée) | ||
| Limites d’explosivité dans l’air | 2,4–8 %vol | ||
| Pression de vapeur saturante | à 20 °C : 413 Pa | ||
| Point critique | 56,7 bar, 341,85 °C | ||
| Thermochimie | |||
| ΔH0 | -330 kJ/mol | ||
| ΔH0 | -384 kJ/mol | ||
| Cp | 144 J/mol.K | ||
| Propriétés électroniques | |||
| 1re énergie d'ionisation | 10,60 eV (gaz) | ||
| Cristallographie | |||
| Classe cristalline ou groupe d’espace | Ibam | ||
| Paramètres de maille | a = 9,952 Å b = 11,767 Å | ||
| Volume | 726,75 Å3 | ||
| Densité théorique | 1,317 | ||
| Précautions | |||
| | |||
| |||
| Phrases R : 10, 20/21/22, 35, 50, | |||
| Phrases S : (1/2), 26, 36/37/39, 45, 61, | |||
| | |||
| |||
| | |||
|
2 3 2 | |||
| | |||
| Produit non classifié | |||
| | |||



Danger | |||
| | |||
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme | |||
| Écotoxicologie | |||
| LogP | 0,36 (estimé) | ||
| Seuil de l’odorat | bas : 0,09 ppm haut : 1 ppm | ||
| | |||
L'acide acrylique ou acide acroléïque ou acide prop-2-ènoïque est un composé organique de formule brute C3H4O2 et de structure moléculaire:
Ce qui peut se résumer par CH2=CHCOOH. C'est un acide carboxylique, un liquide incolore à l'odeur âcre.
Utilisation
L'acide acrylique et ses esters, les acrylates, sont utilisés dans la fabrication de matières plastiques et dans les peintures acryliques.
Production
L'acide acrylique est produit à partir du propylène, un sous-produit issu du raffinage du pétrole.
L'hydrolyse de l'acrylonitrile conduit à l'acide acrylique dont les esters sont les monomères de la synthèse des résines acryliques.
la synthèse d'acide acrylique à partir de l'acétylène s'effectue en présence de nickel carbonyle:
4C2H2 + Ni(CO)4 + 4H2O + 2HCl → 4 CH2 = CH - COOH + NiCl2 + H2.




















































