Cyclohexa-1,4-diène - Définition
La liste des auteurs de cet article est disponible ici.
| 1,4-cyclohexadiène | |||
|---|---|---|---|
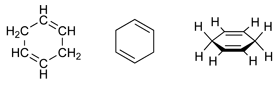
| |||
| Général | |||
| Nom IUPAC | |||
| Synonymes | 1,4-dihydrobenzène, 1,4-CHDN, CHDN | ||
| No CAS | |||
| No EINECS | |||
| PubChem | |||
| ChEBI | |||
| SMILES | |||
| InChI | |||
| Apparence | liquide incolore | ||
| Propriétés chimiques | |||
| Formule brute | C6H8 | ||
| Masse molaire | 80,1277 ± 0,0054 g·mol-1 | ||
| Propriétés physiques | |||
| T° fusion | -49,2 °C | ||
| T° ébullition | 88 °C | ||
| Masse volumique | 0,847 g·cm-3 | ||
| Point d’éclair | -6 °C | ||
| Précautions | |||
| | |||
| |||
| Phrases R : 11, 23/24/25, 36, 45, 48, | |||
| Phrases S : 16, 27, 36/37/39, 45, | |||
| | |||
|
3 2 0 | |||
| Composés apparentés | |||
| Isomère(s) | cyclohexa-1,3-diène | ||
| | |||
Le 1,4-cyclohexadiène est un cycloalcène très inflammable qui se présente sous la forme d'un liquide incolore.
Le 1,4-cyclohexadiène et des composés apparentés peuvent être préparés à partir de benzène en le réduisant avec du lithium ou du sodium en solution dans l'ammoniac liquide, cette réaction étant connue comme la réduction de Birch. Cependant, le 1,4-cyclohexadiène est facilement oxydé en benzène, ceci étant dû à la formation d'un cycle aromatique. Cette conversion en un système aromatique peut être effectuée en laboratoire en utilisant un alcène comme le styrène, avec un agent de transfert d'hydrogène comme le palladium sur charbon actif.
Le γ-terpinène est un dérivé naturel de l'1,4-cyclohexadiène trouvé dans les huiles essentielles de coriandre (Coriandrum sativum), citron (Citrus limon) et cumin (Cuminum cyminum).




















































