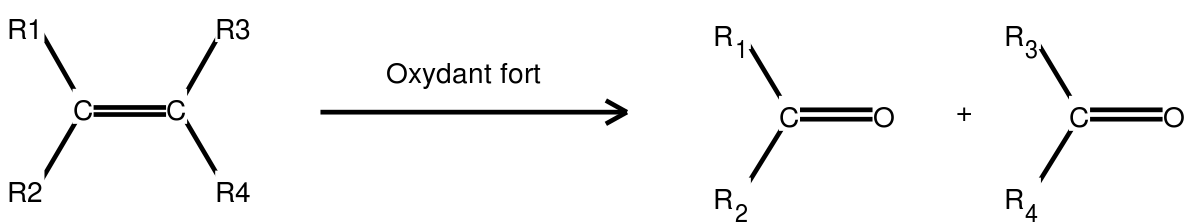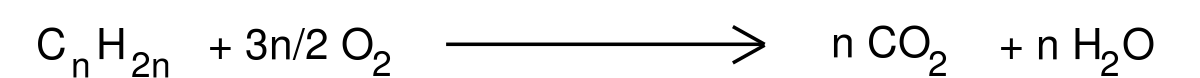Alcène - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
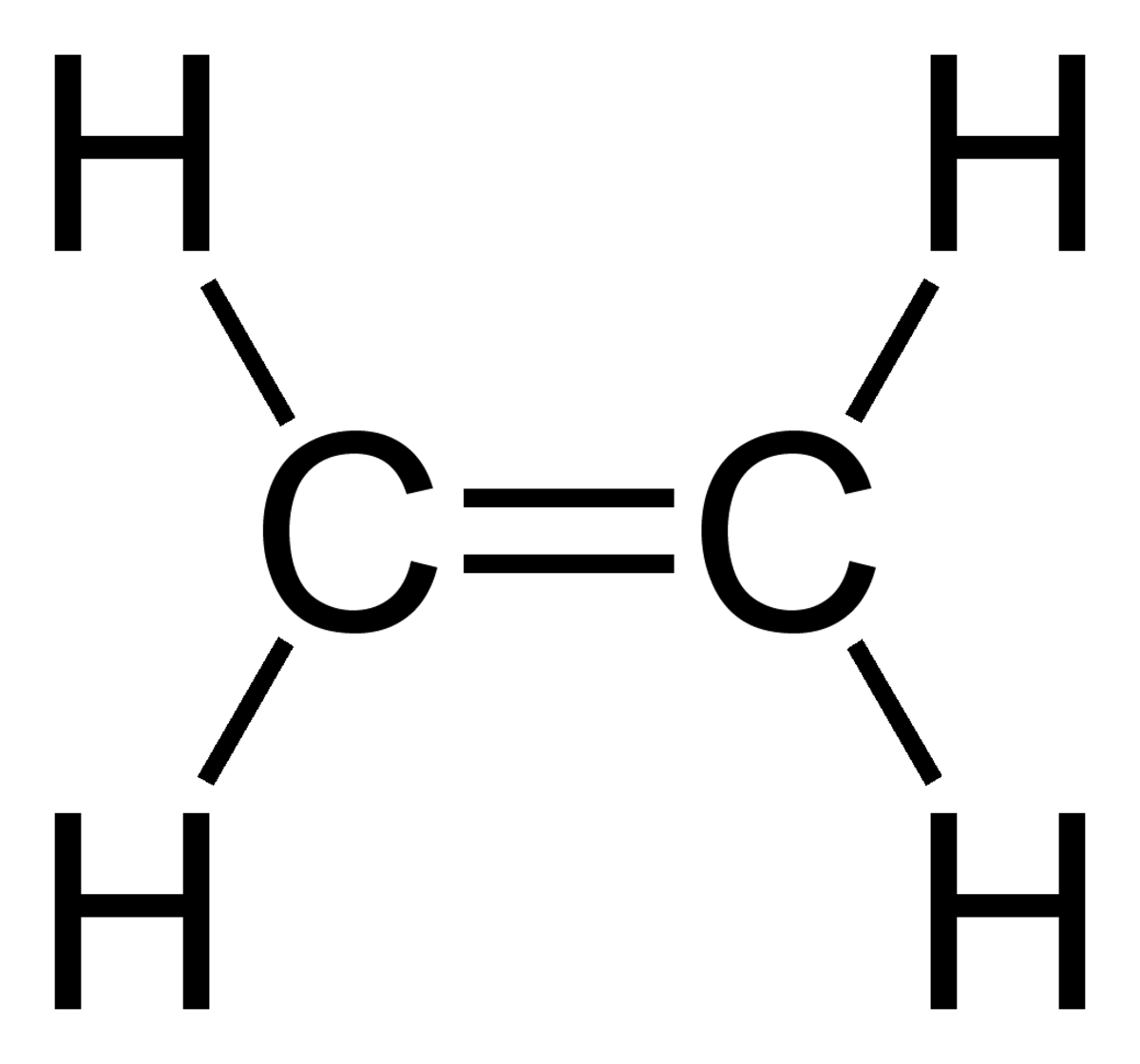
Les alcènes sont des hydrocarbures insaturés, caractérisés par une double liaison covalente entre deux atomes de carbone. Ces liaisons sont toujours de type covalente normale parfaite. Les alcènes non cycliques possèdent une formule brute de la forme CnH2n où n est un entier naturel supérieur ou égal à 2. L'alcène le plus simple est l'éthylène (nom usuel de l'éthène).
Le terme « oléfine » était le nom donné par le passé aux alcènes ; bien qu'encore employé (ainsi que le terme « polyoléfine »), il tombe de plus en plus en désuétude.
Nomenclature
Alcènes non-ramifiés
Il faut utiliser le même nom que celui de l'alcane portant le même nombre d'atomes de carbone, en utilisant le suffixe « -ène » plutôt que « -ane » et en intercalant l'indice de position de la double liaison (voir règle 2a) dans le mot, avant le suffixe, et limité par deux tirets de chaque côté.
Alcènes ramifiés
Voici les règles à suivre pour nommer un alcène ramifié :
Règle 1
Dans la formule de structure, déterminer la chaîne carbonée principale (c'est-à-dire la chaîne la plus longue d'éléments contenant un C) comportant obligatoirement la double liaison. Pratiquement, cela revient à :
- choisir une extrémité de la chaîne carbonée ;
- parcourir la chaîne en passant par le plus grand nombre d'atomes C se suivant.
Règle 2
- Afin de situer la double liaison, numéroter la chaîne principale de façon que le numéro de l'atome C portant la double liaison soit le plus petit possible.
- Suivre la même numérotation pour situer les ramifications.
Règle 3
- Citer le nom de la ramification alkyle, suivi de son indice de position entouré de tirets. Faire suivre du nom de l'alcène comme s'il n'était pas ramifié.
La double liaison peut être déterminée selon les règles de priorité de Cahn-Ingold-Prelog :
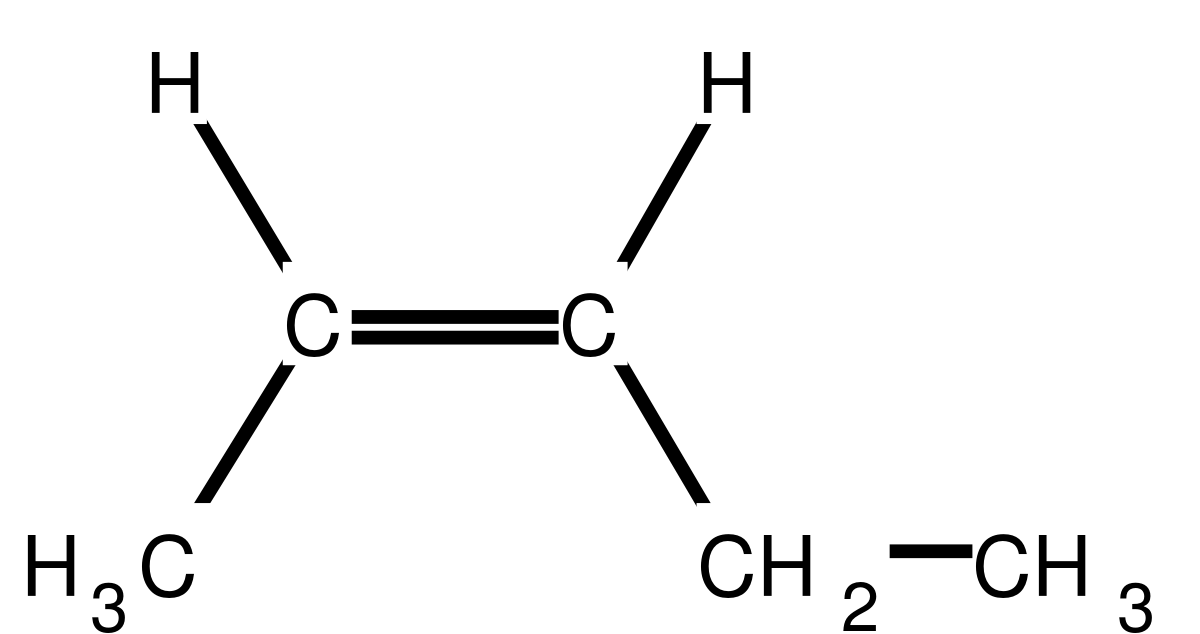
- si les groupes les plus importants liés à chacun des atomes de carbone de la double liaison se retrouvent du même côté par rapport à la double liaison, on parle d'isomère Z (de l'allemand zusammen, ensemble), exemple :
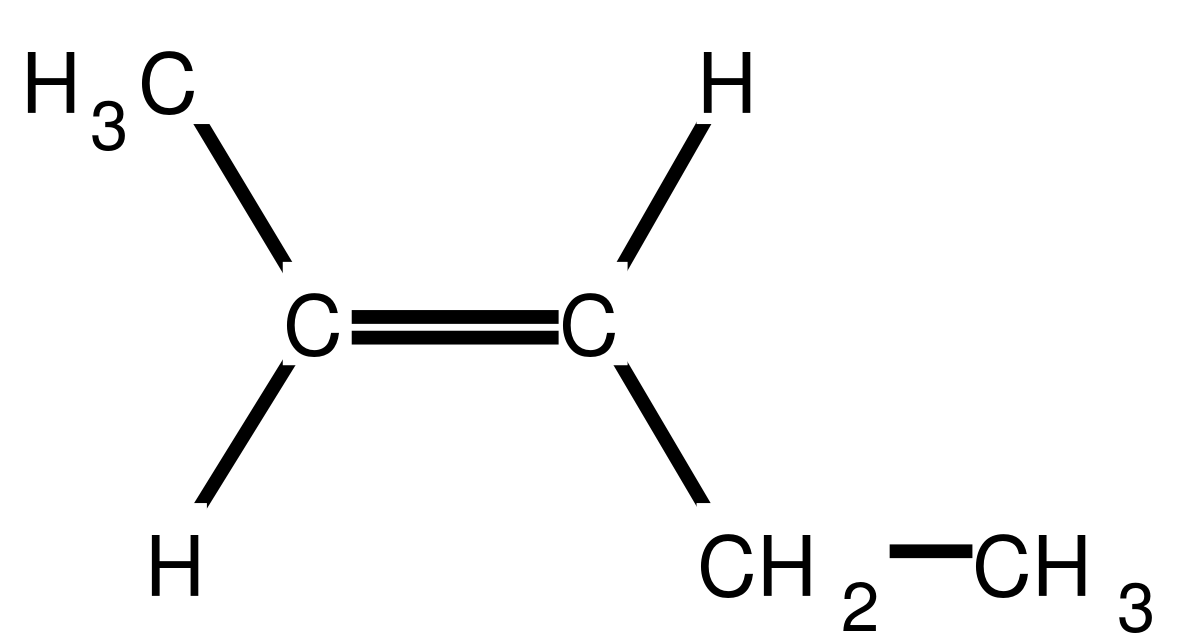
- si les groupes les plus importants liés à chacun des atomes de carbone de la double liaison se retrouvent de côté opposé par rapport à la double liaison, on parle d'isomère E (de l'allemand entgegen, opposé), exemple :
Réactivité
La double liaison est formée d'une liaison σ (sigma) forte (EL = 347 kJ/mol) et d'une liaison π (pi), appelée également liaison insaturée, plus faible (EL = 263 kJ/mol).
La force de la liaison π étant plus faible que celle de la liaison σ, elle cède plus facilement.
Les principales réactions des alcènes sont :
- réaction d'addition sur les carbones porteurs de la double liaison ;
- réaction de destruction et de dégradation.
Réaction d'addition
Lors des réactions, la liaison π peut se rompre : un réactif A-B électrophile va s'additionner sur la double liaison de l'alcène et il y a formation d'un produit saturé. La liaison π a donc été remplacée par deux liaisons σ.
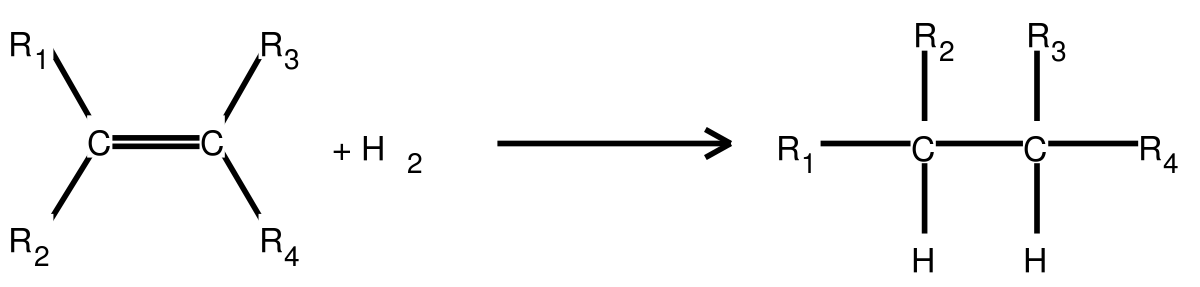
Action du dihydrogène
Action d'un dérivé halogéné
Formation du produit Markovnikov
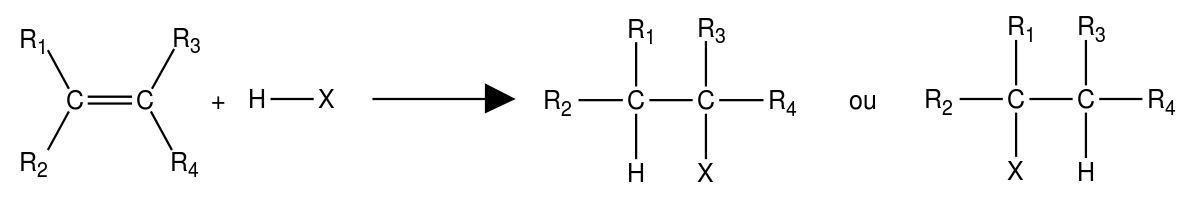
Cette réaction obéit à la règle de Markovnikov :
dans une réaction d'addition de H-X sur un alcène, en l'absence de peroxyde et dans l'obscurité, l'atome d'hydrogène migre vers le carbone moins substitué (c'est-à-dire le plus hydrogéné, pour former le carbocation le plus stable).
Formation du produit Karasch ou anti-Markovnikov
Exemple : addition radicalaire du bromure d'hydrogène sur le 3-méthylhex-3-ène en présence de peroxyde de benzoyle.
Le mécanisme réactionnel est séparable en trois étapes :
initiation :
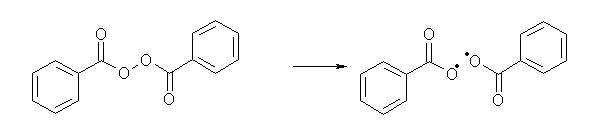
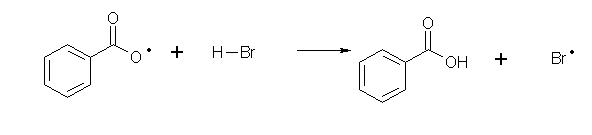
un peroxyde est un bon initiateur de radical, il se coupe spontanément en deux radicaux, qui, à leur tour, attaquent une molécule de HBr pour former le radical de propagation Br• . L'initiation peut aussi être réalisée par irradiation aux UV ;
propagation :
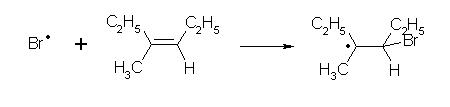
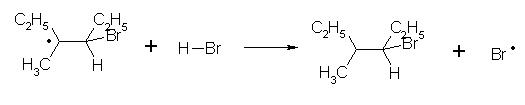
c'est dans l'étape de propagation que se forme le produit final, le 4-bromo-3-méthylhexane ;
terminaison :
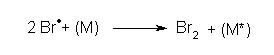
dans cette étape, M est une molécule quelconque du mélange réactionnel, voire une molécule du récipient, elle absorbe l'énergie issue du regroupement de deux radicaux.
Cette réaction, en présence de peroxyde ou d'UV, donne au dérivé halogéné une orientation inverse de celle observée en l'absence de ces réactifs. On parle d'orientation anti-markovnikov, ou d'« effet Karasch ».
Action d'un halogène
→ Halogénation : addition de H-X.
→ Dihalogènation : addition de dichlore ou dibrome (diiode trop peu réactif, difluor trop réactif).
Action de l'eau (hydratation)
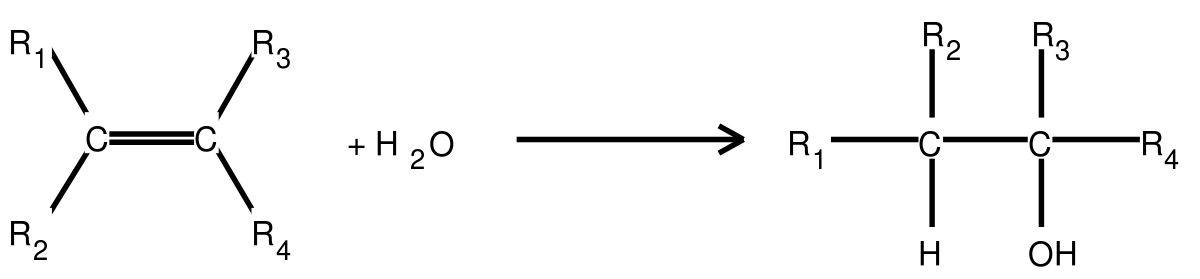
Cette réaction obéit à la règle de Markovnikov :
dans une réaction d'addition de H2O sur un alcène, en l'absence de peroxyde, l'atome d'hydrogène migre vers le carbone le moins substitué (c'est-à-dire le plus hydrogéné).
Action d'un oxydant faible
Sur le plan théorique, on peut utiliser l'ion permanganate en milieu neutre, la réaction sur l'alcène conduit alors à un diol. Cependant, MnO4- reste un oxydant trop fort, on lui préfère en général le tétroxyde d'osmium, qui est utilisé en petite quantité du fait de son extrême toxicité. De ce fait, on utilise de l'eau oxygénée (H2O2) qui le reforme après réaction (il tient donc le rôle de catalyseur).
Action d'une solution d'oxydant fort
(ozonolyse par exemple)
Si R2 est un atome d'hydrogène, alors R1CH=O est un aldéhyde. Néanmoins l'aldéhyde est oxydée en un acide carboxylique par l'ozone présent dans le milieu ; si on désire conserver l'aldéhyde, il est nécessaire d'utiliser un réducteur (le zinc par exemple).
Si R1 et R2 sont des groupes alkyles, alors R1R2C=O est une cétone.
La même réaction est possible avec le permanganate, chauffé en milieu acide. La différence avec l'ozone est que dans le cas de formation d'un aldéhyde, on ne peut empêcher sa transformation en acide carboxylique.
Hydroboration
Permet l'obtention de certains alcools primaires, là où l'addition d'eau conduit à un alcool secondaire, par exemple l'hydroboration du but-1-ène conduit au butan-1-ol, alors qu'une l'hydratation donne du butan-2-ol.
Formation d'époxydes, obtention d'un diol
Un alcène mis en présence de dioxygène conduit à un époxyde. Il est nécessaire de chauffer en présence d'un catalyseur, l'argent par exemple.
En industrie, on utilise des peracides (RCO-O-O-H), dont la liaison peroxyde est très oxydante, le plus utilisé étant le MCPBA (acide méta-chloroperbenzoïque).
L'hydratation (réaction d'addition) d'un peroxyde conduit à un diol.