Réacteur nucléaire naturel d'Oklo - Définition
La liste des auteurs de cet article est disponible ici.
Physique
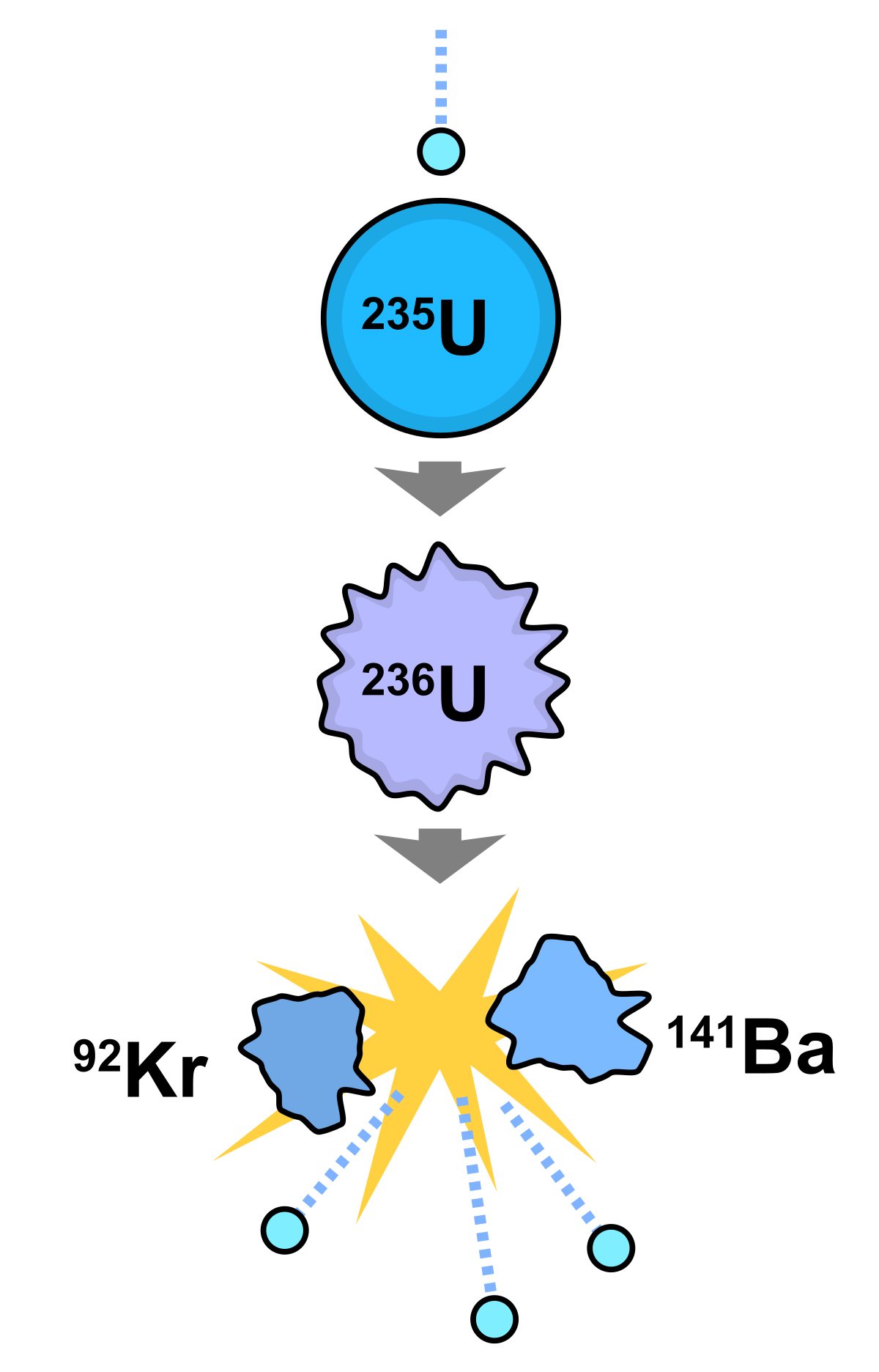
Un réacteur nucléaire naturel est un dépôt d’uranium où les analyses montrent des symptômes de réaction de fission nucléaire en chaîne auto-entretenue. Le phénomène est découvert en 1972 par le physicien français Francis Perrin. Les conditions dans lesquelles une réaction auto-entretenue naturelle peut survenir avaient été décrites en 1956 par Paul Kuroda, à l’Université de l’Arkansas ; les conditions à Oklo sont proches des prévisions théoriques.
Oklo est le seul endroit connu de réacteur nucléaire naturel ; 16 sites y ont été découverts avec des traces de réactions de fission datant de près de 2 milliards d’années
Signature isotopique des produits de fission
Néodyme
Le néodyme trouvé à Oklo a une composition isotopique différente de celle du Nd trouvé ailleurs sur Terre : le Nd typique contient 27 % de 142Nd ; celui de Oklo en contient moins de 6 %, et contient davantage de 143Nd. La composition correspond à celle du produit de la fission du 235U.
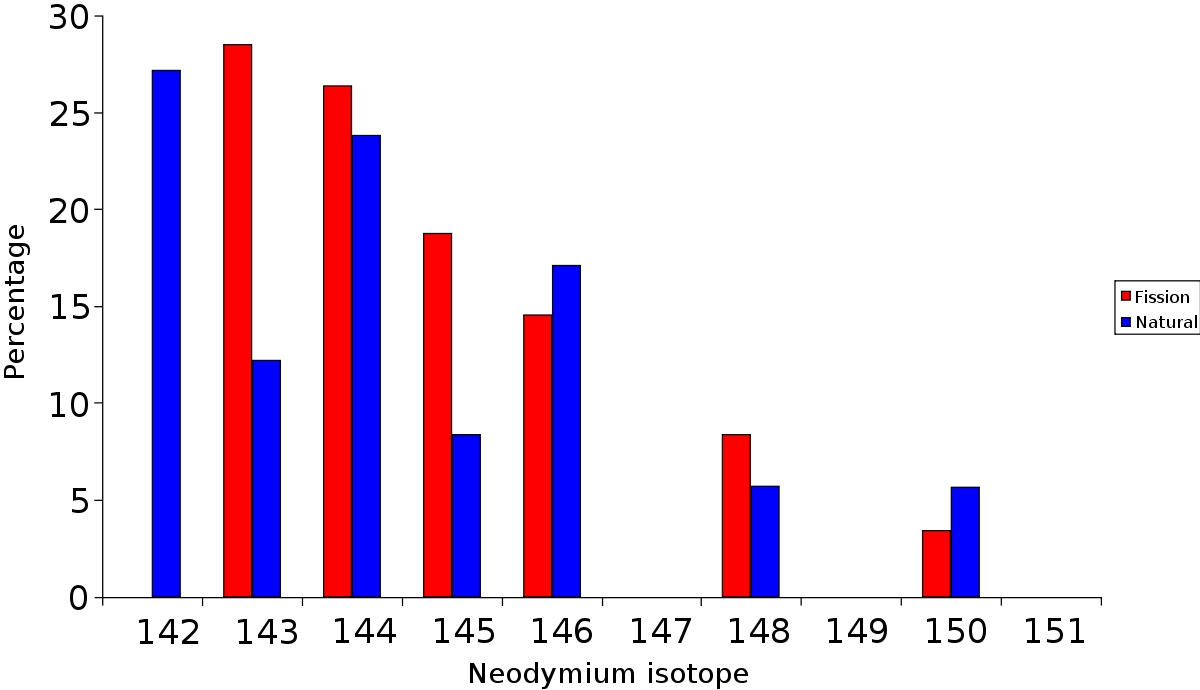
Le 142Ce (un émetteur bêta à longue durée de vie) ne s’est pas encore transformé en 142Nd, même depuis l’extinction des réacteurs.
Ruthénium
Le ruthénium trouvé à Oklo présente une forte concentration de 99Ru (27-30 %, contre 12,7 % typiquement). Ce surplus peut s’expliquer par la désintégration du 99Tc (produit de fission) en 99Ru.
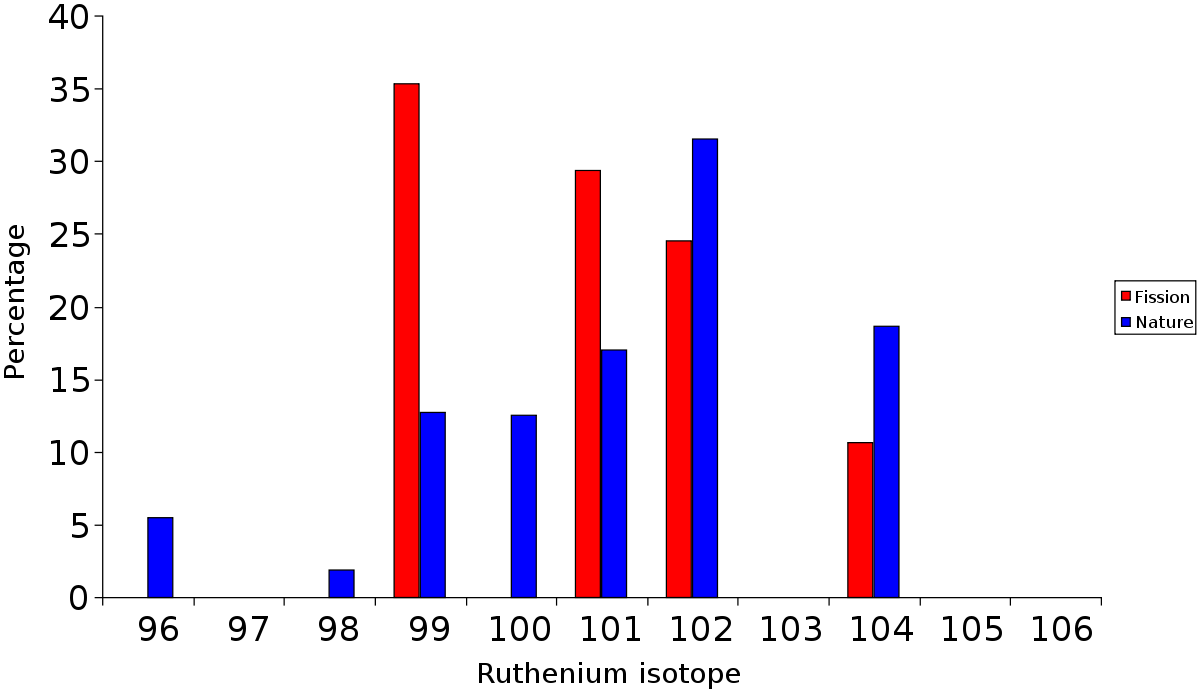
Le 100Mo (un émetteur double bêta à longue durée de vie) ne s’est pas encore transformé en 100Ru, même depuis l’extinction des réacteurs.
Fonctionnement des réacteurs
Un réacteur nucléaire naturel se forme lorsqu’un dépôt de minerai riche en uranium est inondé par de l’eau : l’hydrogène de l’eau agit comme modérateur de neutrons et démarre une réaction en chaîne de fission nucléaire. Au fur et à mesure que la réaction s’intensifie, l’eau s’évapore et s’échappe, ce qui ralentit la réaction, empêchant un emballement du réacteur. Après la baisse de la température, l’eau afflue de nouveau et la réaction raugmente.
La réaction d’Oklo s’est maintenue ainsi pendant plusieurs centaines de milliers d’années. La fission de l’uranium produit cinq isotopes du xénon, qui ont tous été retrouvés dans les restes du réacteur, à différents taux de concentration ; ceci suggère que le taux de la réaction était cyclique (voir explication ci-dessus). D’après les concentrations, la période devait être de 2½ heures environ.
On estime que ces réacteurs naturels ont consommé environ 6 tonnes de 235U (voir la section ), et fonctionné à une puissance de l’ordre de 100 kW, produisant des zones portées à des températures de plusieurs centaines de degrés Celsius. Les produits de fission non volatils n’ont bougé que de quelques centimètres en 2 milliards d’années, ce qui donne un cas d’école de la migration des isotopes radioactifs dans la croûte terrestre, avec des applications dans le stockage en profondeur de déchets de l’industrie nucléaire.
Une telle réaction a pu s’amorcer parce qu’à l’époque où le dépôt a été constitué, la part de l’isotope fissile 235U dans l’uranium naturel était de l’ordre de 3 %, valeur proche de celle de l’uranium enrichi utilisé dans les réacteurs nucléaires actuels. Comme l’uranium 235 a une demi-vie radioactive inférieure à celle de l’uranium 238, son abondance relative diminue avec le temps. La proportion de nos jours est d’environ 0,7 % : un réacteur nucléaire naturel comme celui d’Oklo n’est donc plus possible actuellement.
D’autre part, l’uranium n’est soluble dans l’eau qu’en présence d’oxygène. Quand une eau riche en oxygène érode le minerai d’uranium, elle l’emporte sous forme de particules, et le redépose lorsqu’elle perd son oxygène, augmentant la concentration en uranium à l’endroit où l’oxygène « dégaze » (où il est réduit). La présence d’oxygène — et d’autres phénomènes géologiques — est nécessaire pour élever la concentration de l’uranium. C’est l’augmentation de la teneur en oxygène de l’atmosphère terrestre qui explique que la réaction n’a démarré il n’y a qu’environ 2 milliards d’années, et pas avant, quand les concentrations de 235U étaient encore plus élevées.
Le réacteur naturel d’Oklo est aussi utilisé pour mesurer la constante de structure fine α à différentes époques, et vérifier si elle change au cours du temps, comme l'hypothèse en a été évoquée en mars 2009. En 1976, Alex Shlyakhter a proposé de mesurer les abondances du 149Sm (samarium) pour estimer la section efficace de la capture de neutrons par cet isotope à l’époque d’Oklo, et la comparer à la valeur actuelle.