Dronédarone - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Dronédarone | |
|---|---|
| |
| Général | |
| No CAS | |
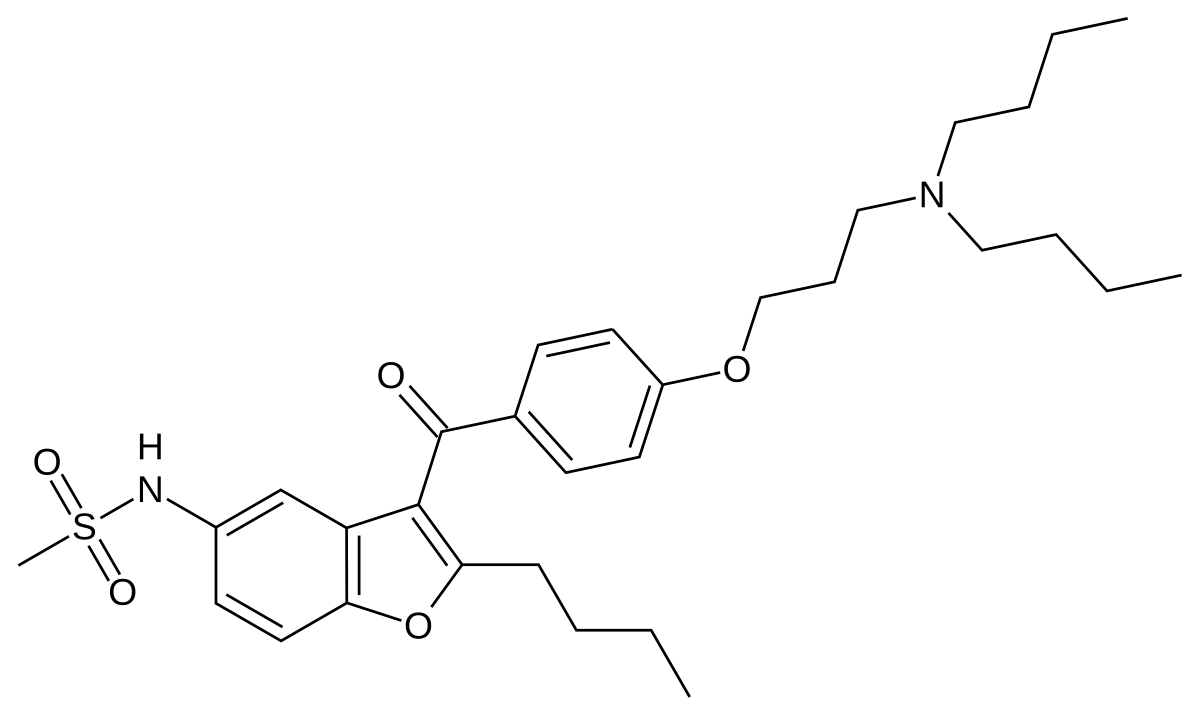
| SMILES | |
| Propriétés chimiques | |
| Formule brute | C31H44N2O5S |
| Masse molaire | 556,756 ± 0,035 g·mol-1 |
| | |
Le dronédarone est un médicament antiarythmique.
Il a reçu un avis de conformité de Santé Canada le 11 août 2009 et est commercialisé dans ce pays sous le nom commercial Multaq, par Sanofi-Aventis. La seule indication retenue est pour les patients ayant subi au moins un épisode de fibrillation auriculaire (FA).
Mode d'action
Il fait partie de la classe III de la classification de Vaughan-Williams et est un équivalent de l'amiodarone. Il joue sur plusieurs canaux ioniques : potassium, sodium, calcium et possède une activité inhibitrice sur le système adrénergique.
Données préliminaires d'efficacité
Les données probantes sur le produit proviennent principalement de l'étude ATHENA, où l'issue principale était un composite des hospitalisations et des décès. Le dronédarone a réduit de 24 % cette issue par rapport au placebo (p < 0,001). La mortalité totale a été réduite de 16 %, toutefois, cette diminution n'était pas statistiquement significative selon le seuil déterminé par l'étude (p = 0,18, p > 0,05). Le nombre de patients inclus dans l'étude (n = 4628) pourrait expliquer le manque de puissance pour cette dernière issue.
Ces résultats sont confirmés par d'autres études, montrant également un ralentissement de la fréquence cardiaque en cas de récidive de fibillation auriculaire.
La dronédarone semble cependant sensiblement moins efficace que l'amiodarone, même si cette dernière est moins bien tolérée.
Métabolisme
La molécule est absorbée par le tube digestif. Il est métabolisé par le cytochrome P450 en une forme peu active. Les molécules potentialisatrices de ce système sont donc susceptible d'augmenter le taux de la forme active de la molécule.
La demi vie d'élimination est de l'ordre de 24 h, ce qui est beaucoup plus court que celle de l'amiodarone.
Données préliminaires d'innocuité
L'avantage de développer une molécule ayant des propriétés pharmacologiques bénéfiques similaires à l'amiodarone est certainement de pouvoir réduire les récidives de FA comme cette dernière molécule, sans toutefois avoir ses effets secondaires. Bien que le suivi moyen dans l'étude ATHENA n'était que de 21 mois, aucune hausse d'effets indésirables pulmonaires ou thyroïdiens n'ont été notés dans le groupe traité par rapport au groupe contrôle (des effets souvent rencontrés avec la prise d'amiodarone). Ces résultats sont prometteurs, mais restent à être validés dans des études avec plus de patients et avec un suivi plus long. Une explication potentielle pour l'absence d'effets secondaires thyroïdiens pour le dronédarone pourrait être le fait que la molécule ne contient pas d'atomes d'iode, comparativement à l'amiodarone.
Il existe un risque d'aggravation d'une insuffisance cardiaque pré-existante, voire une possible augmentation de la mortalité dans ces cas.

















































