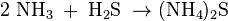Sulfure d'ammonium - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Sulfure d'ammonium | |||
|---|---|---|---|
| Général | |||
| Nom IUPAC | |||
| No CAS | |||
| No EINECS | |||
| SMILES | |||
| InChI | |||
| Apparence | liquide incolore à jaunâtre, odeur proche du sulfure d'hydrogène (œuf pourri) | ||
| Propriétés chimiques | |||
| Formule brute | H8N2S | ||
| Masse molaire | 68,142 ± 0,006 g·mol-1 | ||
| Propriétés physiques | |||
| Masse volumique | 0 997 g·cm-3 (20 °C) | ||
| Limites d’explosivité dans l’air | 4 Vol.-% - 46 Vol.-% | ||
| Pression de vapeur saturante | 546 mbar (20 °C) | ||
| Précautions | |||
| | |||
| |||
| Phrases R : 10, 31, 34, | |||
| Phrases S : 26, 36/37/39, 45, | |||
| | |||
| |||
| | |||
Le sulfure d'ammonium est le sel d'ammonium du sulfure d'hydrogène. Il a pour formule (NH4)2S et appartient à la famille des sulfures.
Occurrence
Dans la nature, c'est un produit du processus de décomposition. Il est aussi présent sous forme gazeuse dans les nuages de l'atmosphère de jupiter.
Synthèse
Le sulfure d'ammonium peut être synthétisé par réaction du sulfure d'hydrogène avec l'ammoniac (gazeux ou en solution aqueuse) en excès.
Propriétés
C'est un composé relativement instable (cristaux se décomposant à -18 °C, mais qui existe et est plus stable en solution aqueuse. Avec un pKa dépassant 15, l'ion hydrosulfure ne peut être déprotoné de façon significative par l'ammoniac. Ainsi, de tells solutions consistent principalement en un mélange d'ammoniac et d'hydrosulfure d'ammonium (NH4)SH. Il a une odeur nauséabonde, proche de celle du sulfure d'hydrogène (œuf pourri), et ses solutions acqueuses peuvent être dangereuses précisément en émettant du H2S.
Utilisations
Le sulfure d'ammonium est souvent utilisé en analyse qualitative non-organique; il permet, en se liant avec le cation métallique lourd (nickel, cobalt, fer, manganèse, chrome, aluminium ou zinc) d'un échantillon inconnu de le faire précipiter, et d'ainsi d'aider à les identifier par des tests de détection.
Le sulfure d'ammonium est aussi utilisé dans le développement photographique, pour appliquer la patine de bronze et dans la fabrication textile.
En raison de son odeur nauséabonde, il est un ingrédient actif de nombreux accessoires de farces et attrapes, et en particulier de certaines boules puantes.