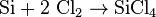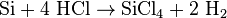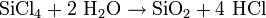Tétrachlorure de silicium - Définition
Source: Wikipédia sous licence CC-BY-SA 3.0.
La liste des auteurs de cet article est disponible ici.
La liste des auteurs de cet article est disponible ici.
Introduction
| Tétrachlorure de silicium | ||
|---|---|---|
|
| ||
| Général | ||
| Nom IUPAC | ||
| Synonymes | Tétrachlorosilane Chlorure de silicium | |
| No CAS | ||
| No EINECS | ||
| PubChem | ||
| SMILES | ||
| InChI | ||
| Apparence | liquide incolore, clair et fumant, d'odeur acre. | |
| Propriétés chimiques | ||
| Formule brute | SiCl4 | |
| Masse molaire | 169,898 ± 0,008 g·mol-1 | |
| Propriétés physiques | ||
| T° fusion | -68 °C | |
| T° ébullition | 57 °C | |
| Solubilité | dans l'eau : réaction bonne dans les solvants chlorés | |
| Masse volumique | 1,48 g·cm-3 | |
| Pression de vapeur saturante | à 20 °C : 26 kPa | |
| Point critique | 35,9 bar, 234,95 °C | |
| Thermochimie | ||
| ΔH° | 28,7 kJ·mol-1 (1 atm, 57,65 °C); 29,7 kJ·mol-1 (1 atm, 25 °C) | |
| Précautions | ||
| | ||
| ||
| Phrases R : 14, 36/37/38, | ||
| Phrases S : (2), 7/8, 26, | ||
| | ||
|
0 3 2 | ||
| | ||

Attention | ||
| Peau | Pas d'absorption par la peau. Corrosif et irritant. | |
| Yeux | Absorption par les yeux. Irritant et corrosif. Brule et provoque des lésions, voire une possible perte de la vue. | |
| | ||
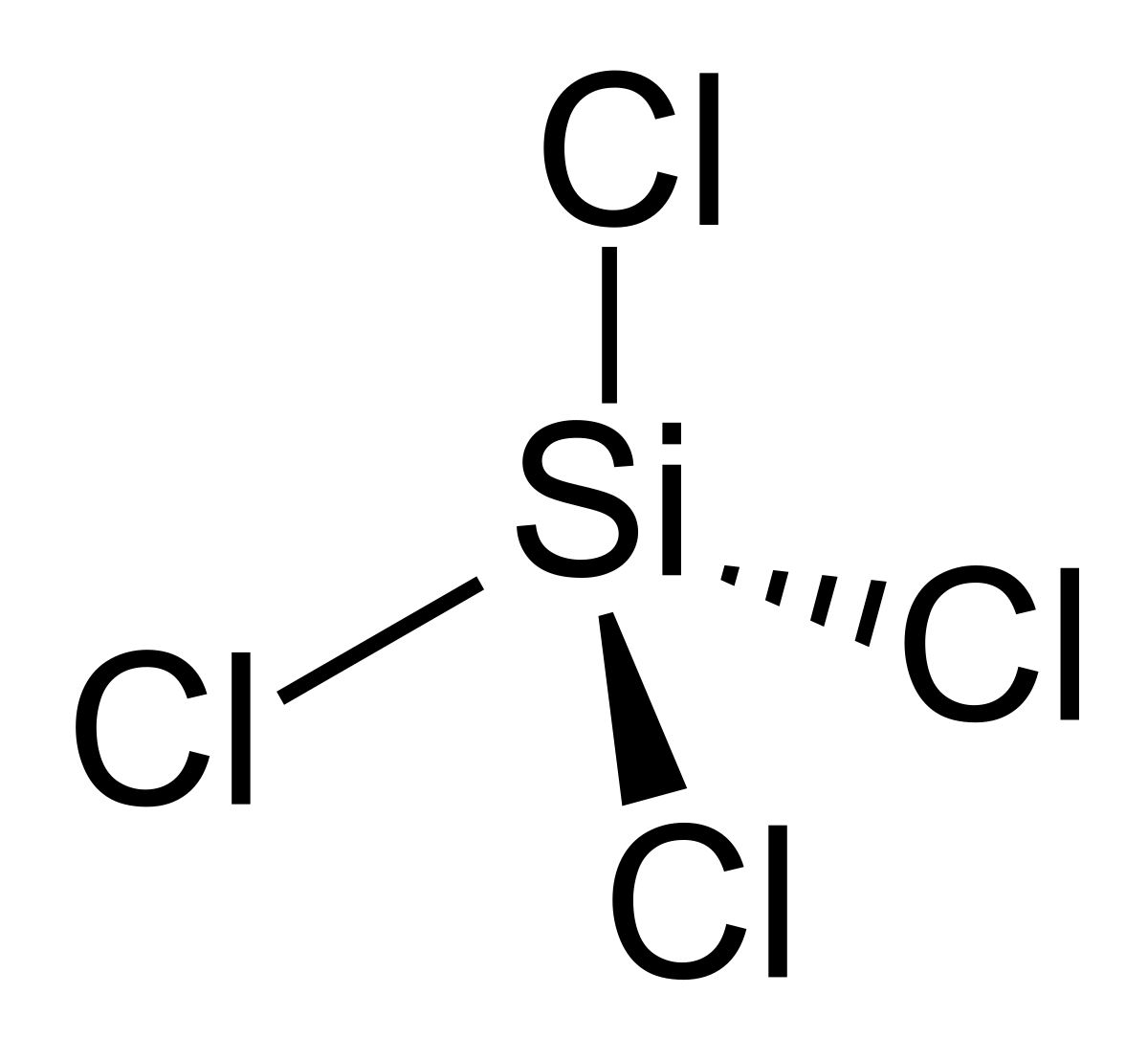
Le tétrachlorure de silicium est un composé chimique, de formule SiCl4. C'est un liquide incolore, relativement volatile.
Fabrication
Le tétrachlorure de silicium est préparé à partir de silicium et de dichlore:
Lors du traitment du dioxyde de silicium on utilise du chlorure d'hydrogène, celui-ci peut aussi être utilisé dans la synthèse du tétrachlorure de silicium:
Réactivité
Le tétrachlorure de silicium est un composé très réactif. En particulier il réagit violemment avec l'eau (contrairement au tétrachlorure de carbone)