Indole - Définition
La liste des auteurs de cet article est disponible ici.
Réactions chimiques mettant en jeu l'Indole
Caractère basique du doublet de l'azote
Bien que l'atome d'azote possède un doublet libre (deux électrons ne participant pas aux liaisons chimiques), l'indole est nettement moins basique que les amines ou que l'aniline. En effet, ce doublet d'électron est délocalisé et participe à l'aromaticité du système. La forme basique (l'indole) est donc nettement plus stable que la forme acide (protonée) pour laquelle l'aromaticité est perdue. La forme protonée possède une constante d'acidité pKa=-3,6. Il faut donc utiliser un acide fort (comme l'acide chlorhydrique), pour protoner une fraction significative d'indole.
Substitution électrophile aromatique
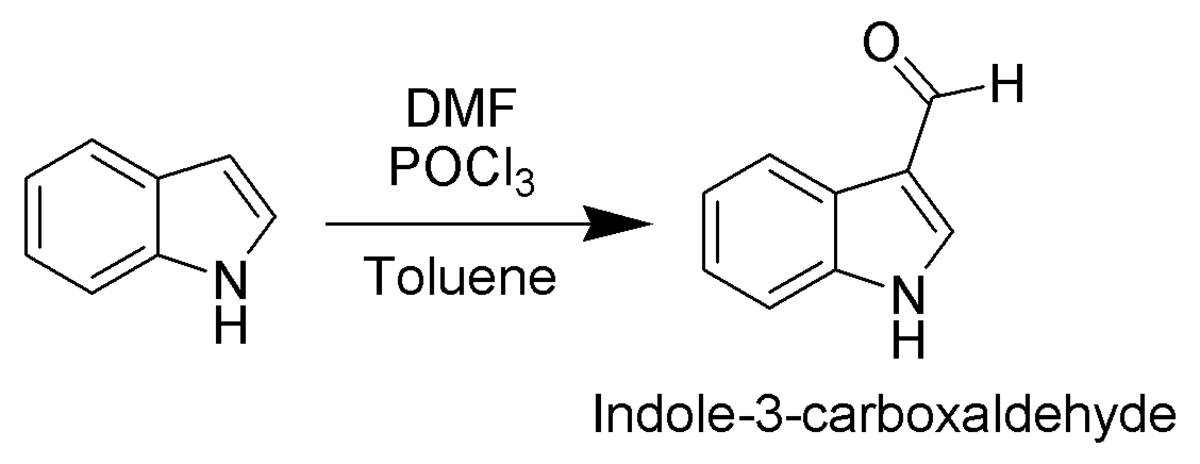
Du fait de son caractère aromatique, l'indole peut subir une substitution électrophile aromatique (substitution d'un atome d'hydrogène par un groupement électrophile. La position la plus réactive vis à vis de la substitution électrophile aromatique est la position C-3 (qui est environ 1000 fois plus réactive que celles situées sur le cycle benzénique). Par exemple, lors d'une formylation de Vilsmeier-Haack effectuée à la température ambiante, seule la position C-3 est substituée (voir schéma).
Les positions situées sur le cycle pyrrole étant plus réactives, les substitutions électrophiles aromatiques du cycle benzénique ne peuvent avoir lieu que lorsque les positions N-1, C-2 et C-3 ont subi une substitution.
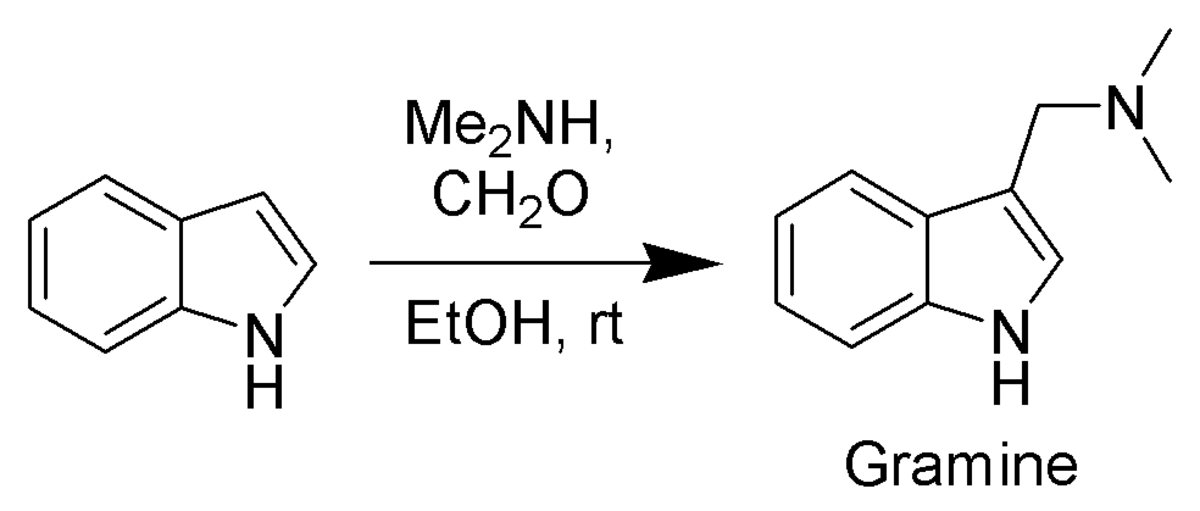
Parmi les composés obtenus par ce type de réactions on peut citer la gramine, un intermédiaire de synthèse important, fabriqué à partir d'indole, de diméthylamine et de formaldéhyde par la réaction de Mannich.
Caractère acide de l'atome d'hydrogène lié à l'azote
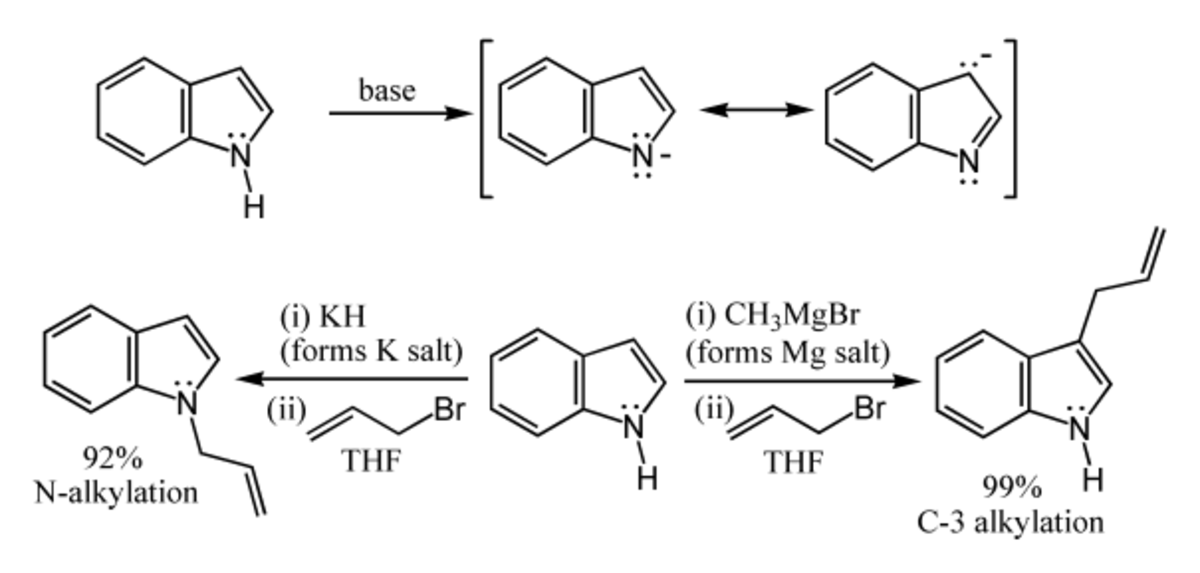
L'atome d'hydrogène porté par l'azote possède un faible caractère acide, avec une constante d'acidité pKa=21 dans le DMSO. La déprotonation de l'atome d'azote nécessite donc l'utilisation d'une base très forte comme l'hydrure de sodium ou le butyllithium, et un milieu totalement anhydre. Les sels résultant de la déprotonation peuvent réagir de deux manières. Les sels très ioniques comme les sels de sodium ou de potassium réagissent préférentiellement par une attaque électrophile sur l'atome d'azote (voie de gauche sur le schéma). À l'inverse, les sels plus covalents, notamment les organo-magnésiens (réactif de Grignard) et les complexes à base de zinc, réagissent préférentiellement par l'intermédiaire du carbone C-3 (voie de droite sur la schéma). De même, le solvant utilisé influe sur la réaction : les solvants polaires et aprotiques comme le DMF ou le DMSO favorisent une réaction par l'atome d'azote, tandis que les solvants apolaires comme le toluène favorisent une réaction par le carbone C-3.
Acidité du carbone, lithiation de la position 2
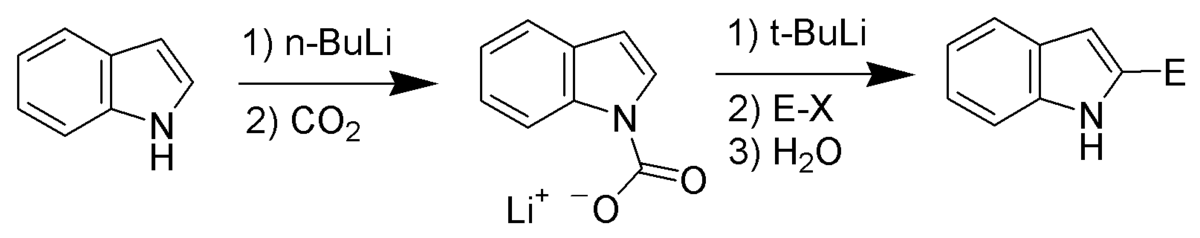
En termes d'acidité, l'atome d'hydrogène le plus acide après celui lié à l'atome d'azote est celui lié à l'atome de carbone en position 2. À condition d'effectuer en premier lieu une protection de la fonction azotée, il est donc possible de déprotoner le carbone en position 2, en utilisant par exemple du butyllithium ou du diisopropylamide lithium (LDA). Le carbanion résultant est un nucléophile très puissant, qui peut donc réagir avec des composés électrophiles. (exemple :
Oxydation de l'indole
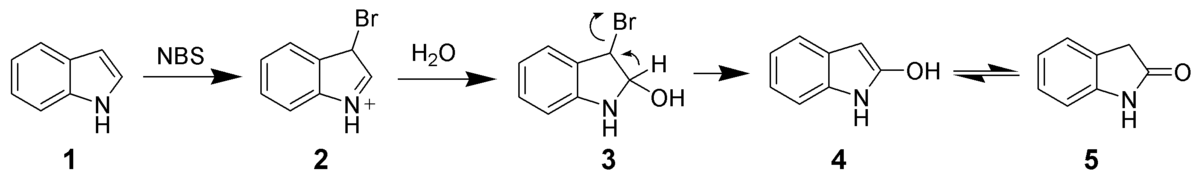
L'indole est un composé riche en électrons (10 électrons délocalisés sur les cycles) qui peut être facilement oxydé. Par exemple, le N-Bromosuccinimide permet d'oxyder l'indole (1) de manière sélective pour former l'oxindole (4 en équilibre avec 5).
Cycloadditions
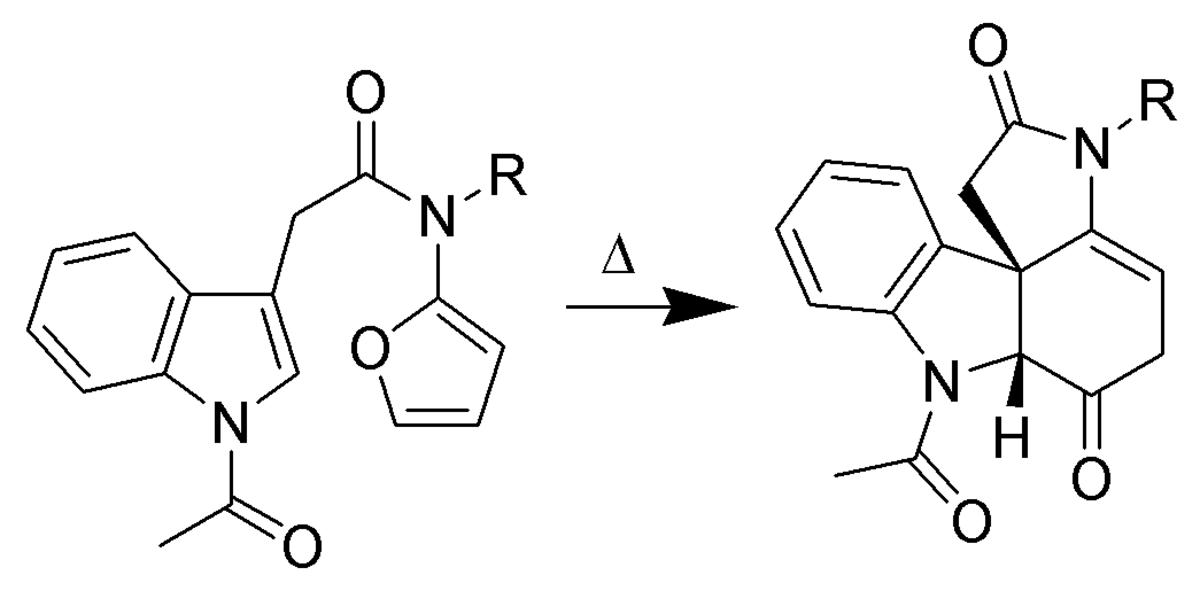
Les liaisons π portées par les atomes de carbone en positions C-2 et C-3 peuvent réagir dans des réactions de type cycloaddition (Réaction de Diels-Alder). Les réactions intermoléculaires ne sont pas favorables. En revanche, les réactions intramoléculaires (utilisant des dérivés substitués de l'indole) permettent d'obtenir de bons rendements. Dans l'exemple présenté ci-dessous, l'indole est le diénophile et le 2-aminofurane est le diène.