Substitution électrophile aromatique - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
La substitution électrophile aromatique (ou SEA, voire SEAr) est une réaction organique au cours de laquelle un atome, en règle générale d'hydrogène, ou un groupe d'atome, fixé à un cycle aromatique est substitué par un groupement électrophile. Cette réaction, la principale dans le groupe des substitutions électrophiles, est très importante en chimie organique, tant dans l'industrie qu'en laboratoire. Elle permet de préparer des composés aromatiques substitués par une grande variété de groupements fonctionnels suivant le bilan :
-
- ArH + EX → ArE + HX
avec Ar un composé aromatique et E un groupement électrophile.
Mécanisme général de la réaction
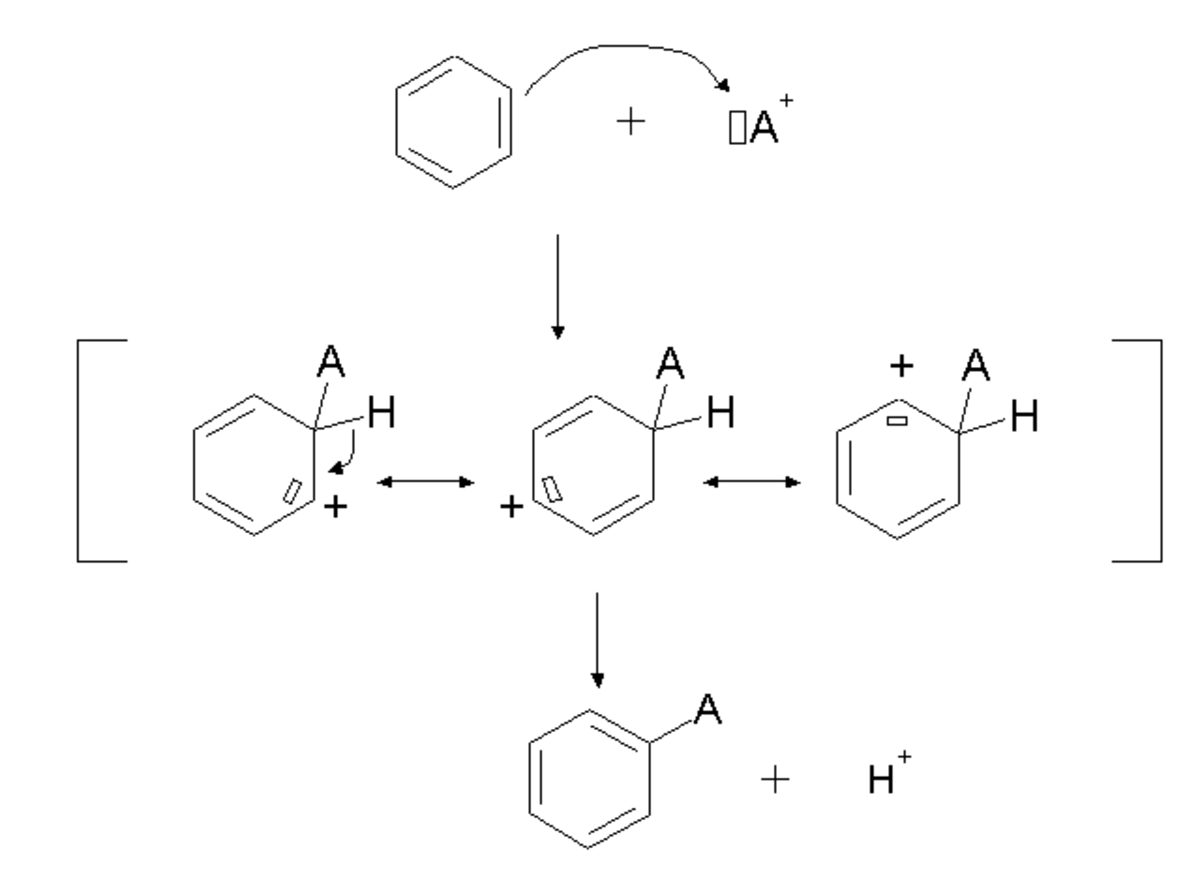
La première étape du mécanisme est une addition au cours de laquelle le composé électrophile A+ réagit avec un doublet électronique du cycle aromatique. Cette étape nécessite généralement une catalyse par un acide de Lewis. Cette addition conduit à la formation d'un carbocation cyclohexadiénil connu sous le nom d’intermédiaire de Wheland (ou complexe σ, ou encore ion arénium). Ce carbocation est instable, puisqu'il correspond à la fois à la présence d'une charge sur la molécule et à une perte d'aromaticité. Il est néanmoins stabilisé par mésomérie : la charge est en réalité délocalisée sur plusieurs atomes du cycle aromatique.
Au cours de la seconde étape, un atome d'hydrogène lié au cycle ayant subi l'addition électrophile part en tant qu'ion H+. L'électron qui était utilisé pour la liaison C-H permet alors au système de retrouver son aromaticité.
Autres substitutions
Réaction de Kolbe-Schmitt
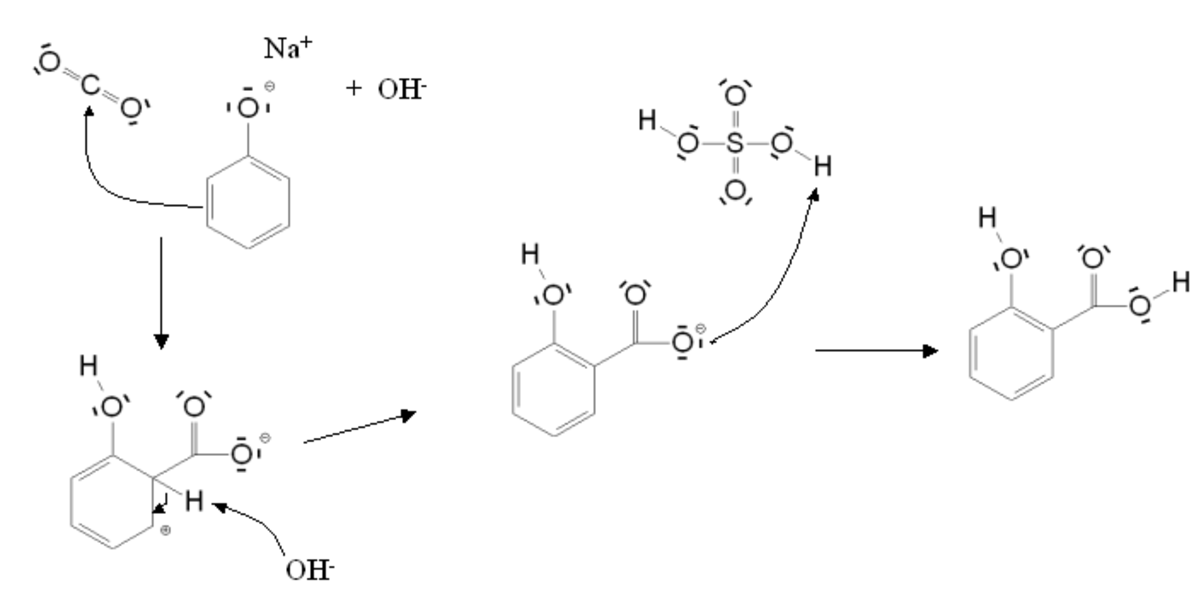
La réaction de Kolbe-Schmitt (ou procédé de Kolbe) est une réaction de carboxylation mise au point par A. Kolbe et R. Schmitt. Au cours de cette substitution électrophile aromatique, du phénolate de sodium (sel de phénol) est chauffé à 125 °C en présence de dioxyde de carbone sous une pression de 100 atm, puis traité par de l'acide sulfurique. Le bilan de la réaction est le suivant :
-
- C6H5OH + NaOH + H2SO4 → C6H4OHCOOH + HSO4-
Au cours de la première étape (pas montrée sur le schéma), le phénol réagit avec de la soude pour former le phénolate de sodium et des ions OH-. Le phénolate réagit ensuite avec le dioxyde de carbone par substitution électrophile aromatique, le centre électrophile étant ici l'atome de carbone du CO2. Les ions OH- formés au cours de la première étape assistent la restauration de l'aromaticité. Le composé obtenu étant la base conjuguée de l'acide carboxylique, la dernière étape consiste en une réaction acide-base avec l'acide sulfurique.
Le produit obtenu au cours de cette réaction est un hydroxy-acide aromatique (ici l'acide salicylique, précurseur de l'aspirine).
Principales substitutions électrophiles aromatiques
Ce chapitre détaille les principales substitutions électrophiles aromatiques utilisées dans l'industrie et en laboratoire. Pour chacune d'entre elles, le mécanisme de la réaction est donné dans le cas particulier du benzène. Ce mécanisme est similaire pour d'autres types de composés aromatiques, aux conditions opératoires (température, solvant...) près.
Nitration aromatique
La nitration aromatique est une substitution électrophile aromatique particulière au cours de laquelle un atome d'hydrogène lié à un atome de carbone du cycle aromatique est substitué par un groupement nitro -NO2 pour former du nitrobenzène. L'électrophile utilisé pour la substitution est NO2+ (ion nitronium), produit in-situ.
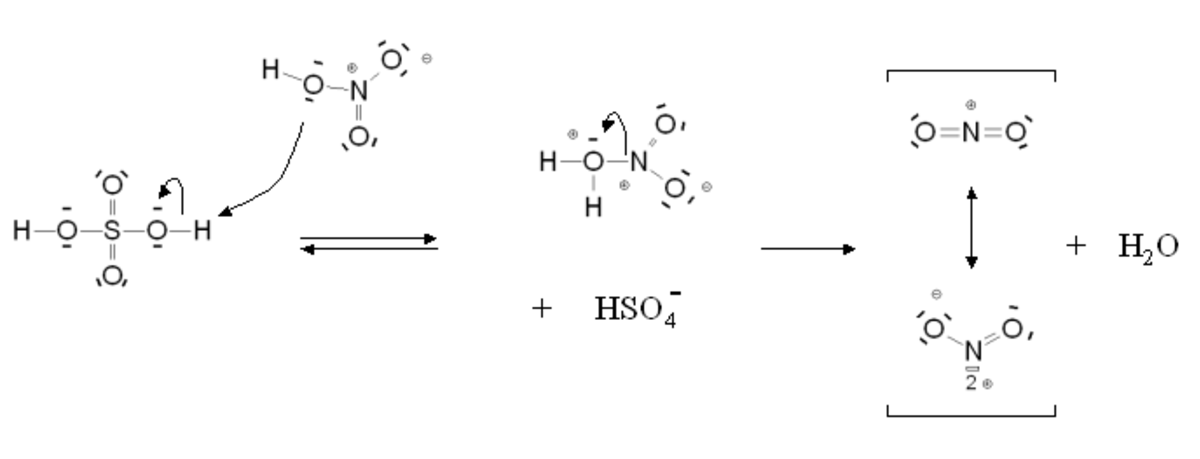
Dans la pratique pour effectuer la substitution, le benzène est chauffé à 50 °C environ dans un mélange d'acide sulfurique et d'acide nitrique. Le schéma réactionnel est le suivant :
-
- (1) 2H2SO4 + HNO3 → 2HSO4- + NO2+ + H3O+
-
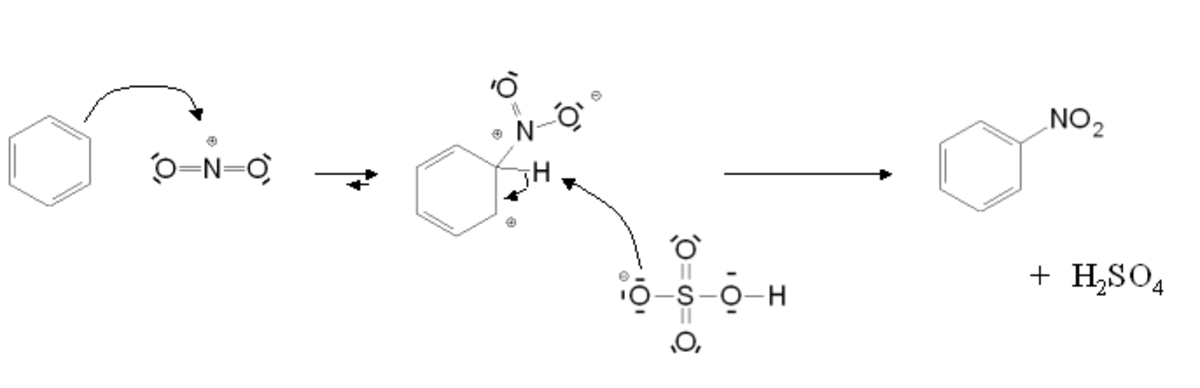
- (2) C6H6 + NO2+ → C6H5NO2 + H+
-
- (3) H+ + H3O+ + 2HSO4- → H3O+ + H2SO4 + HSO4-
L'acide sulfurique joue en quelque sorte le rôle de catalyseur pour la formation de l'ion nitronium. La réaction est également possible avec l'acide nitrique seul, mais elle est alors beaucoup plus lente. Parmi les autres réactifs utilisables pour la nitration aromatique, on peut citer le tétrafluoroborate de nitronium, qui est un sel de nitronium obtenu à partir de fluorure d'hydrogène, d'acide nitrique et de trifluorure de bore.
Si la réaction est catalysée en présence d'acide sulfurique, l'étape cinétiquement déterminante est la nitration du cycle benzénique pour former l'intermédiaire de Wheland. En présence d'acide nitrique seul, il s'agit de la formation de l'ion nitronium.
Le nitrobenzène formé au cours de cette réaction peut notamment être utilisé pour fabriquer de l'aniline par réduction :
-
- C6H5NO2 + 3H2 → C6H5NH2
Sulfonation aromatique
La sulfonation aromatique est une substitution électrophile aromatique particulière au cours de laquelle un atome d'hydrogène lié à un atome de carbone du cycle aromatique est substitué par un groupement acide sulfonique. Dans le cas du benzène, la réaction permet de former de l'acide benzènesulfonique.
La substitution peut être réalisée de deux manières :
- Le benzène est maintenu à 25 °C dans un oléum, solution de SO3 dans l'acide sulfurique (H2SO4) ou mélange de SO3 et d'eau (avec SO3 majoritaire). Le bilan de la réaction est alors :
-
- C6H6 + SO3 → C6H5SO3H
- Le benzène est chauffé dans l'acide sulfurique concentré. SO3 est alors formé in-situ par réaction de l'acide sulfurique sur lui-même. Le bilan de la réaction est alors :
-
- C6H6 + 2 H2SO4 → C6H5SO3H
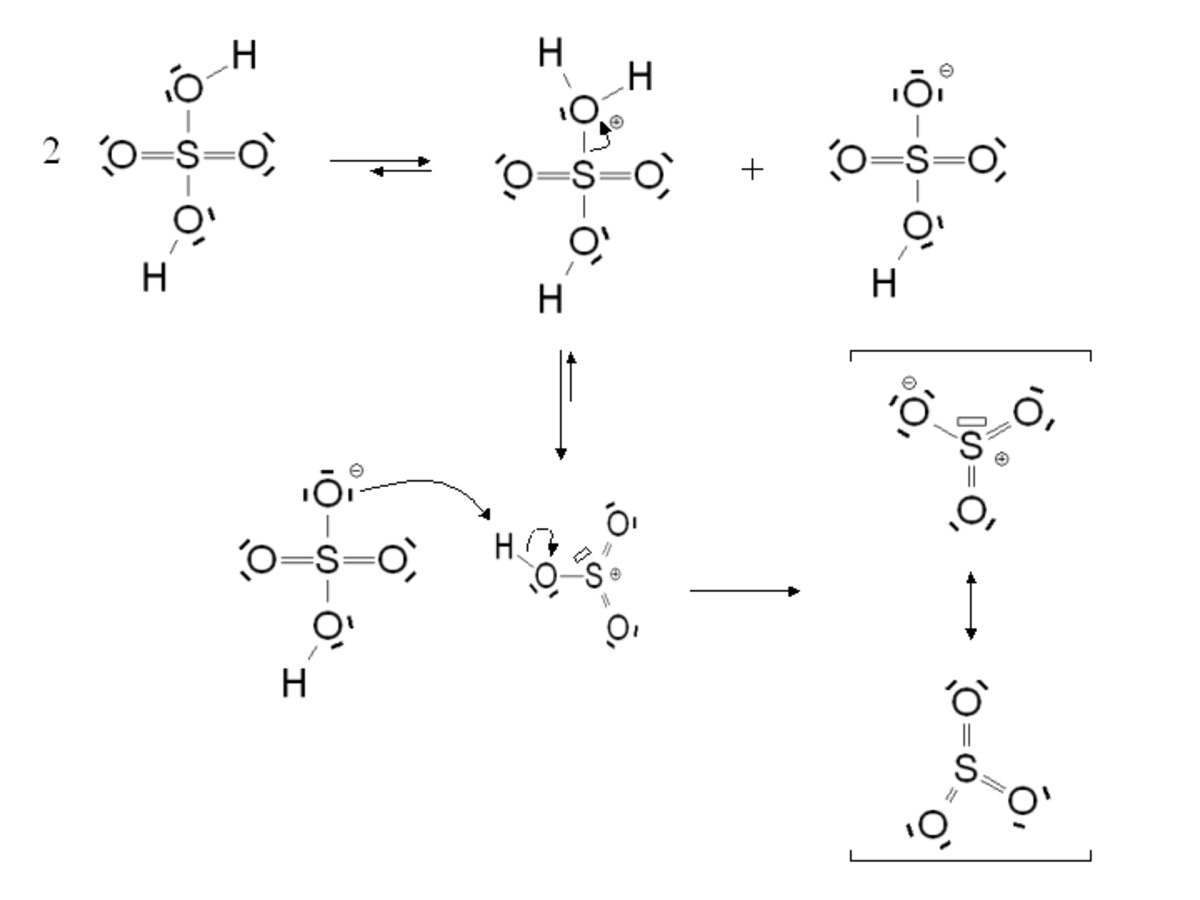
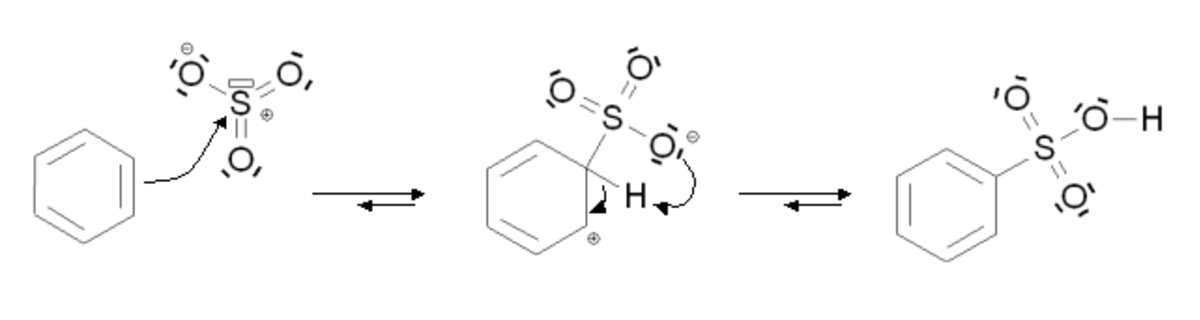
Dans les deux cas, le mécanisme de la réaction est le suivant :
Pour la sulfonation, l'élimination de l'atome d'hydrogène se fait par une réaction intramoléculaire.
Cette réaction ne possède pas d'étape cinétiquement déterminante.
Il s'agit d'une réaction réversible : il est possible d'éliminer le groupement acide sulfonique et de régénérer le benzène en chauffant l'acide benzènesulfonique dans une solution diluée d'acide sulfurique dans de l'eau surchauffée. Le bilan est alors :
-
- C6H5SO3H + H2O(vapeur) → C6H6 + HSO4- + H3O+
L'acide benzènesulfonique formé au cours de cette réaction est un intermédiaire de synthèse important dans l'industrie, utilisé dans la fabrication de colorants et de produits pharmaceutiques. Par ailleurs, il est possible de le réduire en présence de soude fondue pour former du phénol.
Halogénation aromatique
L’halogénation aromatique est une substitution électrophile aromatique au cours de laquelle un atome d'hydrogène lié à un atome de carbone du cycle aromatique est substitué par un élément halogène suivant le bilan suivant :
-
- C6H6 + X2 → C6H5X + HX
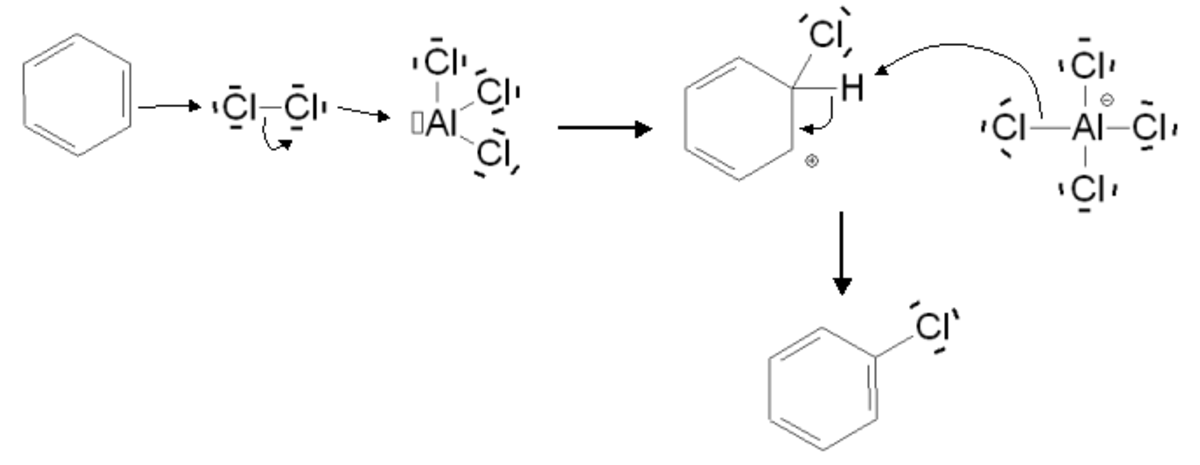
La réaction n'est pas spontanée, mais nécessite la présence d'un catalyseur de type acide de Lewis. Elle s'effectue donc en milieu anhydre. Elle est possible sans catalyseur (mais est alors lente) dans le cas de cycles activés, comme par exemple le phénol. L'halogénation aromatique permet de substituer un atome d'hydrogène par un atome de chlore, de brome ou d'iode. En revanche, elle n'est pas possible avec le fluor. Celui-ci est en effet un oxydant puissant qui entraîne une dégradation du composé aromatique. Le mécanisme de la réaction est le suivant (exemple dans le cas d'une chloration) :
Au cours de la première étape du mécanisme, l'acide de Lewis utilisé comme catalyseur forme un complexe avec le dichlore, ce qui rend la liaison Cl-Cl polarisée. L'un des deux atomes de chlore devient donc électrophile, et peut subir l'attaque nucléophile du cycle aromatique, conduisant ainsi à la formation de l'intermédiaire de Wheland. L'anion formé contribue ensuite dans la deuxième étape à l'élimination de l'atome d'hydrogène et à la restauration de l'aromaticité.
Le catalyseur utilisé est généralement constitué du même élément halogène que celui agissant dans la substitution. Les acides de Lewis les plus couramment employées sont donc ZnCl2, AlCl3 et FeCl3 dans le cas de la chloration, et FeBr3 dans le cas de la bromation. Dans le cas de l'iode, le mécanisme de la réaction est légèrement différent. En effet, le diiode I2 est trop peu réactif. Il doit d'abord réagir avec un agent d'oxydation (par exemple l'acide nitrique) pour former l'ion I+, électrophile, qui interviendra dans l'iodation.
Les halogènes sont des éléments faiblement désactivant pour le cycle aromatique. En conséquence, si la réaction est catalysée et que l'halogène est présent en excès, il pourra se produire des polysubstitutions.
Réactions de Friedel-Crafts
Les réactions de Friedel-Crafts sont des substitutions électrophiles aromatiques particulières au cours desquelles un cycle aromatique est alkylé (substitution d'un atome d'hydrogène par un groupement alkyle) ou acylé (substitution d'un atome d'hydrogène par un groupement acyle).
- Article détaillé : Réaction de Friedel-Crafts.
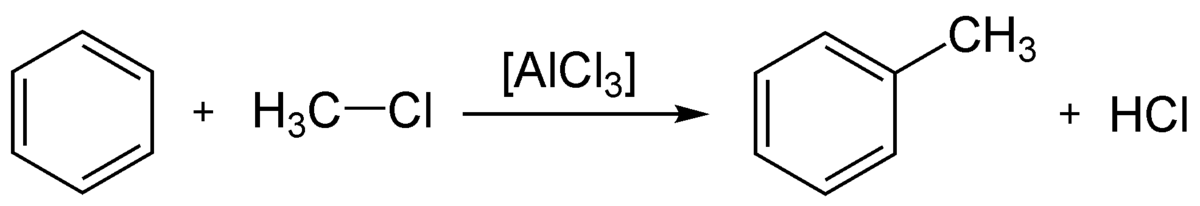
Alkylation
L'alkylation de Friedel-Crafts est une réaction d'alkylation d'un composé aromatique. Cette réaction nécessite une catalyse par un acide de Lewis.
Acylation
L'acylation de Friedel-Crafts est une réaction d'acylation d'un composé aromatique. Comme l'alkylation, elle nécessite une catalyse par un acide de Lewis. Les principaux catalyseurs utilisés sont le chlorure d'aluminium et le bromure d'aluminium. Il y a en général plus besoin de catalyseur que les quantités stoechiométriques, car il complexe avec le produit formé, d'où la nécessité d'une hydrolyse après la réaction pour détruire le complexe.