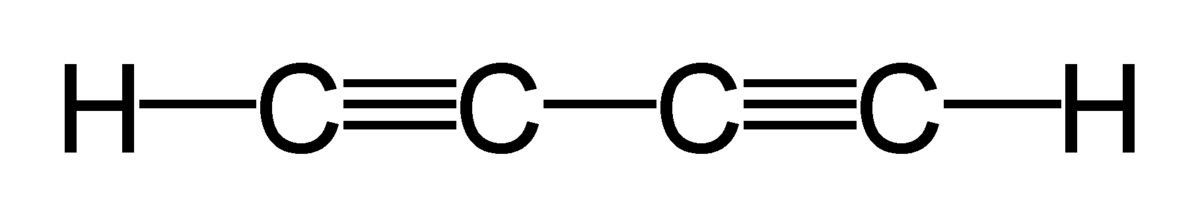Butadiyne - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Buta-1,3-diyne | ||
|---|---|---|
| ||
| Général | ||
| Nom IUPAC | ||
| Synonymes | diacétylène | |
| No CAS | ||
| PubChem | ||
| SMILES | ||
| InChI | ||
| Apparence | Gaz incolore | |
| Propriétés chimiques | ||
| Formule brute | C4H2 | |
| Masse molaire | 50,0587 ± 0,0033 g·mol-1 | |
| Propriétés physiques | ||
| T° fusion | −36 °C | |
| T° ébullition | 10,3 °C | |
| Précautions | ||
| | ||
| ||
| Phrases R : 11, 19, | ||
| | ||
Le butadiyne aussi appelé diacétylène ou diéthyne, de formule brute C4H2, est un hydrocarbure aliphatique très insaturé de la famille des alcynes qui contient deux liaisons carbone-carbone simples et deux triples liaisons conjuguées. Il est la premier composé de la série des polyynes.
Propriétés
Le butadiyne est extrêmement inflammable et brûle dans l'air en dégageant une fumée noire, contenant dioxyde de carbone et eau. En raison de ses triples liasons, le butadidyne est très réactif; il peut être utilisé pour des additions électrophiles, des réactions de polymérisation (polydiacétylène) et pour des réaction de Diels-Alder.
Présence dans la nature
Le butadiyne a été identifié dans l'atmosphère de Titan (le plus grand satellite de Saturne) et dans la nébuleuse protoplanétaire CRL 618(en) par ses modes de vibrations caractéristiques. Dans l'atmosphère de Titan, cette molécule est presque entièrement formée par réaction entre l'éthyne (acétylène) et le radical éthynyl HC≡C∙ qui est produit par photolyse de l'éthyne. Ce radical peut en fait réagir efficacement avec la triple liaison de l'éthyne même à très basses températures.
Synthèse
Le butadiyne peut être obtenu par dimérisation de l'éthyne (couplage oxydatif). On appelle aussi cette réaction couplage de Glaser.