Chloronaphtalène - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Tétrachloronaphthalène | |||
|---|---|---|---|
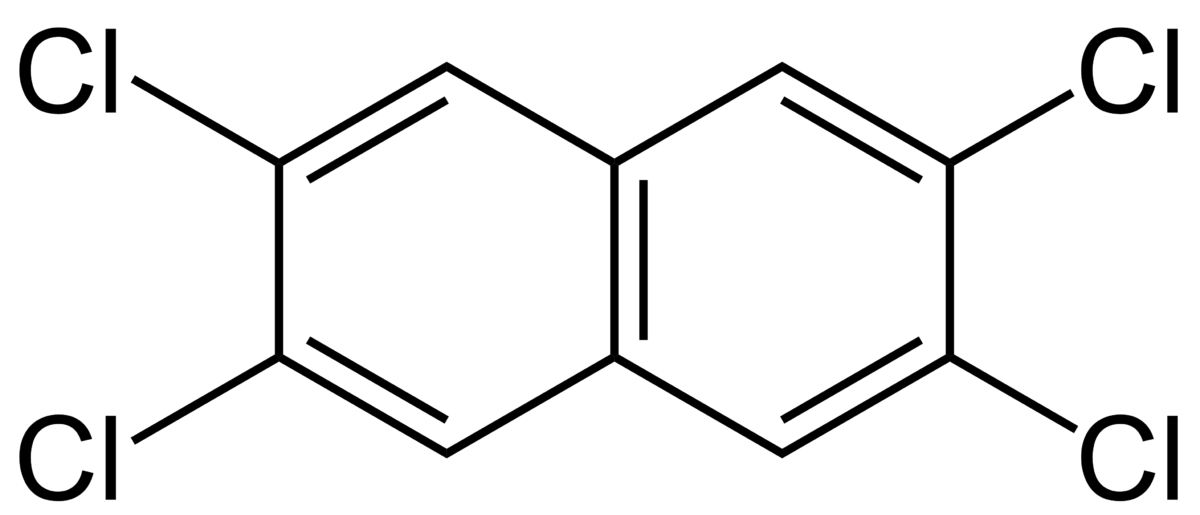
| |||
| Général | |||
| Nom IUPAC | |||
| No CAS | |||
| No EINECS | |||
| SMILES | |||
| Apparence | cristaux incolores à jaune pâle, d'odeur caractéristique. | ||
| Propriétés chimiques | |||
| Formule brute | C10H10-nClN | ||
| Masse molaire | 265,951 ± 0,016 g·mol-1 | ||
| Propriétés physiques | |||
| T° fusion | 182 °C | ||
| T° ébullition | 312 à 360 °C | ||
| Solubilité | dans l'eau : nulle | ||
| Masse volumique | 1,6 g·cm-3 | ||
| Point d’éclair | 210 °C (coupelle ouverte) | ||
| Pression de vapeur saturante | à 25 °C : | ||
| Précautions | |||
| | |||
| |||
| Phrases R : 21/22, 36/38, 50/53, | |||
| Phrases S : 35, 60, 61, | |||
| | |||
| Produit non contrôlé | |||
| | |||
Les Chloronaphtalènes (PCN pour Polychlorinated naphthalene) sont des produits fabriqués par réaction chimique entre le chlore le naphtalène, se présentant sou l’aspect d’un solide d’odeur douceatre et âcre qui est fabriqué à partir du charbon ou du pétrole, et souvent utilisé pour le traitement anti-mite. La formule chimique générique est la suivante : C10H10-nClN
Utilisations
Les chloronaphtalènes commerciaux sont des mélanges de 75 Isomères auxquels il faut ajouter les sous-produits. Ils sont souvent caractérisés par leur fraction en chlore total. Lorsque la proportion de chlore augmente, les PCN deviennent de plus en plus pâteux voire solides à température ambiante. Certains chloronaphtalènes ont été utilisés comme revêtements isolants pour câbles électriques. D'autres ont été employés pour le traitement du bois, comme additifs pour le caoutchouc et les plastiques, comme diélectriques pour les condensateurs et comme lubrifiants.
Effets sur la santé
Après environ vingt ans de production commerciale, les risques pour la santé ont commencé à être rapportés chez les travailleurs exposés aux chloronaphtalènes : éruptions cutanées sévères et atteintes hépatiques qui ont conduit à des décès parmi les travailleurs.Une conférence sur les dangers a été organisée à la Harvard School of Public Health en 1937, et plusieurs autres publications traitant des dangers des chloronaphtalènes ont été faites avant 1940. Les choronaphtalènes contenant trois atomes de chlore ou davantage par molécule ont habituellement été considérés comme plus dangereuses que les molécules moins chlorées, mais lorsqu’on approche du nombre maximum de huit atomes, les risques semblent diminuer.
Il y a eu environ quarante ans de décalage, entre la divulgation des risques des chloronaphtalènes et la mise en œuvre d’une réglementation gouvernementale. Aux Etats-Unis, l'exposition aux chloronaphtalènes a été drastiquement réduite après 1976, à la suite de la promulgation du Toxic Substances Control Act. Les grands fabricants d'équipements ont interdit l’utilisation des chloronaphtalènes dans leurs produits, et les principaux producteurs ont abandonné leur activité. En 1983 la production mondiale de chloronaphtalènes était presque arrêtée à l'exception de petites quantités utilisées pour l'expérimentation et la recherche. Jusqu'à ces dernières années Du Pont de Nemours produisait un caoutchouc synthétique, le Néoprène FB, fabriqué en Irlande du Nord à partir de pentachloronaphthalene. Aujourd'hui, les chloronaphtalènes sont commercialisés par quelques entreprises seulement, dont Ukrgeochem de Simferopol, en Ukraine.
Alors que certains cloronaphtalènes peuvent être décomposés par la lumière du soleil et, à un rythme très lent, par certains micro-organismes, de nombreux chloronaphtalènes persistent dans l'environnement. Après plus de 80 années d'utilisation et une production totale de plusieurs centaines de millions de kilogrammes, les résidus des chloronaphtalènes ont été largement disséminés. Une exposition aiguë provoque la chloracné. L'exposition chronique augmente le risque de maladie du foie. Une augmentation des risques de survenue d’un cancer a été suspectée, mais à ce jour non encore démontrée. Les préoccupations actuelles à propos des chloronaphtalènes concernent notamment leur libération comme sous-produits d'incinération des déchets.



















































