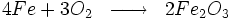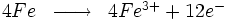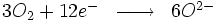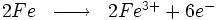Corrosion aqueuse - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
La corrosion désigne l'altération d'un objet manufacturé par l'environnement. Les exemples les plus connus sont les altérations chimiques des métaux dans l'eau — avec ou sans oxygène — telles la rouille du fer et de l'acier, ou la formation de vert-de-gris sur le cuivre et ses alliages (bronze, laiton). Ces altérations chimiques sont regroupées sous le terme de corrosion aqueuse. Elles sont dues à des effets de plusieurs sortes : dissolution des métaux dans l'eau, apparition de piles électrochimiques, existence de gradients de concentration, aération différentielle ou piqûration. Globalement, la corrosion aqueuse est un phénomène dont l'impact économique est très important, nécessitant une grande variété de moyens de protections des métaux.
Corrosion généralisée : la dissolution des métaux
La corrosion des métaux consiste essentiellement en leur oxydation, qui est un « retour à l'état naturel. » Cependant, l'oxydation n'est pas nécessairement la combinaison d'un élément avec de l'oxygène. D'une manière plus générale, il s'agit d'une réaction chimique au cours de laquelle un composé considéré cède des électrons.
Par exemple, le fer s'oxyde en présence du dioxygène de l'air pour former de l'hématite (Fe203) :
peut s'écrire
L'hématite peut donc être décrite comme un cristal ionique (Fe3+2, O2-3), ce qui n'est pas tout à fait exact, mais donne une bonne approche du phénomène d'oxydation. Au cours de la réaction, le fer perd des électrons : on dit qu'il est oxydé. L'oxygène gagne de ce fait des électrons : on dit qu'il est réduit.
La corrosion des métaux en milieu aqueux résulte de l'oxydation du métal, mais pas nécessairement par le dioxygène de l'air qui est dissous dans l'eau : l'oxydation peut également se produire avec d'autres espèces chimiques, notamment des ions.
Lorsque l'on plonge du fer dans une solution acide (pH < 7), le fer se dissout avec un dégagement de dihydrogène. En fait, il s'agit là d'une version accélérée de la corrosion en milieu aqueux :
Les ions Fe3+ passent alors en solution, et peuvent éventuellement se combiner avec l'oxygène dissout dans l'eau et former de l'hématite. Cette dissolution est favorisée en milieu acide, mais elle est aussi possible dans une solution aqueuse neutre (pH = 7) ou basique (pH > 7) puisque l'eau contient de toutes manières des ions H3O+.
Cette dissolution dans l'eau par oxydation s'appelle corrosion généralisée.
L'oxydation peut aussi se produire sans dissolution. Par exemple, l'oxygène réagit avec l'aluminium pour former une couche d'oxyde (alumine Al2O3) ; si cette couche est compacte et adhérente, elle protège la pièce. On dit que le métal est passivé. Une pièce passivée continue à se dissoudre, mais à une vitesse extrêmement lente, la couche d'oxyde dite « passive » fait un écran. La pièce est donc considérée comme totalement protégée contre la corrosion.
La stabilité du fer dans l'eau dépend :
- du pH, qui détermine la concentration d'ions H3O+ dans l'eau ;
- du potentiel électrique de la pièce en fer par rapport à la solution, qui détermine la capacité des électrons à quitter le fer.
On peut ainsi tracer un diagramme potentiel-pH (E, pH), en indiquant les zones de stabilité du fer (Fe), les zones de stabilité de l'ion Fe2+ (ou « ion fer II »), les zones de stabilité de l'ion Fe3+ (ou « ion fer III ») et les zones de passivation. Il s'agit donc d'une sorte de « carte », les zones délimitées par des frontières indiquant les couples de valeurs (E, pH) pour lesquelles une espèce est stable. Ce diagramme porte le nom de diagramme de Pourbaix, et peut être tracé pour tous les métaux.
Pour savoir si un matériau est adapté à un milieu, il suffit de regarder le diagramme de Pourbaix de ce matériau. Si le couple (E, pH) se situe dans une zone de stabilité, le matériau est protégé contre la corrosion généralisée.