Dioxygène - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Dioxygène | |||||
|---|---|---|---|---|---|
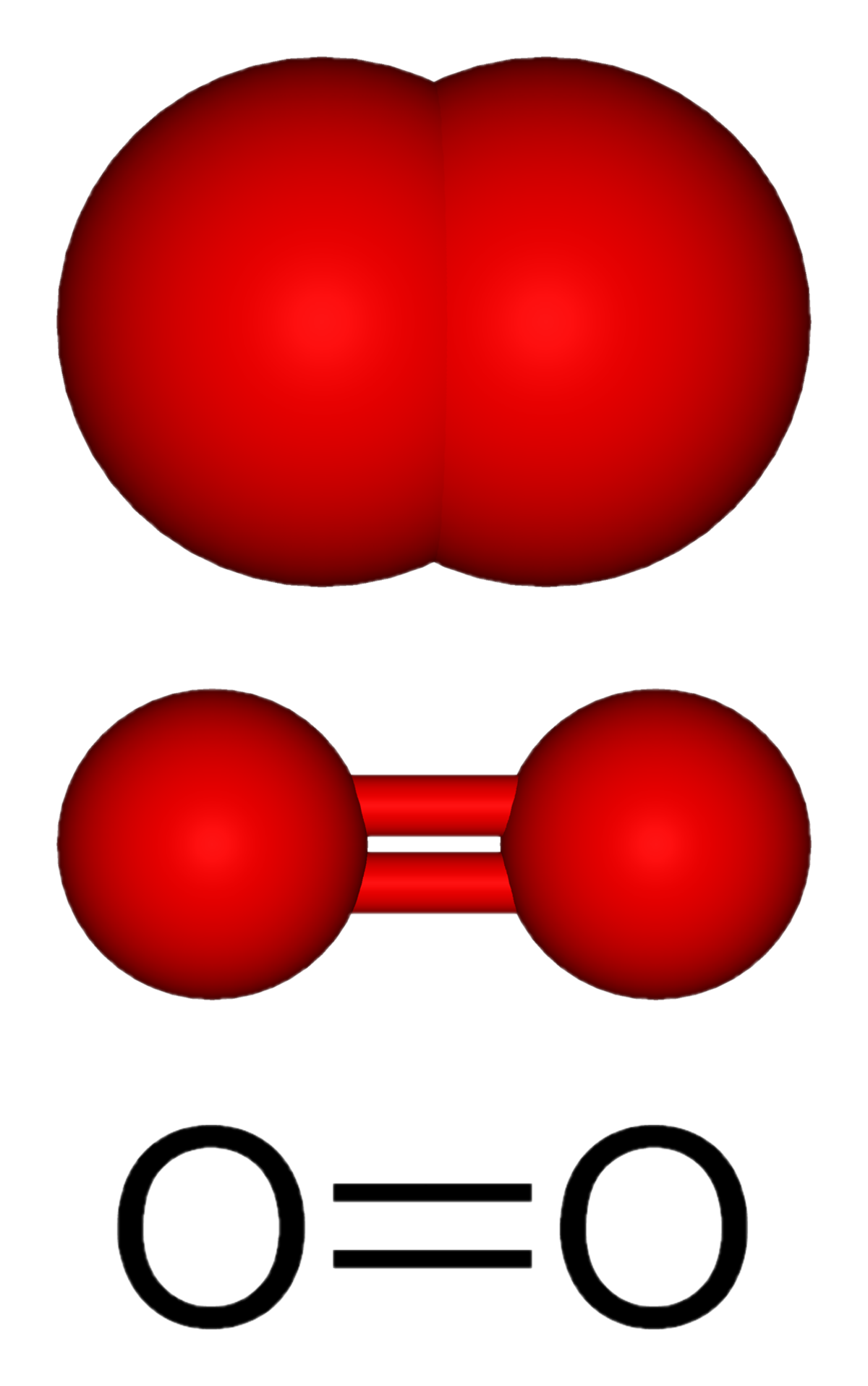
| |||||
| Général | |||||
| Nom IUPAC | |||||
| Synonymes | oxygène | ||||
| No CAS | |||||
| No EINECS | |||||
| PubChem | |||||
| No E | E948 | ||||
| SMILES | |||||
| InChI | |||||
| Apparence | gaz incolore à température ambiante, gaz liquéfié ou liquide extrêmement froid incolore à bleu | ||||
| Propriétés chimiques | |||||
| Formule brute | O2 | ||||
| Masse molaire | 31,9988 ± 0,0006 g·mol-1 | ||||
| Diamètre moléculaire | 0,292 nm | ||||
| Propriétés physiques | |||||
| T° fusion | -219 °C | ||||
| T° ébullition | -183 °C | ||||
| Solubilité | dans l'eau à 20 °C : 3,1 ml/100 ml, 14,6 mg·l-1 (eau à 0 °C) | ||||
| Masse volumique | |||||
| Pression de vapeur saturante | à -118 °C : 5 080 kPa | ||||
| Point critique | -118,67 °C 50,422 bar 0,6361 kg·l-1 | ||||
| Point triple | -218,7916 °C 0,00149 bar | ||||
| Thermochimie | |||||
| ΔH° | 213 kJ/kg | ||||
| ΔH° | 6,82 kJ·mol-1 (1 atm, -182,95 °C) | ||||
| Cp | |||||
| Propriétés électroniques | |||||
| 1re énergie d'ionisation | 12,0697 ± 0,0002 eV (gaz) | ||||
| Précautions | |||||
| | |||||
| |||||
| Phrases R : 8, | |||||
| Phrases S : 2, 17, | |||||
| | |||||
| |||||
| | |||||
|
0 3 0 OX | |||||
| | |||||


| |||||
| | |||||


Danger | |||||
| | |||||
Le dioxygène est une molécule composée de deux atomes d'oxygène, notée O2, qui est à l'état de gaz aux conditions normales de pression et de température.
Il a été découvert le 1er août 1774 par le chimiste anglais Joseph Priestley, et baptisé du nom d'« oxygène » par le chimiste français Antoine Lavoisier en 1778.
Il est également appelé « molécule d'oxygène », ou simplement « oxygène » dans le langage courant (à ne pas confondre avec l'élément chimique de même nom).
Il est incolore, inodore et insipide.
Il compose 20,95 % en volume et 23,2 % en masse de l'atmosphère terrestre. C'est un gaz indispensable à beaucoup de formes de vie, auxquelles il fournit l'oxygène nécessaire à la respiration des cellules. Il n'est en revanche pas indispensable à certaines bactéries dites anaérobies facultatives, et il est même mortel pour les bactéries anaérobies strictes.
Il participe au même titre que le dichlore à des réactions d'oxydo-réduction, essentiellement dans son cas la combustion et la corrosion.



















































