Dibenzofurane - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Dibenzofurane | |
|---|---|
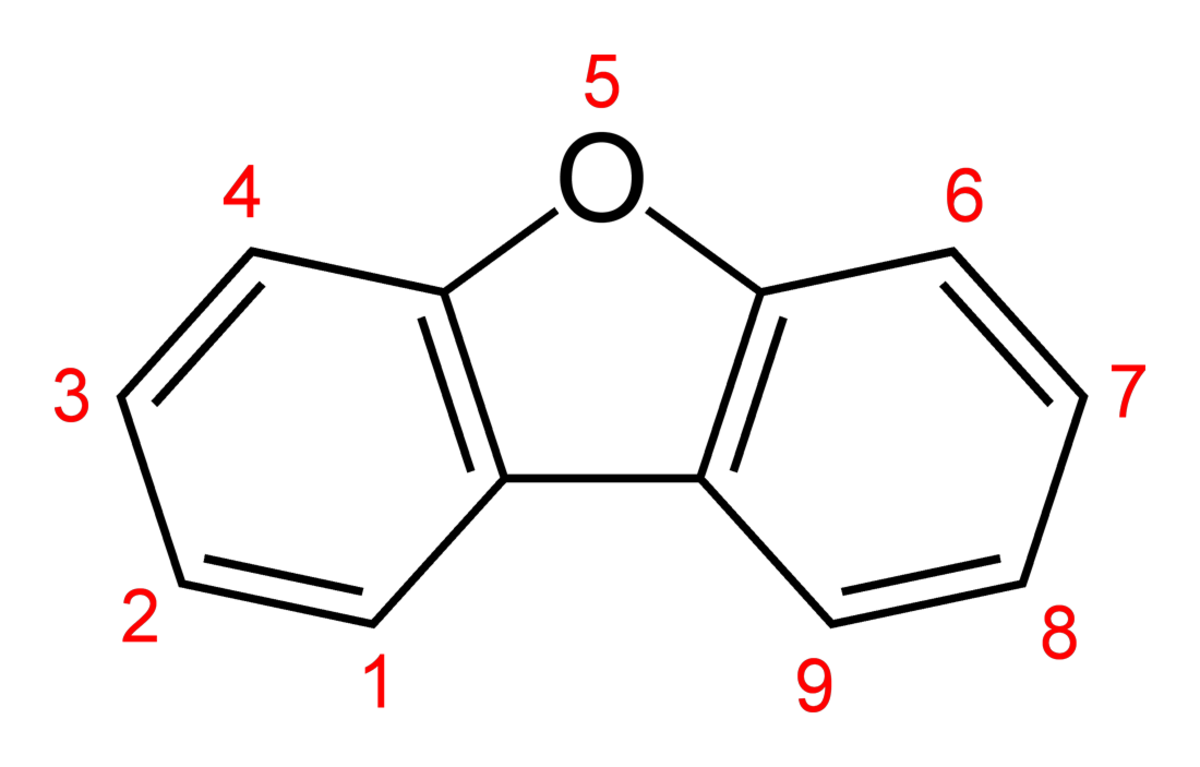
| |
| Général | |
| Nom IUPAC | |
| Synonymes | oxyde de diphénylène |
| No CAS | |
| No EINECS | |
| PubChem | |
| ChEBI | |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule brute | C12H8O |
| Masse molaire | 168,1913 ± 0,0105 g·mol-1 |
| Propriétés physiques | |
| T° fusion | 81,85 °C |
| T° ébullition | 285,05 °C |
| Solubilité | 3,1 mg·l-1 (eau,25 °C) |
| Masse volumique | 1,3 g·cm-3 |
| Point d’éclair | 148 °C |
| Point critique | 550,85 °C, 36,4 bar |
| Thermochimie | |
| S0 | 196,18 J·K-1·mol-1 |
| ΔH0 | 47,3 kJ·mol-1 |
| ΔH0 | -29,2 kJ·mol-1 |
| ΔH° | 18,6 kJ·mol-1 à 82,55 °C |
| Cp | 199,01 J·K-1·mol-1 (solide,25 °C) |
| PCI | -5 836,3 kJ·mol-1 (solide) |
| Écotoxicologie | |
| LogP | 4,12 |
| | |
Histoire
Ce composé fut synthétisé pour la première foie en 1866 par C. Lesimple à partir du phosphate de triphényle et de l'oxyde de calcium. Il fut caractérisé en 1871 par W. Hoffmeister et découvert comme étant un composant du goudron en 1901 par G. Kraemer et R. Weissgerber.
Production et synthèse
Il est extrait du goudron où il est présent à une concentration d'environ 1 % dans une fraction comprise allant de 270 à 290 °C qui contient environ 30 % de dibenzofurane. Une seconde distillation le séparant de l'acénaphtène et une cristallisation permettent d'obtenir un produit techniquement pur.
Il peut être synthétisé par déshydrogénation du phénol à 450 °C, par déshydrogénation oxydative du phénol et cyclisation du 2-cyclohexenylcyclohexanone ainsi formé, par cyclisation de diphényléther en présence de l'acétate de palladium ou encore par pyrolyse de l'anhydride phtalique en présence de furane. L'extraction du goudron couvrant les besoins, les synthèses n'ont pas d'applications industrielles.
Propriétés physico-chimiques
Le benzofurane est soluble dans le diéthyléther, le benzène, l'acide acétique, peu soluble dans l'éthanol et insoluble dans l'eau.
Utilisation
Pour sa résistance à la chaleur, il est utilisé comme fluide caloporteur. Il sert de précurseur à plusieurs additifs pour plastiques, pour des monomères, de parfums, de produits pharmaceutiques ou de sédatifs.

















































