Nicotinamide adénine dinucléotide - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Nicotinamide adénine dinucléotide | |
|---|---|
| Général | |
| Synonymes | NAD+ Coenzyme I |
| No CAS | |
| No EINECS | |
| DrugBank | |
| SMILES | |
| InChI | |
| Apparence | solide |
| Propriétés chimiques | |
| Formule brute | C21H27N7O14P2 |
| Masse molaire | 663,4251 ± 0,0243 g·mol-1 |
| Écotoxicologie | |
| DL | 4 333 mg·kg-1 (souris, i.p.) |
| | |
Le nicotinamide adénine dinucléotide, ou NAD, est un coenzyme d'oxydoréduction présent dans toutes les cellules vivantes. Le composé est un dinucléotide, puisqu'il est composé de deux nucléotides liés par leurs groupes phosphate. Un des nucléotides contient une adénine tandis que l'autre contient un nicotinamide. Dans le métabolisme, le NAD+ est impliqué dans les réactions redox en transportant des électrons. Ce coenzyme est présent sous deux formes dans la cellule. NAD+ est un agent d'oxydation et NADH est un agent de réduction. Le transfert d'électron est la principale fonction du NADH.
Structure
Le NAD est dérivé de la vitamine B3 (ou vitamine PP) : la nicotinamide.
La figure 1 présente la structure du NAD+ (forme oxydée). Ce coenzyme n'est pas fixé sur l'apoenzyme, c'est un cosubstrat.
Intérêt en biochimie analytique
Il réside dans une propriété physique particulière : le NAD+ possède un maximum d'absorption en ultraviolet à 260 nm ; la forme réduite (NADH) quant à elle possède deux maxima d'absorption en UV, un premier à 260 nm et un second à 340 nm. En suivant l'absorbance à 340 nm, on pourra suivre l'évolution de la réaction enzymatique, une augmentation d'absorbance indiquant une formation de NADH (la réaction va dans le sens de la réduction du substrat) tandis qu'une diminution d'absorbance indique la consommation de NADH, donc une formation de NAD+ (la réaction va dans le sens de l'oxydation du substrat). La courbe
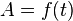
Le coefficient d'extinction molaire de la forme réduite (NADH) à 340 nm vaut 6 220 mol-1·l·cm-1
Mode d'action
Le coenzyme fixe réversiblement un ion H+ et deux électrons sur le noyau nicotinamide (figure 2) en présence d'une enzyme de la classe des oxydoréductases. Ainsi, le réducteur NADH,H+ est une source d'hydrure H-.
Le couple oxydant/réducteur est le suivant : NAD+/NADH,H+
Rôle dans le métabolisme
Le NAD est un coenzyme qui est présent dans toutes les cellules et qui aide les enzymes à transférer les électrons pendant les réactions d'oxydo-réductions du métabolisme de formation de l'ATP.

















































