Peroxyde d'hydrogène - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Peroxyde d'hydrogène | |||||||
|---|---|---|---|---|---|---|---|
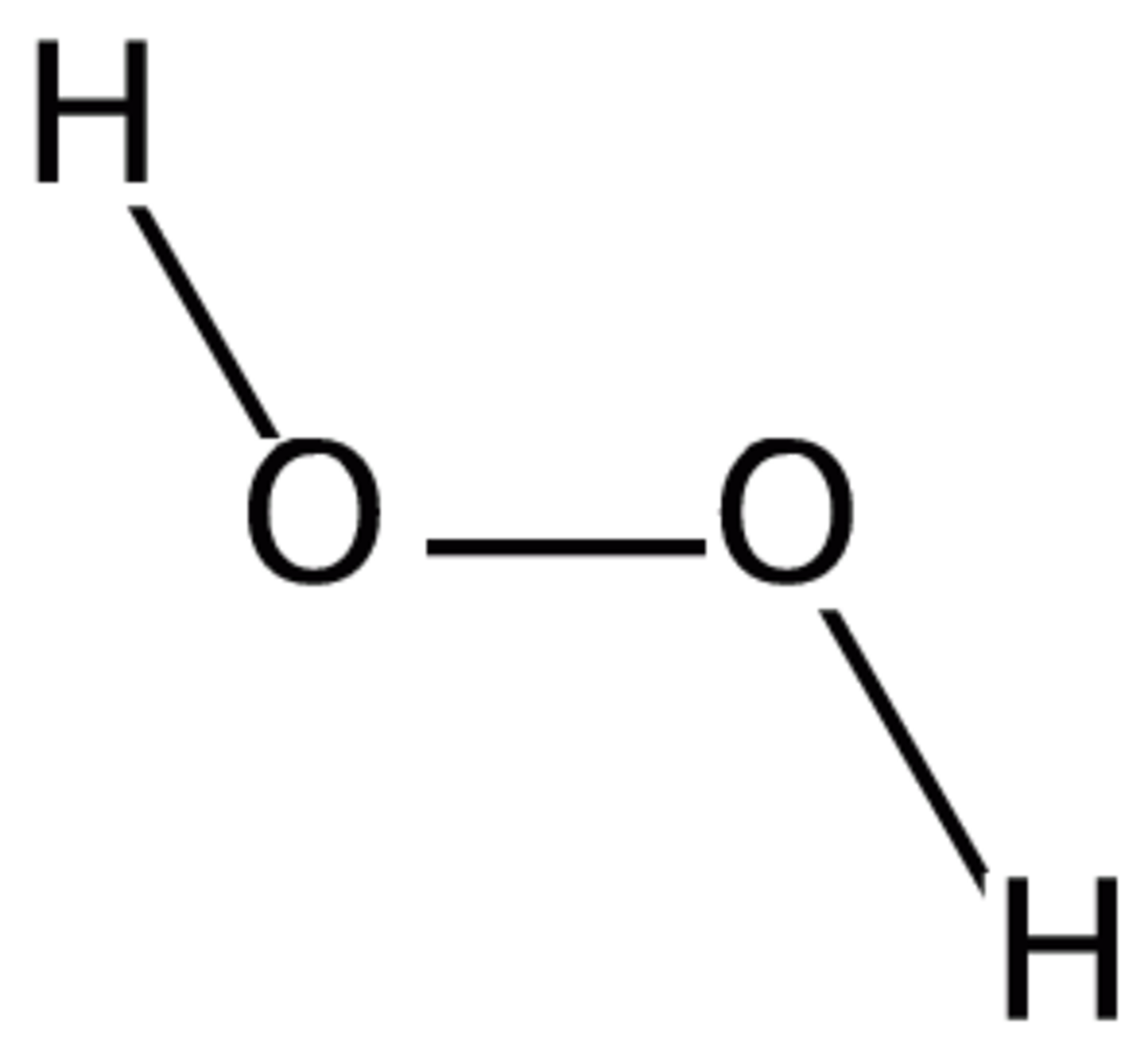
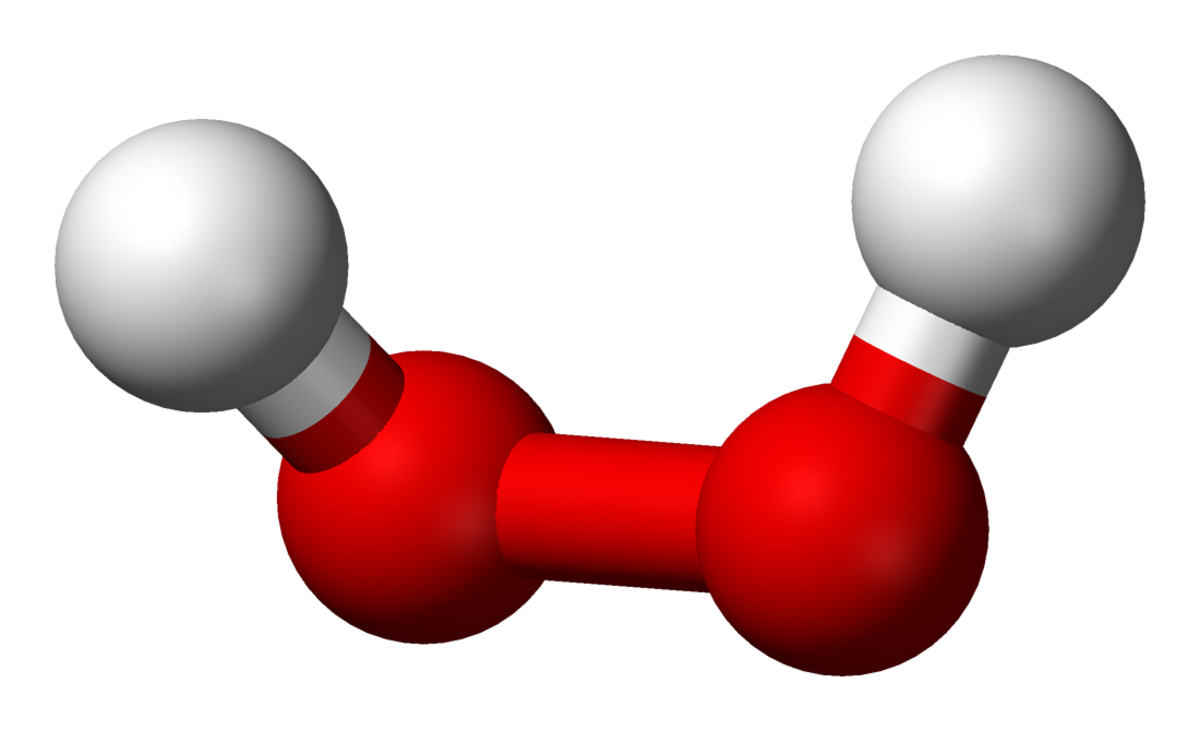
| |||||||
| Général | |||||||
| Nom IUPAC | |||||||
| Synonymes | Eau oxygénée, perhydrol | ||||||
| No CAS | |||||||
| No EINECS | |||||||
| Code ATC | A01, D08, S02 | ||||||
| SMILES | |||||||
| InChI | |||||||
| Apparence | liquide bleu pale (à l'état pur) | ||||||
| Propriétés chimiques | |||||||
| Formule brute | H2O2 | ||||||
| Masse molaire | 34,0147 ± 0,0007 g·mol-1 | ||||||
| Moment dipolaire | 1,573 ± 0,001 D | ||||||
| Susceptibilité magnétique | χm -17,3×10-6 cm3·mol-1 | ||||||
| Diamètre moléculaire | 0,358 nm | ||||||
| Propriétés physiques | |||||||
| T° fusion | -6 °C (10 %m), -33 °C (35 %m), | ||||||
| T° ébullition | 102 °C (10 %m), 108 °C (35 %m), | ||||||
| Solubilité | dans l'eau : miscible, sol. dans l’oxyde de diéthyle, insol. dans l’éther de pétrole, décomposé par de nombreux solvants organiques | ||||||
| Masse volumique | 1,03 g·cm-3 (10 %m, 25 °C), 1,13 g·cm-3 (35 %m, 25 °C), | ||||||
| Pression de vapeur saturante | à 20 °C : 0.2 (90 %), 0.1 (70 %) kPa. 3,9 mbar à 30 °C. 13,2 mbar à 50 °C | ||||||
| Thermochimie | |||||||
| S0 | 232,95 J/mol·K | ||||||
| S0 | 110 J/mol·K | ||||||
| ΔH0 | -136,11 kJ·mol-1 | ||||||
| ΔH0 | -187,5 kJ·mol-1 | ||||||
| ΔH0 | -200 kJ·mol-1 | ||||||
| ΔH° | 51,6 kJ·mol-1 (1 atm, 25 °C) | ||||||
| Propriétés électroniques | |||||||
| 1re énergie d'ionisation | 10,58 ± 0,04 eV (gaz) | ||||||
| Propriétés optiques | |||||||
| Indice de réfraction |
| ||||||
| Précautions | |||||||
| | |||||||
| |||||||
| Phrases R : 5, 8, 20/22, 35, | |||||||
| Phrases S : 1/2, 17, 26, 28, 36/37/39, 45, | |||||||
| | |||||||
>60 % :
20 à 60 % :
8 à 20 % :
| |||||||
| | |||||||
|
0 3 3 OX | |||||||
| | |||||||


| |||||||
| | |||||||


Danger | |||||||
| | |||||||
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme | |||||||
| Inhalation | Irritation sévère, mort possible. | ||||||
| Peau | Blanchit; nettoyer immédiatement. | ||||||
| Yeux | Dangereux ; laver immédiatement pendant un quart d'heure. | ||||||
| Ingestion | Blessure sérieuse, mort possible. | ||||||
| autre | |||||||
| Écotoxicologie | |||||||
| DL | 2 000 mg·kg-1 souris oral >50 000 mg·kg-1 souris i.v. 1 072 mg·kg-1 souris s.c. 880 mg·kg-1 souris i.p. 12 000 mg·kg-1 souris peau | ||||||
| CL | 2000 mg/m³/4 heures rat inhalation | ||||||
| | |||||||
Le peroxyde d'hydrogène (HO), communément appelé eau oxygénée ou encore perhydrol (appellation industrielle), est un composé chimique liquide et visqueux, aux puissantes propriétés oxydantes (il est aussi réducteur). C'est donc un agent blanchissant efficace qui sert de désinfectant et (à haute concentration) d'oxydant ou monergol dans les fusées spatiales. Sa concentration est parfois indiquée en volumes ; une solution à 3 volumes correspond à environ 3 %m.