Allicine - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Allicine | |
|---|---|
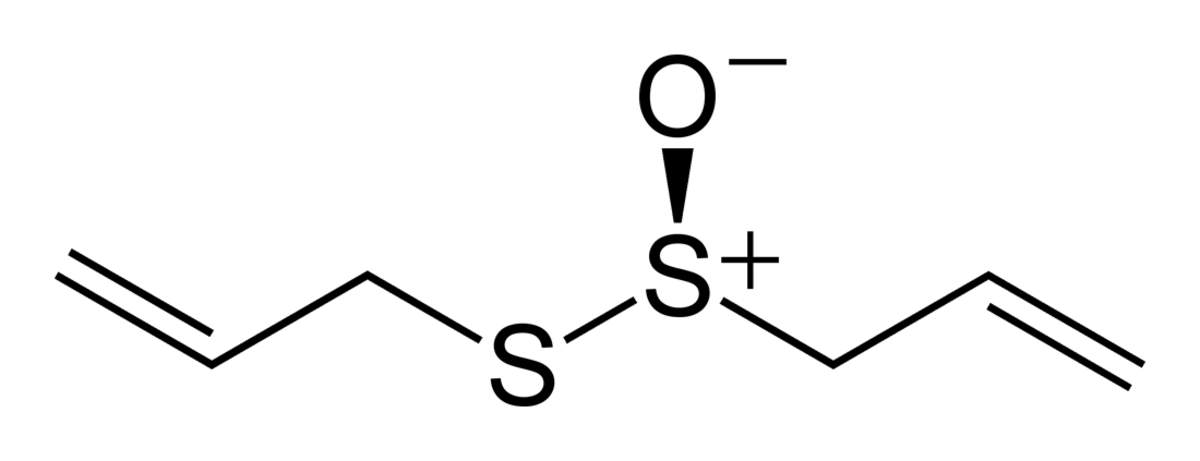
| |
| Général | |
| Nom IUPAC | |
| Synonymes | diallyl thiosulfinate |
| No CAS | |
| PubChem | |
| SMILES | |
| InChI | |
| Apparence | liquide incolore |
| Propriétés chimiques | |
| Formule brute | C6H10OS2 |
| Masse molaire | 162,273 ± 0,016 g·mol-1 |
| Propriétés physiques | |
| T° fusion | <25 °C |
| T° ébullition | décomp |
| Masse volumique | 1,112 g·cm-3 |
| | |
L'allicine est un composé organo-sulfuré abondant dans l'ail sous une forme un peu plus complexe, comme on le trouve également dans les oignons et dans d'autres espèces de la famille des Alliacées. Elle a été isolée pour la première fois et étudiée en laboratoire par Chester J. Cavallito en 1944. C'est un liquide incolore avec une odeur piquante caractéristique. Ce composé présente des propriétés anti-bactérienne et anti-fongique. L'allicine fait partie des mécanismes de défense de certaines Alliacées comme l'ail contre les attaques d'insectes et autres prédateurs.
Structure et occurrence
L'allicine présente un groupe fonctionnel thiosulfinate, R-S(=O)-S-R. Ce composé n'est pas présent dans l'ail tant qu'il ne subit pas de dommages tissulaires. Dans le cas où cela arrive, l'allicine est formée par action de l'enzyme alliinase sur l'alliine. L'allicine est chirale (l'atome de soufre portant l'oxo est asymétrique) et seul l'énantiomère S apparaît naturellement. Le mélange racémique peut être formé par oxydation du disulfure d'allyle (CH2=CH-CH2-S-S-CH2-CH=CH2):
- (SCH2CH=CH2)2 + RCO3H → CH2=CHCH2S(O)SCH2CH=CH2 + RCO2H
avec RCO3H = l'acide méta-chloroperbenzoïque
L'enzyme alliinase est désactivée irréversiblement par un pH inférieur à 3. Ainsi, l'allicine n'est généralement pas produite dans le corps d'un consommateur d'ail frais ou en poudre. De plus, l'allicine est instable, se dégradant en 16 heures à 26 °C.
Bénéfices physiologiques potentiels
De nombreuses études sur l'animal publiées entre 1995 et 2005 indiquent que l'allicine peut :
- réduire l'artériosclérose et les dépôts de graisse dans les artères.
- normaliser la balance lipoprotéinique et réduire la pression sanguine.
- avoir des propriétés anti-thrombose,
- anti-inflammatoire et anti-oxydant d'une certaine importance.
D'autres études ont montré un fort effet oxydatif dans l'intestin nuisible aux cellules intestinales.
En 2009, V. Vaidya, K. Ingold et D. Pratt ont élucidé la manière dont l'allicine agit pour produire ces effets médicaux, notamment en piégeant des radicaux libres délétères. Selon eux, ce sont les acides sulféniques produits par la décomposition de l'allicine qui réagissent extrêmement rapidement avec les radicaux libres en s'y liant. « We suggest that the peroxyl-radical-trapping activity of garlic is primarily due to 2-propenesulfenic acid formed by the decomposition of allicin. » (Nous suggérons que l'activité de piégeage des radicaux peroxyl de l'ail soit essentiellement due à l'acide 2-propénesulfénique formé par la décomposition de l'allicine.).
Activité anti-bactérienne
Un compte-rendu de l'activité bactéricide de l'allicine a été fait par S. Ankri et D. Mirelman en 1999. Du fait de la prévalence croissante de souches de Staphylococcus aureus résistantes à la méticilline (MRSA) dans les hôpitaux et en dehors, il y a un besoin urgent de trouver de nouveaux agents qui puissent être utilisés contre ces bactéries. Dans cette optique, R. Cutler et P. Wilson, en 2004, ont étudié l'effet de l'allicine sur ces bactéries. Ils ont utilisé un nouveau extrait d'allicine aqueux et stable et ont obtenu des résultats très prometteurs :
- Ils ont noté que l'utilisation d'un extrait à base d'eau de l'allicine stabilise les molécules d'allicine.
- Ils ont aussi noté que ceci est vraisemblablement dû à l'établissement d'une liaison hydrogène entre un atome d'hydrogène d'une molécule d'eau avec l'oxygène de l'allicine et aussi qu'il y a peut-être, dans l'ail écrasé, des composants solubles dans l'eau qui déstabilisent cette liaison (probablement, la dilution de ces composants dans l'eau aide à préserver les molécules d'allicine).
- R. Cutler et P. Wilson ont testé l'allicine sur trente isolats clinicaux de MRSA présentant diverses susceptibilités à la mupirocine (82% montrent une résistance intermédiaire ou totale à la mupirocine). Les souches ont été testées par antibiogramme. 88% des souches testées avaient une concentration minimale inhibitive (en) (MIC) pour l'extrait d'allicine à 16 μg·ml-1 et toutes étaient inhibées par la solution à 32 μg·ml-1. De plus, 88% des isolats avaient des concentrations minimales bactériocides (en) (MBC) à 128 μg·ml-1 et toutes ont été tuées à 256 μg·ml-1.
- R. Cutler et P. Wilson ont aussi trouvé qu'une crème aqueuse (en) d'allicine était quelque peu moins efficace que l'extrait d'allicine. Cependant, à 500 μg·ml-1, cette crème était aussi active contre toutes les bactéries testées, à comparer avec la mupirocine dosée à 20 000 μg·ml-1 (c'est-à-dire 20 mg·ml-1) couramment utilisée pour les applications topiques.