Gramicidine - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Gramicidine | ||
|---|---|---|
 | ||
| Général | ||
| Synonymes | Bacillus brevis gramicidin D | |
| No CAS | ||
| No EINECS | ||
| Code ATC | R02 | |
| DrugBank | ||
| Propriétés chimiques | ||
| Formule brute | C99H140N20O17 | |
| Masse molaire | 1 882,2947 ± 0,0981 g·mol-1 | |
| Propriétés physiques | ||
| Solubilité | 5×10−7 mol·l-1 | |
| Précautions | ||
| | ||
| ||
| Phrases R : 20/21, 36/37/38, | ||
| Phrases S : 26, 36, | ||
| | ||
La Gramicidine est un mélange d'antibiotiques, aussi nommé gramicidine D d'après René Dubos qui découvrit ce peptide à la fin des années 1930. Ce mélange est composé de gramicidine A (80%), B (6%) et C (14%), et est isolé dans la bactérie Bacillus brevis. C'est un pentadécapeptide composé de 15 acides aminés que l'on retrouve sous forme de chaine linéaire, contrairement à la gramicidine S cyclique. La gramicidine est considérée comme le premier antibiotique naturel découvert et commercialisé.
Histoire
En 1939, le microbiologiste franco-américain René Dubos isole la tyrocidine, et démontre ensuite avec Rollin D. Hotchkiss que cette substance est un mélange composé de tyrocidine et de gramicidine.
Bien que des injections intrapéritonéales sur des souris aient montré que celles-ci étaient protégées contre des infections bactériennes fatales, la gramicidine D est toxique lorsqu'elle est administrée par voie intraveineuse, et ne peut donc être utilisée pour traiter des infections systémiques. Néanmoins, la gramicidine D fut utilisée comme pommade durant la Seconde Guerre mondiale pour traiter des blessures et des ulcères et est encore utilisée dans certaines préparations.
Au cours de sa quatrième année d'étude en chimie à l'université d'Oxford (1946-1947), Margaret Thatcher travaille sur la cristallisation de la gramicidine B, sous la direction de Dorothy Hodgkin (prix Nobel de chimie en 1964).
Mode d'action
Les gramicidines linéaires sont une famille d'antibiotiques de type porine dont l'activité antibactérienne s'exerce par l'augmentation de la perméabilité cationique de la membrane plasmique de la bactérie cible. Cette perméabilité est due à la formation de canaux au travers de la bicouche lipidique, du fait de la structure en hélice de la gramicidine dimérique.
Activité antibactérienne
La gramicidine est active contre les bactéries à gram positif, excepté la bactérie Bacilli, et contre les organismes à gram négatif, comme les bactéries Neisseria. Cette activité antibactérienne est utilisée comme antimicrobien, antimycosique et antiprotozoaire (en), et ce depuis sa découverte. Divers agents pathogènes de maladies sexuellement transmissibles comme Neisseria gonorrhoeae, Candida albicans et Chlamydia trachomatis sont connus pour être sensible à cet antibiotique.
Activité antivirale
La gramicidine est étudiée comme antiviral, et présente une activité contre le VIH et l'herpes à des concentrations de l'ordre du nanogramme.
Structure
Structure primaire
Les gramicidines se présentent sous la forme de pentadécapeptides linéaires, de masse molaire d'environ 1900 g·mol−1. La structure primaire est constituée de 15 acides aminés, alternant les conformations L- et D-, avec un groupement formyl en position N-terminale et une fonction alcool en position C-terminale :
Dans le mélange gramicidine D, l'espèce prédominante est la gramicidine A (80%), où l'acide aminé en position 11 (dénoté X dans la séquence) se trouve être un résidu -Trp. Les gramicidines B et C présentent elles respectivement des résidus -Phe et -Tyr en position 11. De plus, il faut noter qu'en position 1, le résidu -Val est remplacé par le -Ile dans 5 à 20% des molécules.
Cette séquence est l'une des plus hydrophobe connue, et par conséquence la solubilité dans l'eau de la gramicidine est très faible, de l'ordre de 5×10−7 mol·l-1.
Structure secondaire
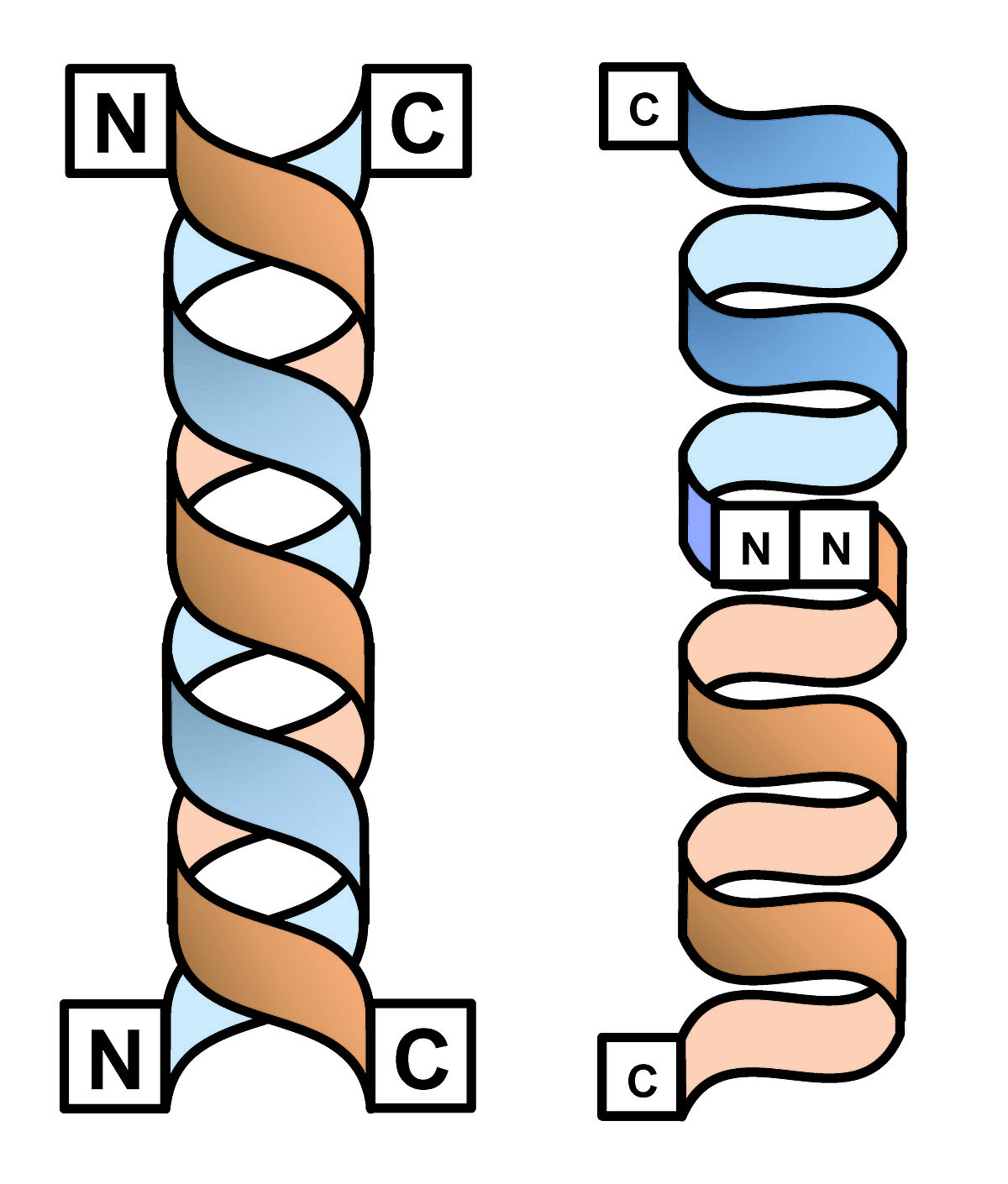
La particularité de l'alternance d'acides aminés L- et D- dans la structure primaire de la gramicidine implique une grande sensibilité quant à l'environnement dans lequel est placé le peptide. Deux formes principales ont été observé : la forme dimérique en simple hélice et la forme dimérique en double hélice:
- Dans la forme double hélice, les deux chaînes polypeptidiques forment entre elles une série de liaisons hydrogène intermoléculaires sur toute la longueur des chaînes (sous la forme de feuillets bêta parallèles ou antiparallèles) et sont enroulées sous forme d'hélice. Cette structure est décrite comme structure ππ5,6 ou ππ6,4 (l'exposant indiquant le nombre d'acide aminé par tour dans chaque hélice monomérique). La version antiparallèle de la double hélice est désignée comme étant la forme poreuse.
- Dans la forme simple hélice, chacune des deux chaînes polypeptidiques forment aussi des liaisons hydrogène, mais principalement de manière intramoléculaire. Les acides aminés en position N-terminale forment six liaisons hydrogène intermoléculaires qui permettent d'associer les deux monomères. Cette structure est décrite comme structure ββ6,3 (de même que précédemment, l'exposant indiquant le nombre d'acide aminé par tour dans chaque hélice monomérique). Cette forme est désignée comme étant la forme canal. Le diamètre de ce canal est de l'ordre de 4 Å, et la longueur du dimère atteint 26 Å, du même ordre de grandeur que la partie hydrophobe de la bicouche lipidique de la membrane plasmique.