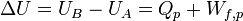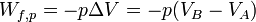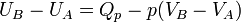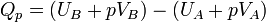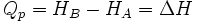Enthalpie - Définition
L'enthalpie (du préfixe en- et du grec thalpein: chauffer) est une fonction d'état de la thermodynamique, dont la variation permet d'exprimer la quantité de chaleur mise en jeu pendant la transformation isobare d'un système thermodynamique au cours de laquelle celui-ci reçoit ou fournit un travail mécanique.
Définition
Considérons une transformation monobare au cours de laquelle le système passe d’un état A à un état B d’équilibres en échangeant de la chaleur
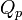
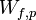
Le premier principe permet d’écrire :
U étant la fonction d'état énergie interne
À pression constante le travail des forces de pression est égal à :
D'où :
On définit ainsi une nouvelle fonction d’état, la fonction enthalpie
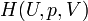
|
|
Il s’ensuit que :
Par conséquent, à pression constante, la chaleur mise en jeu, qui n’est pas une fonction d’état, devient égale à la variation de la fonction d’état enthalpie H. La variation de cette fonction ne dépend que de l’état final et de l’état initial du système et est indépendante du chemin suivi par la transformation.
C’est l’intérêt de l’application de la fonction enthalpie dans les cas très courants de transformations effectuées à l’air libre, à pression atmosphérique constante.
Cette propriété est à la base de la calorimétrie à pression constante. Par abus de langage on confond souvent les termes chaleur et enthalpie.
Propriétés
L'enthalpie a la dimension d'une énergie, et s'exprime en joules dans le système International.
La propriété mathématique induite pour toute fonction d'état implique que sa différentielle est totale exacte c'est-à-dire qu'elle est égale à la somme des différentielles partielles par rapport à chaque variable.
Différentielle de l'enthalpie
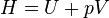
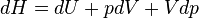
- Appliquons le premier principe
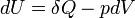
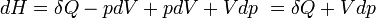
- Appliquons le second principe
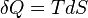
d'où
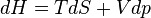
Réaction Isenthalpique
Une réaction isenthalpique est une réaction où l'enthalpie ne varie pas. Un bon exemple est la détente de Joule-Thomson