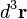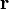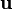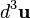Équation de Boltzmann - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
L'équation de Boltzmann (1872) est une équation intégro-différentielle de la théorie cinétique qui décrit l'évolution d'un gaz peu dense hors d'équilibre. Elle permet notamment de démontrer le théorème H, et d'étudier la relaxation du gaz d'un état d'équilibre local vers l'équilibre global caractérisé par la distribution de Maxwell des vitesses.
La première solution analytique complète a été obtenue dans le cas des interactions de type « sphères dures » par Ukai dans les années 1970, mais seulement pour des solutions proches de l'équilibre. La plus grande avancée reste la théorie des solutions renormalisées de Ronald DiPerna et du médaille Fields Pierre-Louis Lions qui fournit l'existence de solution, même loin de l'équilibre. Leur régularité et unicité reste un problème ouvert très important.
Modèle mécanique du gaz
On considère un gaz de sphères dures constitué de N atomes identiques de masse m et de rayon r. Ces atomes :
- sont confinés dans une boîte ;
- voyagent à vitesse constante entre les collisions ;
- rebondissent élastiquement les uns sur les autres ;
- rebondissent élastiquement sur les parois de la boîte.
Équation de Boltzmann non-relativiste
Opérateur de Liouville non-relativiste
Soit un gaz placé dans un champ de force externe macroscopique
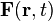
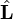
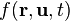
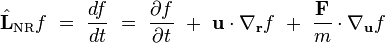
Équation de Boltzmann non-relativiste
Du fait des collisions, la fonction de distribution à une particule possède une variation totale non-nulle ; elle obéit à l'équation de Boltzmann :
![\hat{\mathbf{L}}[f] \ = \ \mathbf{C}[f]](https://static.techno-science.net/illustration/Definitions/autres/3/39b7a251d58e83b07a31534a45a9db1d_d0955e339453536e6d2bb49a8a395a5d.png)
où
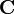
Théorème de Lanford
Limite de Boltzmann-Grad
La limite dite de Boltzmann-Grad consiste à prendre la limite conjointe :
- d'un nombre d'atomes
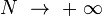
- d'un rayon
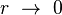
en maintenant le produit
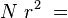
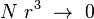
Théorème de Lanford (1973)
Lanford a démontré rigoureusement qu'un gaz de sphères dures dilué dans
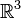
En dépit de cette restriction sur la durée, ce théorème mathématique rigoureux est très important conceptuellement, puisque l'équation de Boltzmann entraine le théorème H, à propos duquel Boltzmann fut accusé de pratiquer des « mathématiques douteuses ». Il n'en demeure pas moins qu'il reste à démontrer que ce résultat reste vrai pour des temps macroscopiques, ainsi que lorsque les atomes sont confinés dans une boite.
Fonction de distribution à une particule
On note
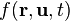
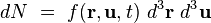
représente le nombre de molécules de gaz situées à l'instant t dans un petit volume d'espace