Isothiocyanate d'allyle - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Isothiocyanate d'allyle | |||
|---|---|---|---|
| |||
| Général | |||
| Nom IUPAC | |||
| No CAS | |||
| No EINECS | |||
| PubChem | |||
| SMILES | |||
| InChI | |||
| Apparence | liquide huileux incolore | ||
| Propriétés chimiques | |||
| Formule brute | C4H5NS | ||
| Masse molaire | 99,154 ± 0,009 g·mol-1 | ||
| Propriétés physiques | |||
| T° fusion | -103,15 °C | ||
| T° ébullition | 151,9 °C | ||
| Masse volumique | 1,02 g·cm-3 | ||
| T° d’auto-inflammation | 250 °C (décomposition) | ||
| Point d’éclair | 48 °C | ||
| Thermochimie | |||
| Cp | 156,9 J·mol-1·K-1 (liquide,16,85 °C) | ||
| Précautions | |||
| | |||
| |||
| Phrases R : 10, 24/25, 36/37/38, 50/53, | |||
| Phrases S : 36/37, 45, 61, | |||
| | |||
| |||
| | |||
|
2 3 0 | |||
| Écotoxicologie | |||
| DL | 308 mg·kg-1 (souris, oral) 80 mg·kg-1 (souris, s.c.) | ||
| LogP | 2,15 | ||
| | |||
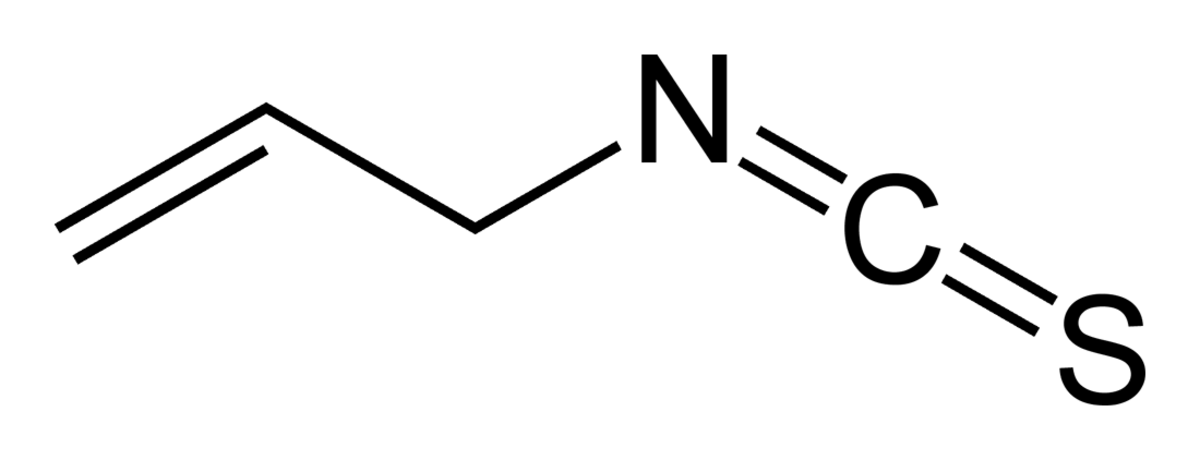
L'isothiocyanate d'allyle est un composé organo-sulfuré de formule semi-développée CH2CHCH2NCS. Cette huile incolore est responsable du goût piquant de la moutarde, du raifort et du wasabi. Elle est peu soluble dans l'eau mais beaucoup plus dans la plupart de solvants organiques
Biosynthèse et fonctions biologiques
L'isothiocyanate d'allyle provient des graines de moutarde noire (Brassica nigra) ou de moutarde brune (Brassica juncea). Quand ces graines sont broyées, la myrosinase, une enzyme est libérée et réagit sur la sinigrine, un glucosinolate pour donner de l'isothiocyanate d'allyle.
L'isothiocyanate d'allyle sert aux plantes comme une défense contre les herbivores. Comme il est aussi toxique pour la plante elle-même, il est stocké sous la forme inoffensive du glucosinolate et de l'enzyme qui sont séparés. Quand un animal mâche la plante, l'isothiocyanate d'allyle est libéré et repousse l'animal.
Sécurité
L'isothiocyanate d'allyle est moyennement toxique avec un LD50 de 151 mg·kg-1 mais il est dangereusement lacrymogène.
Production et synthèse
L'isothiocyanate d'allyle est produit commercialement par la réaction du chlorure d'allyle avec du thiocyanate de potassium :
- CH2=CHCH2Cl + KSCN → CH2=CHCH2NCS + KCl.
Le produit obtenu de cette façon est aussi connu comme "huile de moutarde synthétique". L'isothiocyanate d'allyle peut aussi être obtenu par distillation à sec de graines de moutarde. Le produit obtenu par ce procédé est aussi appelé "huile de moutarde volatile" et sa pureté est autour de 92%. Il est principalement utilisé comme agent de saveur et d'assaisonnement alimentaire. L'isothiocyanate d'allyle synthétique est utilisé comme insecticide, antibactérien ou nématicide et, dans certains cas, pour protéger les cultures.
L'hydrolyse de l'isothiocyanate d'allyle donne de l'allylamine.




















































