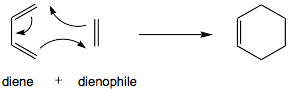Alcène - Définition
La liste des auteurs de cet article est disponible ici.
Propriétés physiques
Les alcènes ont des températures d'ébullition un peu plus basses que celles des alcanes correspondants car les forces de van der Waals sont plus faibles ; en effet, une double liaison prend plus d'espace qu'une simple liaison, donc les molécules s'empilent de façon moins compacte et les forces intermoléculaires sont moins importantes. Il en résulte qu'il faut fournir moins d'énergie pour les rompre : les températures d'ébullition sont plus basses. Ils brûlent avec une flamme claire.
Les alcènes sont gazeux jusqu'au butène, puis liquides et enfin solides à partir de C16. Leur solubilité, médiocre dans l'eau, est bonne dans l'alcool et l'éther.
Réaction de Diels-Alder
La réaction de Diels-Alder est un cas particulier des cycloadditions entre systèmes π. Il s'agit d'une addition d'un réaction entre un diène conjugué, et un dièneophile, un alcène substitué. L'exemple-type de cette réaction est la réaction entre le buta-1,3-diène et l'éthylène pour former le cyclohexène :